Quelle est la différence entre le lactate et le lactate déshydrogénase
Le différence clé entre le lactate et la lactate déshydrogénase Est-ce que le lactate est la forme déprotonée d'acide lactique, tandis que la lactate déshydrogénase est une enzyme qui est importante pour convertir le lactate en pyruvate.
L'acide lactique est un composé acide organique ayant la formule chimique CH3CH (OH) COOH. Nous pouvons l'isoler comme une substance solide blanche qui est miscible avec de l'eau. La solution aqueuse est incolore. Il existe des sources naturelles d'acide lactique, et la production peut être effectuée artificiellement, ainsi que. La base conjuguée de l'acide lactique est un anion lactate. Le lactate se convertit en pyruvate en présence d'enzyme de lactate déshydrogénase.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que le lactate
3. Qu'est-ce que la lactate déshydrogénase
4. Lactate vs lactate déshydrogénase sous forme tabulaire
5. Résumé - lactate vs lactate déshydrogénase
Qu'est-ce que le lactate?
Le lactate est un anion et la base conjuguée de l'acide lactique. Il s'agit d'un anion d'acide monocarboxylique hydroxy qui se forme à partir de la déprotonation du groupe carboxy dans l'acide lactique. Généralement, nos cellules musculaires, nos globules rouges, notre cerveau et d'autres tissus peuvent produire cet anion pendant le processus de production d'énergie anaérobie. En d'autres termes, le lactate est le produit final du métabolisme anaérobie, et il génère dans les muscles squelettiques, le cerveau, les érythrocytes, la peau et l'intestin comme produit d'élimination par la gluconéogenèse dans le foie et l'oxydation complète. Par conséquent, l'anion lactate peut être trouvé dans de faibles niveaux dans notre sang.
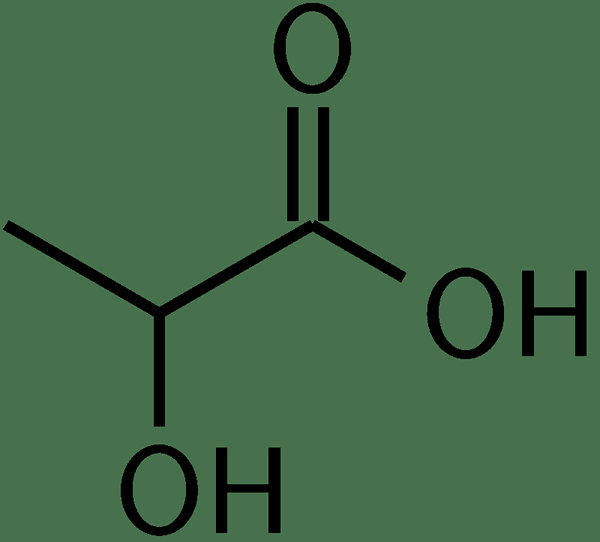
Figure 01: La structure chimique de l'acide lactique
Cependant, la formation accrue d'anion lactate ou la diminution de l'élimination de cet anion peut provoquer une acidose lactique. Il existe deux types en tant qu'acidose lactique de type A et acidose lactique de type B. Parmi eux, l'acidose lactique de type A se produit en raison de l'augmentation de la formation de lactate par l'hypoxie tissulaire. L'acidose lactique de type B se produit en raison des ingestion de médicaments et de toxines, ce qui entraîne une production accrue de formation.
Qu'est-ce que la lactate déshydrogénase?
La lactate déshydrogénase est une enzyme qui peut convertir le lactate en pyruvate. Nous pouvons désigner ce nom comme Enzyme LDH ou Enzyme LD. Nous pouvons trouver cette enzyme presque dans toutes les cellules vivantes. De plus, cette enzyme peut catalyser à la fois les réactions vers l'avant et les inverses de la conversion du lactate en pyruvate.
Cette enzyme convertit le lactate en pyruvate et vers le dos en convertissant NAD + en NADH. En d'autres termes, une enzyme de déshydrogénase peut transférer un hydrure d'une molécule à une autre. Nous pouvons trouver une enzyme de lactate déshydrogénase dans les tissus corporels, y compris les cellules sanguines et les muscles cardiaques parce que cette enzyme est libérée lorsque les tissus sont endommagés.

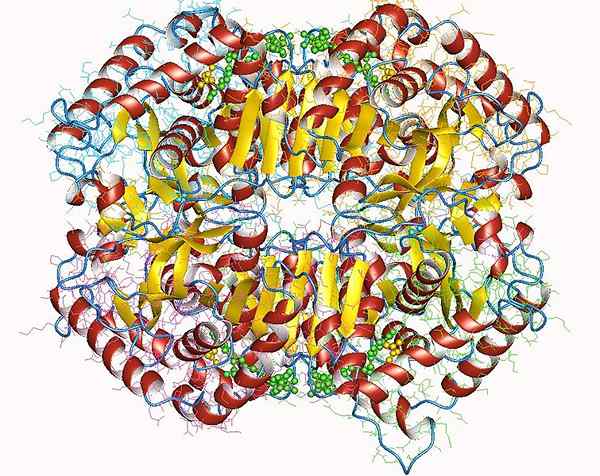
Figure 02: lactate déshydrogénase
Lorsqu'il y a une concentration élevée de lactate déshydrogénase, l'enzyme de lactate déshydrogénase a tendance à présenter une inhibition de rétroaction qui provoque une diminution de la conversion du pyruvate en lactate. De plus, cette enzyme peut catalyser la déshydrogénation du 2-hydroxybutyrate.
Lorsque vous envisagez la structure chimique de l'enzyme de lactate déshydrogénase, chez l'homme, cette enzyme utilise son (193) comme accepteur de proton et fonctionne avec les sites de liaison de coenzyme et de substrat. Ce site actif de son (193) se trouve également dans l'enzyme LDH de nombreux autres animaux.
Quelle est la différence entre le lactate et le lactate déshydrogénase?
La base conjuguée de l'acide lactique est un anion lactate. Le lactate se convertit en pyruvate en présence d'enzyme de lactate déshydrogénase. La principale différence entre le lactate et la lactate déshydrogénase est que le lactate est la forme déprotonée d'acide lactique, tandis que la lactate déshydrogénase est une enzyme qui est importante pour convertir le lactate en pyruvate.
L'infographie suivante répertorie les différences entre le lactate et la lactate déshydrogénase sous forme tabulaire pour une comparaison côte à côte.
Résumé - lactate vs lactate déshydrogénase
La base conjuguée de l'acide lactique est un anion lactate. Le lactate se convertit en pyruvate en présence d'enzyme de lactate déshydrogénase. La principale différence entre le lactate et la lactate déshydrogénase est que le lactate est la forme déprotonée d'acide lactique, tandis que la lactate déshydrogénase est une enzyme qui est importante pour convertir le lactate en pyruvate.
Référence:
1. «Lactate." Centre national d'information sur la biotechnologie. Base de données de composés PubChem, U.S. Bibliothèque nationale de médecine.
Image gracieuseté:
1. «7 Milchsäure» par Schemiker (Talk) - Propre travaux (domaine public) via Commons Wikimedia
2. «1i10» par les auteurs de dépôt: lire, j.UN., Hiver, V.J., Eszes, c.M., Sessions, R.B., Brady, R.L.; Visualisation Auteur: Utilisateur: Astrojan - RCSB (CC par 3.0) via Commons Wikimedia


