Quelle est la différence entre Zwitterion et Dipôle
Le Différence clé entre Zwitterion et Dipôle Est-ce que Zwitterion est une molécule neutre ayant des charges électriques intérieures, tandis que le dipôle est la présence de extrémités chargées positives et négatives ou de pôles magnétiques nord et sud.
Les termes zwitterion et dipôle sont liés les uns aux autres en fonction de la présence de deux phénomènes opposés dans le même système. Par exemple, les zwitterions contiennent des charges positives et négatives dans la même molécule, tandis que le dipôle électrique contient des extrémités chargées positives et négatives sur le même champ électrique.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que Zwitterion
3. Qu'est-ce que le dipôle
4. Zwitterion vs dipôle sous forme tabulaire
5. Résumé - Zwitterion vs Dipôle
Qu'est-ce que Zwitterion?
Zwitterion, ou le sel intérieur, est une molécule composée d'un nombre égal de groupes fonctionnels chargés positifs et négatifs. En d'autres termes, une Zwitterion contient des groupes cationiques et anioniques dans la même molécule en quantités égales. Le terme zwitterion s'accompagne principalement d'acides aminés, mais il est également utilisé avec des molécules d'acide sulfamique, de l'acide anthranilique et de la protonation EDTA.
Par exemple, les acides aminés dans une solution aqueuse forment un équilibre chimique entre la molécule d'acide aminé parentale et le zwitterion. Cet équilibre chimique se forme à deux étapes. À la première étape, un proton est transformé du groupe carboxyle de la molécule d'acide aminé en molécule d'eau, formant l'ion hydronium et les espèces chimiques chargées négativement d'acide aminé. Par la suite, dans la deuxième étape, un proton est transféré de l'ion hydronium au groupe amine de la même molécule d'acide aminé, ayant maintenant une charge négative. Cela constitue une charge positive sur le groupe amine alors qu'il y a une charge négative sur le groupe carboxyle. Par conséquent, une réaction d'isomérisation a lieu, formant un zwitterion.
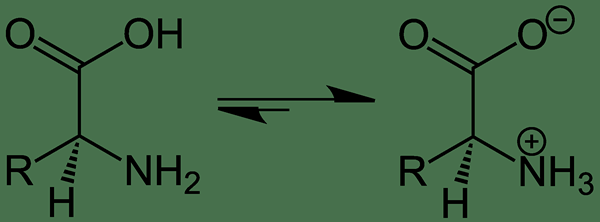
Figure 01: La formation d'une zwitterion dans une solution contenant des molécules d'acide aminé
Généralement, il n'est pas possible d'étudier l'équilibre entre le composé et son zwitterion expérimentalement. Cependant, nous pouvons obtenir des informations en utilisant le contexte théorique.
Qu'est-ce que le dipôle?
Le terme dipôle se réfère au dipôle électrique ou magnétique qui est utilisé dans l'électromagnétisme. Les dipôles électriques traitent de la séparation des charges opposées (charges positives et négatives) dans tout système électromagnétique. E.g. une paire de charges électriques ayant une ampleur égale et des signes de charge opposée et sont séparés par une petite distance. Dans un dipôle magnétique, nous pouvons observer une circulation fermée d'un système de courant électrique.

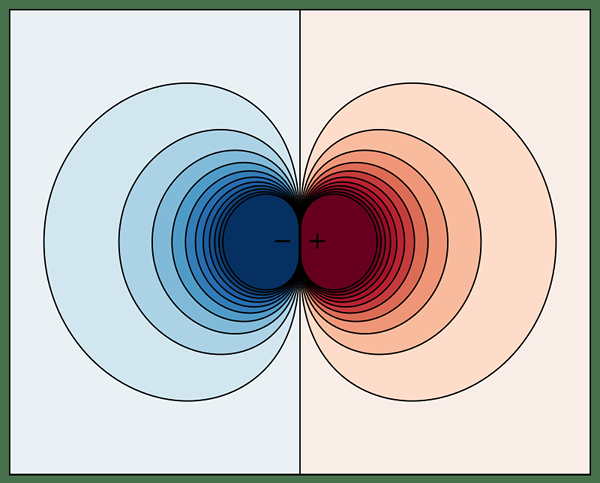
Figure 02: Dipôle
Qu'il s'agisse d'un dipôle électrique ou d'un dipôle magnétique, nous pouvons les caractériser par moment dipolaire. Le moment dipolaire est une quantité vectorielle. Dans un simple dipôle électrique, le moment dipolaire dirige de la charge négative vers la charge positive. L'ampleur de ce moment dipolaire est égale à la force de chacune de ces charges, fois la distance de séparation entre ces charges. De même, il y a un moment dipolaire magnétique pour les dipôles magnétiques qui pointent à travers la boucle de courant magnétique. Il a une ampleur égale au courant dans la boucle fois la zone de la boucle.
De plus, il peut y avoir d'autres classifications pour les dipôles; Par exemple, il existe un dipôle physique qui contient deux charges ponctuelles égales et opposées; Le dipôle point est la limite que nous pouvons obtenir en laissant la séparation devenir nul tout en gardant un moment dipolaire fixe, etc.
Quelle est la différence entre Zwitterion et Dipôle?
Les termes zwitterion et dipôle sont liés les uns aux autres en fonction de la présence de deux phénomènes opposés dans le même système. Cependant, la principale différence entre Zwitterion et Dipôle est que Zwitterion est une molécule neutre ayant des charges électriques intérieures, tandis que le dipôle est la présence de extrémités chargées positives et négatives ou de poteaux magnétiques nord et sud.
Le tableau suivant présente la différence entre Zwitterion et Dipôle en détail.
Résumé - Zwitterion vs Dipôle
Les termes zwitterion et dipôle sont liés les uns aux autres en fonction de la présence de deux phénomènes opposés dans le même système. La principale différence entre Zwitterion et Dipôle est que Zwitterion est une molécule neutre ayant des charges électriques intérieures tandis que le dipôle est la présence de extrémités chargées positives et négatives ou de pôles magnétiques nord et sud.
Référence:
1. Helmenstine, Anne Marie. «Définition dipolaire en chimie et physique."Thoughtco, août. 29, 2020.
Image gracieuseté:
1. «Formules structurelles zwitterion acide aminé V.1 ”par Jü - Propre travaux (CC0) via Commons Wikimedia
2. «DipoleContourpoint» par Geek3 - Propre travaux (CC BY-SA 4.0) via Commons Wikimedia


