Différence entre l'isomorphisme et le polymorphisme
Différence clé - l'isomorphisme contre Polymorphisme
Les composés peuvent exister sous différentes formes dans la nature. Ces différentes formes peuvent être des morphologies ou des structures différentes différentes. La structure d'un composé chimique détermine les propriétés physiques de ce composé. Parfois, les propriétés chimiques sont également déterminées par la structure. Le «morphisme» est un terme utilisé pour nommer le terme «morphologie». Il décrit l'apparence externe d'un composé. Les termes isomorphisme et polymorphisme sont utilisés pour décrire ces apparences externes. Le polymorphisme signifie l'existence d'un composé sous plus d'une forme cristalline. L'isomorphisme est l'existence de deux ou plusieurs composés ayant la même morphologie. Le différence clé entre l'isomorphisme et le polymorphisme est que L'isomorphisme fait référence à la présence de deux ou plusieurs composés avec des morphologies identiques tandis que le polymorphisme se réfère à la présence de morphologies différentes de la même substance.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que l'isomorphisme
3. Qu'est-ce que le polymorphisme
4. Comparaison côte à côte - isomorphisme vs polymorphisme sous forme tabulaire
5. Résumé
Qu'est-ce que l'isomorphisme?
L'isomorphisme fait référence à la présence de deux ou plusieurs composés avec des morphologies identiques. Cela signifie l'existence de la même structure cristalline dans différents composés. Ces composés sont appelés substances isomorphes. Les substances isomorphes ont presque la même forme et la même structure.
Ces composés ont le même rapport entre les atomes présents dans ces composés. Cela indique que les formules empiriques des substances isomorphes sont identiques. Mais les propriétés physiques des substances isomorphes sont différentes les unes des autres car elles ont des combinaisons atomiques différentes. Ex: masse, densité, réactivité chimique sont quelques-unes des propriétés physiques qui diffèrent en substances isomorphes. Considérons quelques exemples afin de comprendre ce qu'est l'isomorphisme en chimie.
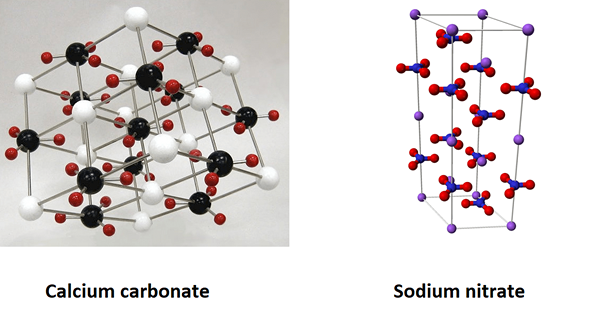
- Carbonate de calcium (CACO3) et le nitrate de sodium (nano3).

Figure 01: La comparaison du carbonate de calcium et du nitrate de sodium sous forme de substances isomorphes
Le carbonate de calcium et le nitrate de sodium sont de forme trigonale. Le rapport atomique des atomes présents dans chaque composé est de 1: 1: 3. Mais ces composés ont des propriétés physiques et chimiques différentes. Leurs masses molaires sont également différentes les unes des autres (carbonate de calcium = 100 g / mol et nitrate de sodium = 85 g / mol).
- Phosphate de sodium (Na3Pote4) et l'arsénéate de sodium (Na3ASO4).
Ces composés existent en forme tétraédrique, et la formule empirique de ces composés a le rapport atomique 3: 1: 4. Mais ils ont des propriétés chimiques et physiques différentes.
Qu'est-ce que le polymorphisme?
Le polymorphisme fait référence à la présence de différentes morphologies de la même substance. La substance qui montre le polymorphisme est connue sous le nom substances polymorphes. Ici, un composé particulier existe sous différentes formes et formes cristallines.
La substance polymorphe montre des similitudes et des différences basées sur la structure. Mais la plupart du temps, les propriétés chimiques sont les mêmes car c'est le même composé qui existe sous différentes formes. Mais les propriétés physiques sont différentes. , Le caco3 (carbonate de calcium) existe sous forme orthorhombique ou sous forme hexagonale.
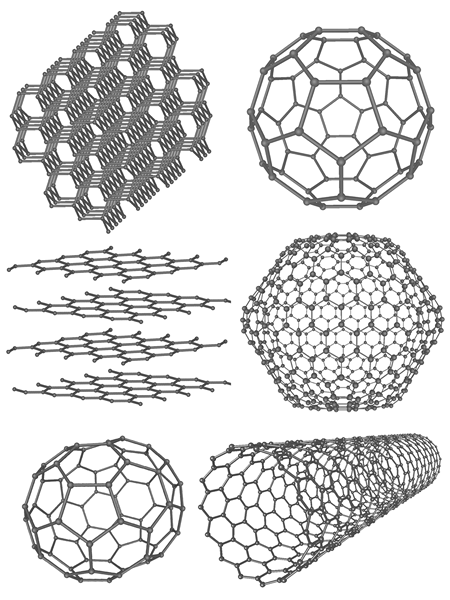
Figure 02: Allotropes de carbone
L'allotropie est un terme connexe au polymorphisme. L'allotropie fait référence au polymorphisme d'un élément particulier. Les composés montrant l'allotropy sont appelés allotropes. Les allotropes se produisent lorsqu'un élément forme une structure cristalline avec des arrangements différents. Par exemple, les allotropes de formulaire de carbone tels que le diamant ou le graphite. Ces allotropes ont des propriétés chimiques et physiques différentes.
Quelle est la différence entre l'isomorphisme et le polymorphisme?
Isomorphisme vs polymorphisme | |
| L'isomorphisme fait référence à la présence de deux ou plusieurs composés avec des morphologies identiques. | Le polymorphisme fait référence à la présence de différentes morphologies de la même substance. |
| Forme | |
| Les substances isomorphes ont des formes identiques. | Les substances polymorphes ont des formes différentes. |
| Composé | |
| L'isomorphisme concerne deux ou plusieurs composés différents. | Le polymorphisme décrit les différentes formes du même composé ou élément. |
| Dans les éléments | |
| L'isomorphisme est absent dans les éléments. | Le polymorphisme est présent dans les éléments. |
| Ratio atomique | |
| Les substances isomorphes ont la même ration atomique dans la formule empirique. | Les substances polymorphes ont des rapports atomiques similaires ou différents. |
Résumé - Isomorphisme contre Polymorphisme
L'isomorphisme et le polymorphisme expriment deux idées opposées. La différence entre l'isomorphisme et le polymorphisme est que l'isomorphisme fait référence à la présence de deux ou plusieurs composés avec des morphologies identiques tandis que le polymorphisme se réfère à la présence de morphologies différentes de la même substance.
Référence:
1.«La cristallisation et le polymorphisme.»American Chemical Society. Disponible ici
2.«L'isomorphisme (cristallographie).»Wikipedia, Wikimedia Foundation, 17 février. 2018. Disponible ici
3.«Allotropy.»Wikipedia, Wikimedia Foundation, 3 mars. 2018. Disponible ici
Image gracieuseté:
1.'Caco3-calcite-structure'By tem5psu - propre travail, (cc by-sa 4.0) via Commons Wikimedia (modifié)
2.«Sodium-nitrate-unit-cell-3d-balls» Ben Mills - propre travail, (domaine public) via Commons Wikimedia (modifié)
3.'Allotropes of Carbon'by mstroeck (talk) (uploads) - propre travail, (CC by-sa 3.0) via Commons Wikimedia


