Différence entre 18 Electron Rule et Ean Rule

Le différence clé entre 18 et la règle d'électrons et la règle Ean est que la règle de 18 électrons indique que Il doit y avoir 18 électrons de valence autour du métal dans des complexes de coordination afin de devenir stable alors que La règle EAN décrit qu'un atome métallique doit obtenir la configuration électronique du gaz noble présent dans la même période afin de devenir stable.
La règle de 18 électrons et la règle EAN indiquent que l'obtention d'une configuration d'électrons à gaz noble rend un atome métallique stable. Selon la règle des 18 électrons, nous devons considérer les électrons de valence de l'atome métallique alors que selon la règle EAN, nous devons considérer toute la teneur en électrons de l'atome métallique. Cependant, ces deux termes sont principalement discutés sous des composés organométalliques où nous pouvons trouver des complexes de coordination ayant un atome de métal de transition au centre, entouré de ligands. Ces termes sont appliqués à l'atome métallique central pour voir si ces complexes sont stables ou non.
CONTENU
1. Aperçu et différence clé
2. Quelle est la règle des 18 électrons
3. Qu'est-ce que la règle Ean
4. Comparaison côte à côte - Règle d'électrons vs règne dans la forme tabulaire
5. Résumé
Quelle est la règle des 18 électrons?
18 La règle d'électrons est un concept en chimie que nous utilisons pour déterminer la stabilité d'un atome métallique dans un composé organométallique en déterminant s'il dispose de 18 électrons de valence. C'est une version simplifiée de la règle EAN. Dans la règle EAN, nous devons considérer le nombre total d'électrons de l'atome, mais nous ne considérons ici que le nombre d'électrons de valence. La coquille de valence d'un métal de transition peut être donnée sous une forme générale comme suit:
nd (n + 1) s (n + 1) p
La configuration électronique du métal peut contenir un maximum de 18 électrons. Par conséquent, la configuration d'électrons à gaz noble a toutes les 18 houes d'électrons remplies d'électrons. C'est pourquoi nous appelons ce concept comme une règle d'électrons 18.
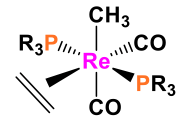
Qu'est-ce que la règle Ean?
La règle EAN est un concept en chimie qui stipule que si l'atome métallique central dans un composé organométallique a la configuration électronique du gaz noble présent dans la même période que le métal, alors le complexe est stable. Le terme ean signifie un numéro atomique efficace. Ici, ce concept considère le nombre total d'électrons présents dans l'atome métallique. Il est similaire à la règle des 18 électrons car cela indique également que le fait d'avoir la configuration d'électrons à gaz noble rend le complexe métallique stable.
Par exemple, considérons un complexe métallique ayant l'ion Fe2 + au centre. Le nombre atomique de fer est de 26. Puisque cet ion a une charge de +2, le nombre total d'électrons sera de 24. Par conséquent, si les ligands qui se lient à cet atome métallique donne 12 électrons à l'ion métallique afin que la configuration électronique du fer soit terminée (pour obtenir la configuration d'électrons à gaz noble = 36 pour la période où le fer est), alors le complexe métallique devient écurie.
Quelle est la différence entre la règle d'électrons 18 et la règle EAN?
La règle de 18 électrons et la règle EAN indique que l'obtention d'une configuration d'électrons à gaz noble les rend stables. Cependant, la différence clé entre la règle de 18 électrons et la règle EAN est que la règle de 18 électrons indique qu'il doit y avoir 18 électrons de valence autour du métal dans les complexes de coordination pour devenir stable, tandis que la règle EAN décrit qu'un atome métallique doit obtenir l'électron Configuration du gaz noble présent dans la même période pour devenir stable.
L'infographie ci-dessous résume la différence entre la règle de 18 électrons et la règle EAN.

Résumé - 18 Règle d'électrons vs règne
La règle de 18 électrons et la règle EAN indique que l'obtention d'une configuration d'électrons à gaz noble les rend stables. La principale différence entre la règle des électrons 18 et la règle EAN est que la règle de 18 électrons indique qu'il doit y avoir 18 électrons de valence autour du métal dans les complexes de coordination afin de devenir stable, tandis que la règle EAN indique qu'un atome métallique doit obtenir l'électron Configuration du gaz noble présent dans la même période afin de devenir stable.
Référence:
1. «24.3: la règle à 18 électrons.”Chemistry LibreTexts, LibreTexts, 5 juin 2019, disponible ici.
Image gracieuseté:
1. «18 Electron Rule Exemple» par Derrekli - Propre travaux (CC BY-SA 4.0) via Commons Wikimedia


