Différence entre le citrate de zinc et le gluconate de zinc
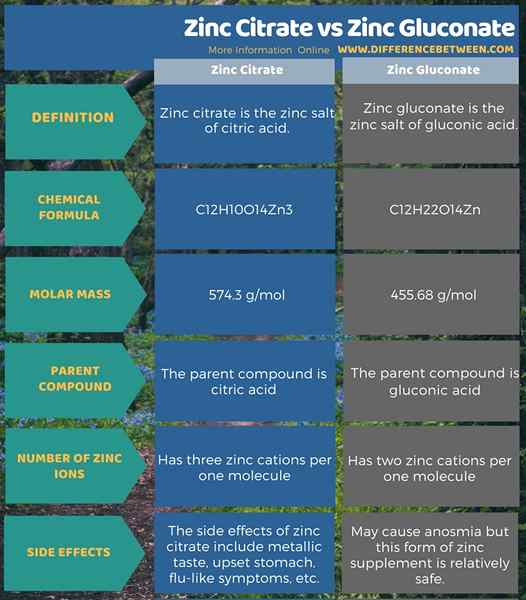
Le différence clé entre le citrate de zinc et le gluconate de zinc est que Le composé parent du citrate de zinc est de l'acide citrique tandis que le composé parent du gluconate de zinc est de l'acide gluconique.
Le citrate de zinc et le gluconate de zinc sont deux formes de compléments alimentaires que nous utilisons pour prévenir une carence en zinc. Le zinc est un minéral essentiel que notre corps peut facilement absorber. Par conséquent, si nous n'obtenons pas suffisamment de quantité de zinc, nous devrons peut-être prendre ces compléments alimentaires comme indiqué par le médecin. Laissez-nous dans plus de détails sur ces composés.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que le citrate de zinc
3. Qu'est-ce que le gluconate de zinc
4. Comparaison côte à côte - Citrate de zinc vs gluconate de zinc sous forme tabulaire
5. Résumé
Qu'est-ce que le citrate de zinc?
Le citrate de zinc est le sel de zinc de l'acide citrique. La formule chimique de ce composé est C12HdixO14Zn3. Sa masse molaire est de 574.3 g / mol. Par conséquent, ce composé contient trois cations de zinc (Zn+2) associé à deux ions citrate. Ce composé est bien connu comme un complément alimentaire utile pour prévenir la carence en zinc. En règle générale, nous prenons cela oralement en capsule ou comme tablette.
Cependant, en raison de la présence de zinc, cela peut avoir un goût métallique. C'est un effet secondaire du traitement. Cependant, prendre une petite quantité de boisson après avoir pris la tablette peut éviter ce goût inhabituel. De plus, ce traitement peut irriter le tube digestif, entraînant un maux d'estomac. Un autre effet secondaire important est que nous pouvons obtenir des symptômes pseudo-grippaux, notamment la fièvre, les maux de gorge, les frissons, etc.
Qu'est-ce que le gluconate de zinc?
Le gluconate de zinc est le sel de zinc de l'acide gluconie. La formule chimique de ce composé est C12H22O14Zn. Il a la masse molaire, 455.68 g / mol. Il contient un cation en zinc (Zn+2) associé à deux anions d'acide gluconique. De plus, c'est un complément alimentaire populaire et une bonne source de zinc. Nous pouvons trouver de l'acide gluconique dans des sources naturelles, mais pour la préparation du supplément, les industries produisent de l'acide gluconique via la fermentation du glucose par Aspergillus Niger ou certaines espèces de champignons.
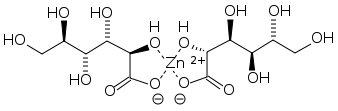
Figure 01: Structure du gluconate de zinc
Plus important encore, ce composé est utilisé pour traiter un rhume. Nous pouvons l'utiliser dans des pastilles pour traiter les symptômes du rhume. Lorsque l'on considère les effets secondaires de ce composé, l'anosmie (perte d'odeur) est un effet secondaire signalé. Cependant, ce composé est relativement sûr que les autres suppléments de zinc.
Quelle est la différence entre le citrate de zinc et le gluconate de zinc?
Le citrate de zinc est le sel de zinc de l'acide citrique. La formule chimique est C12HdixO14Zn3 et la masse molaire de est 574.3 g / mol. De plus, le composé parent de ce composé est l'acide citrique. Tandis que le gluconate de zinc est le sel de zinc de l'acide gluconie. La formule chimique est C12H22O14Zn et la masse molaire de sont 455.68 g / mol. Ici, le composé parent est l'acide gluconique. Par conséquent, la principale différence entre le citrate de zinc et le gluconate de zinc est leur composé parent respectif. Bien que le citrate de zinc ait de nombreux effets secondaires, notamment le goût métallique, les maux d'estomac, les symptômes pseudo-grippaux, etc. Le gluconate de zinc n'a que quelques effets secondaires tels que l'anosmie, donc il est relativement sûr.

Résumé - Citrate de zinc vs gluconate de zinc
Les suppléments en zinc sont très importants car le zinc est un minéral essentiel. Par conséquent, le citrate de zinc et le gluconate de zinc sont deux formes de suppléments. La différence entre le citrate de zinc et le gluconate de zinc est que le composé parent du citrate de zinc est de l'acide citrique tandis que le composé parent du gluconate de zinc est de l'acide gluconique.
Référence:
1. «Citrate de zinc.»Information du Centre national pour la biotechnologie. Base de données de composés PubChem, u.S. Bibliothèque nationale de médecine. Disponible ici
2. Uddin, rae. «Effets secondaires du citrate de zinc.”Livestrong.Com, Leaf Group, 14 août. 2017. Disponible ici
3. «Gluconate de zinc.»Information du Centre national pour la biotechnologie. Base de données de composés PubChem, u.S. Bibliothèque nationale de médecine. Disponible ici
Image gracieuseté:
1.«Structure du gluconate de zinc en EN: Utilisateur: Slashme (domaine public) via Commons Wikimedia


