Différence entre l'acide phosphorique et l'acide citrique

Le différence clé entre l'acide phosphorique et l'acide citrique est que l'acide phosphorique est un acide minéral faible, tandis que l'acide citrique est un acide organique faible.
L'acide phosphorique et l'acide citrique sont des acides faibles. Par conséquent, ces acides ne peuvent pas se dissocier complètement en ions; Ils ne peuvent que se dissocier partiellement dans les ions.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que l'acide phosphorique
3. Qu'est-ce que l'acide citrique
4. Similitudes - acide phosphorique et acide citrique
5. Acide phosphorique vs acide citrique sous forme tabulaire
6. Résumé - acide phosphorique vs acide citrique
Qu'est-ce que l'acide phosphorique?
L'acide phosphorique est un acide minéral faible ayant la formule chimique H3Pote4. Le nom IUPAC de ce composé est l'acide orthophosphorique, et nous pouvons l'identifier comme un acide non toxique. De plus, c'est un composé contenant du phosphore important à partir duquel l'ion phosphate de dihydrogène (H2Pote4-) est dérivé. Par conséquent, les ions dans l'acide phosphorique sont très importants pour les plantes car c'est la principale source de phosphore.
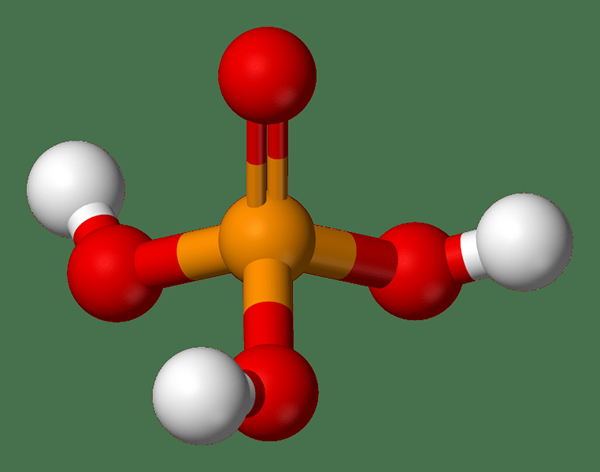
Figure 01: Structure de l'acide phosphorique
La masse molaire de l'acide phosphorique est de 97.99 g / mol. Il peut y avoir des formes hydratées et anhydres de ce composé. L'acide phosphorique apparaît comme un solide blanc qui est déliquescent et inodore. De plus, la production d'acide phosphorique a deux voies: processus humide et processus thermique. Le processus humide utilise la fluoroapétite (phosphate roche) pour la production de cet acide, ainsi que l'acide sulfurique concentré. La réaction chimique est la suivante:
Californie5(Po4) 3f + 5h2DONC4 + 10h2O → 3H3Pote4 + 5CASO4.2H2O + HF
Dans le processus thermique, le phosphore liquide (P4) et l'air subissent une réaction chimique à l'intérieur d'un four à 1800-3000 K. Tout d'abord, une machine pulvérise le liquide de phosphore dans une chambre de fournaise, où le phosphore brûle dans l'air réagissant avec l'oxygène (O2). Le produit de cette étape réagit avec l'eau dans une tour d'hydratation pour produire l'acide.
P4 (l)+ 5o2 (g)→ 2p2O5 (g)
P2O5 (g)+ 3h2O(l)→ 2H3Pote4 (aq)
L'application la plus courante et la plus importante de l'acide phosphorique est la production d'engrais contenant du phosphore. De plus, il existe trois formes majeures de sels de phosphate qui sont utiles comme engrais: le triple phosphate, l'hydrogène diammonium et le monoammonium dihydrogéphosphate.
Qu'est-ce que l'acide citrique?
L'acide citrique est un acide organique faible qui se produit naturellement chez les agrumes. Puisqu'il existe de nombreuses applications de ce composé, les fabricants ont tendance à produire une grande quantité d'acide citrique par an. Certaines de ses applications importantes incluent l'utilisation comme acidedificateur, comme arôme et agent chélatant. On peut observer que cet acide se produit sous deux formes comme la forme anhydre et la forme monohydratée.
La forme anhydre d'acide citrique est la forme sans eau. Il apparaît comme une substance incolore et est également inodore. Il n'y a pas d'eau sous sa forme sèche et granulée. Nous pouvons produire ce composé par cristallisation à partir de l'eau chaude.

Figure 02: acide citrique sous forme solide
L'acide citrique anhydre est formé à partir de la forme monohydrate à 78 ° C. La densité de la forme anhydre est 1.665 g / cm3. Il fond à 156 ° C et le point d'ébullition de ce composé est de 310 ° C. La formule chimique de ce composé est C6H8O7 , tandis que la masse molaire est de 192.12 g / mol.
L'acide citrique monohydraté est la forme contenant de l'eau d'acide citrique. Il a une molécule d'eau associée à une molécule d'acide citrique. Nous appelons cette eau l'eau de cristallisation. Cette forme d'acide citrique est formée par cristallisation à partir de l'eau froide.
Quelles sont les similitudes entre l'acide phosphorique et l'acide citrique?
- L'acide phosphorique et l'acide citrique sont des acides faibles.
- Les deux acides ne peuvent pas se dissocier complètement; Ils se dissocient partiellement en ions
- Ce sont des acides non toxiques.
Quelle est la différence entre l'acide phosphorique et l'acide citrique?
L'acide phosphorique et l'acide citrique sont des acides faibles. Par conséquent, ces acides ne peuvent pas se dissocier complètement en ions; Ils ne peuvent que se dissocier partiellement dans les ions. La principale différence entre l'acide phosphorique et l'acide citrique est que l'acide phosphorique est un acide minéral de l'échelle, tandis que l'acide citrique est un acide organique faible. De plus, l'acide phosphorique apparaît comme un solide blanc qui est déliquescent, tandis que l'acide citrique apparaît comme un solide / granules incolore ou sous forme liquide.
L'infographie suivante répertorie les différences entre l'acide phosphorique et l'acide citrique sous forme tabulaire.
Résumé - acide phosphorique vs acide citrique
L'acide phosphorique est un acide minéral faible ayant la formule chimique H3Pote4, tandis que l'acide citrique est un acide organique faible et il se produit naturellement chez les agrumes. La principale différence entre l'acide phosphorique et l'acide citrique est que l'acide phosphorique est un acide minéral de l'échelle, tandis que l'acide citrique est un acide organique faible.
Référence:
1. "Acide citrique." Centre national d'information sur la biotechnologie. Base de données de composés PubChem, U.S. Bibliothèque nationale de médecine.
Image gracieuseté:
1. «Phosphorique-acide-3D-balls» (domaine public) via les communes Wikimedia
2. «Zitronensäure Kristallzucht» par Tipfox - Propre travaux (CC BY-SA 4.0) via Commons Wikimedia


