Différence entre la lysine et la l-lysine
Différence clé - Lysine vs L-lysine
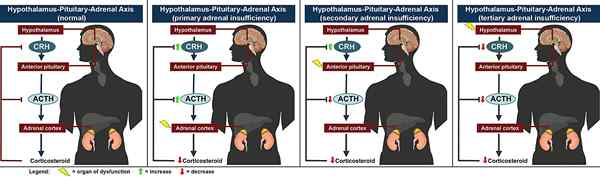
La lysine et la l-lysine sont les deux types d'acides aminés, partageant les mêmes propriétés physiques, il y a une certaine différence entre elles. Le La différence clé entre la lysine et la l-lysine est la capacité de faire tourner la lumière polarisée plan. La lysine est un acide α-amino essentiel à l'origine biologique active. Il peut se produire sous deux formes isomères en raison de la possibilité de former deux éantiomères différents autour de l'atome de carbone chiral. Ceux-ci sont connus sous le nom de formes L et D, analogues aux configurations gaucher et droitiers. Ces formes L et D seraient optiquement actives et tournent la lumière polarisée plane dans un sens différent; dans le sens horaire ou anti-horloge. Si la lumière fait pivoter la lysine dans le sens antihoraire, alors la lumière présente la lévorotation, et elle est connue sous le nom de l-lysine. Cependant, il convient de noter soigneusement ici que l'étiquetage D et L des isomères n'est pas le même que le marquage D et L.
Qu'est-ce que la lysine?
La lysine est un acide aminé essentiel lequel est non synthétisé dans notre corps et doit être fourni par le régime régulier. Par conséquent, la lysine est un acide aminé essentiel pour les humains. Il s'agit d'un composé organique biologiquement important composé d'amine (-nh2) et des groupes fonctionnels d'acide carboxylique (-COOH) avec formule chimique NH2-(Ch2)4-CH (NH2) -Cooh. Les éléments clés de la lysine sont le carbone, l'hydrogène, l'oxygène et l'azote. En biochimie, les acides aminés ayant à la fois l'amine et les groupes d'acide carboxylique attachés au premier atome de carbone (alpha-) sont connus sous le nom de acides α-amino. Ainsi, la lysine est également considérée comme des acides α-aminés. La structure de la lysine est donnée dans la figure 1.
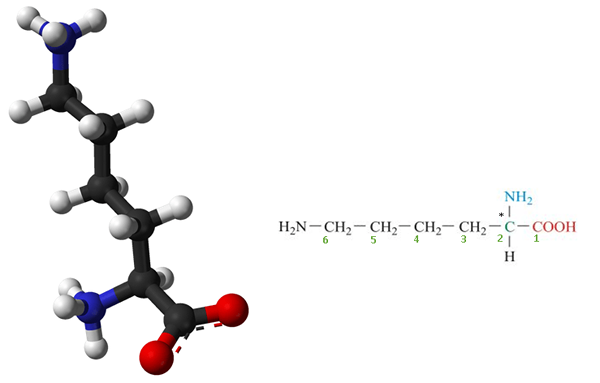
Figure 1: Structure moléculaire de la lysine (* L'atome de carbone est un atome de carbone chiral ou asymétrique et représente également l'atome d'alpha-carbone)
La lysine est de nature basique car elle contient deux groupes amino basiques et un groupe acide acide acide carboxylique. Par conséquent, il forme également une liaison hydrogène étendue en raison de la présence de deux groupes amino. Bonnes sources de lysine sont des sources animales riches en protéines telles que œufs, viande rouge, agneau, porc et volaille, fromage et certains poissons (comme la morue et les sardines). La lysine est aussi Riche en protéines végétales comme le soja, les haricots et les pois. Cependant, c'est un acide aminé limitant dans la plupart des grains de céréales, mais il est abondant dans la plupart des impulsions et des légumineuses.
Qu'est-ce que la l-lysine?
Lysine a quatre groupes différents autour des 2nd carbone, et c'est structure asymétrique. De plus, la lysine est un acide aminé optiquement actif en raison de la présence de cet atome de carbone asymétrique ou chiral. Ainsi, la lysine peut créer des stéréoisomères qui sont des molécules isomères ayant la même formule moléculaire, mais diffèrent dans les orientations tridimensionnelles de leurs atomes dans l'espace. Les énantiomères sont deux stéréoisomères qui sont liés les uns aux autres par une réflexion ou ce sont des images miroir les unes des autres. La lysine est disponible en deux formes énantiomères connues sous le nom de L- et D- et les énantiomères de la lysine sont donnés sur la figure 2.

Figure 2: Énantiomères d'acide aminé de lysine. Les groupes COOH, H, R et NH2 sont disposés autour de l'atome C de manière dans le sens des aiguilles d'une montre, l'énantiomère est appelé L-forme et D. L- et D- se référer uniquement à la disposition spatiale autour de l'atome de carbone et ne référez pas à l'activité optique. Alors que les formes L et D d'une molécule chirale tournent le plan de lumière polarisée dans différentes directions, certaines formes L (ou formes D) tournent la lumière vers la gauche (levo ou la forme l) et d'autres vers la droite (Dextro ou D-Form). Les formes L et D sont appelées isomères optiques.
La l-lysine et la d-lysine sont des énantiomères les uns des autres ont les mêmes propriétés physiques, à l'exception de la direction dans laquelle ils tournent la lumière polarisée. Ils ont une relation d'image miroir non superprimable. Cependant, la nomenclature de D et L n'est pas courante dans les acides aminés, y compris la lysine. Ils tournent la lumière polarisée en plan dans la même ampleur mais dans des directions différentes. L'isomère D et L de la lysine qui tourne la lumière polarisée plan d-lysine et celui qui tourne la lumière polarisée du plan dans le sens antihoraire L-lysine (Figure 2).
L-lysine est le la plupart disponibles stables de lysine disponibles. La d-lysine est une forme synthétique de lysine et peut être synthétisée à partir de la l-lysine par racémisation. Il est utilisé dans le traitement de la poly-d-lysine, qui est utilisé comme matériau de revêtement pour améliorer la fixation cellulaire. La l-lysine joue un rôle significatif dans le corps humain, dans l'absorption du calcium, le développement des protéines musculaires et la synthèse des hormones, des enzymes et des anticorps. Industriellement, la l-lysine est produite par un processus de fermentation microbienne en utilisant Corynebacterium glutamicum.
Quelle est la différence entre la lysine et la l-lysine?
La lysine et la l-lysine ont les mêmes propriétés physiques, à l'exception de la direction dans laquelle ils tournent la lumière polarisée. En conséquence, la l-lysine peut avoir des effets biologiques et des propriétés fonctionnelles sensiblement différentes. Cependant, des recherches très limitées ont été effectuées afin de distinguer ces effets biologiques et ces propriétés fonctionnelles. Certaines de ces différences peuvent inclure,
Goût
L-lysine: Les formes L des acides aminés ont tendance à être insipides.
D-lysine: Les formes D des acides aminés ont tendance à avoir un goût sucré.
Par conséquent, la l-lysine peut être moins / pas plus douce que la lysine.
Abondance
L-lysine: Les formes en L de l'acide aminé, y compris la l-lysine, sont la forme la plus abondante de la nature. À titre d'exemple, neuf des dix-neuf acides Amino L-Amino couramment trouvés dans les protéines sont dextrorotatoires et les autres sont lévorotatifs.
D-lysine: Les D-formes d'acides aminés qui ont été observées expérimentalement se sont révélées très rarement.
Références: Salomons, T.W. Graham et Graig B. Fryhle (2004). Chimie organique (8e ed). Hoboken: John Wiley & Sons, Inc. Everhardus, un. (1984). Stéréochimie, base de non-sens sophistiqué en pharmacocinétique et pharmacologie clinique, Journal européen de pharmacologie clinique, 26, 663-668. Image gracieuseté: «L-lysine-monocation-from-hydrochlorure-dihydrate-xtal-3d-balls» par Ben Mills - propre travail via Wikimedia Commons