Différence entre l'isomérisation et l'aromatisation
Le différence clé entre l'isomérisation et l'aromatisation L'isomérisation implique la conversion de l'isomère sur un autre isomère tandis que l'aromatisation implique la conversion d'un composé aliphatique en un composé aromatique.
L'isomérisation et l'aromatisation sont des réactions de synthèse importantes en chimie organique. Ces réactions impliquent la conversion d'une structure chimique existante en une structure chimique légèrement différente. Dans l'isomérisation, une forme isomère se convertit en une autre forme isomère, tandis que dans l'aromatisation, un composé aliphatique se convertit en un composé aromatique.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que l'isomérisation
3. Qu'est-ce que l'aromatisation
4. Comparaison côte à côte - isomérisation vs aromatisation sous forme tabulaire
5. Résumé
Qu'est-ce que l'isomérisation?
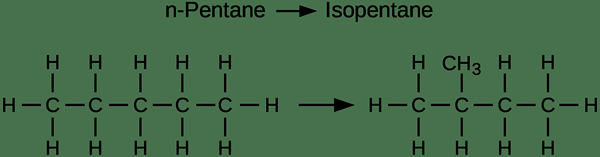
L'isomérisation est un type de réaction chimique dans laquelle une forme isomère d'un composé organique se transforme en une autre forme isomère. La plupart des composés chimiques n'ont qu'un seul isomère; Par conséquent, l'isomérisation de ces composés se réfère à la conversion de sa structure en sa forme isomère. Cependant, certains composés chimiques ont plus d'une forme isomère; Ensuite, l'isomérisation fait référence à la conversion d'une forme isomère dans l'une de ses autres formes isomères. Le composé nouvellement formé (ou la nouvelle forme isomère) se forme avec la même composition chimique mais une connectivité ou une configuration atomique différente.

Figure 01: Exemple d'isomérisation (Conversion de N-Pentane en isopentane)
Par exemple, la conversion du butane en isobutène est une réaction d'isomérisation. Dans cette réaction, le butane est une structure d'hydrocarbures à chaîne droite. Cependant, l'isobutène est une structure ramifiée. Nous pouvons atteindre cette isomérisation via le traitement thermique du butane (environ 100 degrés Celsius). Ce traitement thermique se fait en présence d'un catalyseur approprié. Ici, la connectivité atomique du composé chimique change. Par conséquent, les propriétés chimiques et physiques du composé chimique changent également.
Dans les alcènes, la forme d'isomérisation la plus courante est l'isomérisation cis-trans. Dans ce processus, la connectivité atomique ne change pas beaucoup parce que lorsque les isomères cis se transforment en isomère trans, seuls les groupes de substituants attachés à la double liaison changent. En plus de cela, nous pouvons également observer le processus d'isomérisation parmi les composés inorganiques. Dans ce processus, l'isomérisation des complexes de métal de transition est la forme la plus courante.
Qu'est-ce que l'aromatisation?
L'aromatisation est un processus chimique où un seul précurseur non aromatique se convertit en un système aromatique. En règle générale, nous pouvons atteindre l'aromatisation par déshydrogénation d'un composé cyclique existant; Par exemple, la conversion du cyclohexane en benzène. Ici, un composé hétérocyclique forme.
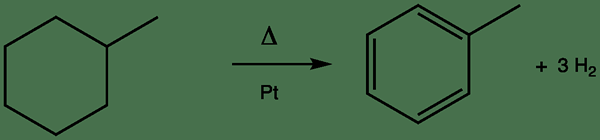
Figure 02: Aromatisation
Un exemple courant d'aromatisation dans le raffinage d'huile est la déshydrogénation du naphtène. Cette réaction est catalysée par le platine, et dans cette réaction, le naphtène est converti en toluène, qui est un composé aromatique.
Quelle est la différence entre l'isomérisation et l'aromatisation?
L'isomérisation et l'aromatisation sont des réactions de synthèse importantes en chimie organique. La principale différence entre l'isomérisation et l'aromatisation est que l'isomérisation implique la conversion de l'isomère sur un autre isomère tandis que l'aromatisation implique la conversion d'un composé aliphatique en un composé aromatique. Un exemple commun d'isomérisation est la conversion du butane en isobutène tandis que la conversion du cyclohexane en benzène est un exemple d'aromatisation.
Le tableau suivant résume la différence entre l'isomérisation et l'aromatisation.
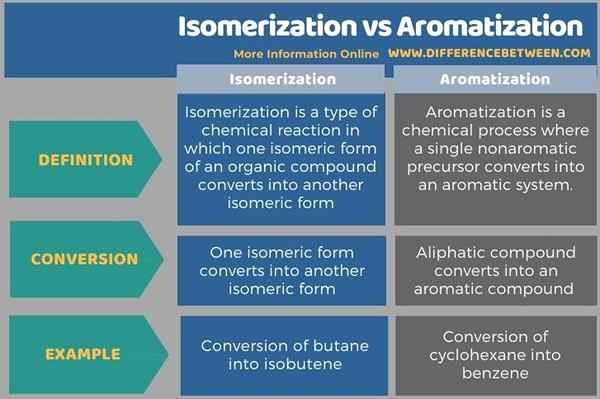
Résumé - isomérisation vs aromatisation
Le résumé de l'IB, l'isomérisation et l'aromatisation sont des réactions de synthèse importantes en chimie organique. La principale différence entre l'isomérisation et l'aromatisation est que l'isomérisation implique la conversion de l'isomère ON en un autre isomère tandis que l'aromatisation implique la conversion d'un composé aliphatique en un composé aromatique.
Référence:
1. «Aromatisation.»Wikipedia, Wikimedia Foundation, 25 février. 2020, disponible ici.
Image gracieuseté:
1. «Isomérisation du pentane» par hydrargyrum, basé sur la version PNG annotée antérieure par Mbeychok - Dérivé vecteur du fichier: Pentanisomerisierung.PNG (domaine public) via Commons Wikimedia
2. «MEC6H11TOPHME» par Smokefoot - Propre travaux (CC BY-SA 4.0) via Commons Wikimedia


