Différence entre l'énergie d'ionisation et l'énergie de liaison
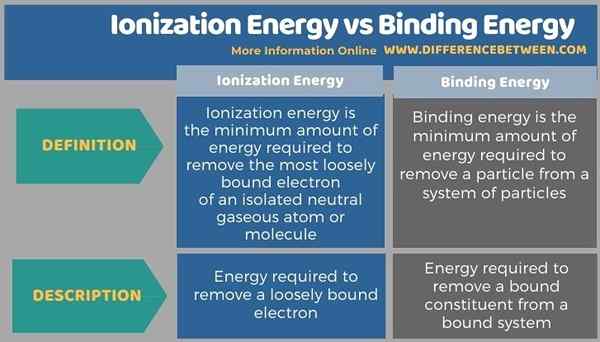
Le différence clé entre l'énergie d'ionisation et l'énergie de liaison est que L'énergie d'ionisation est la quantité minimale d'énergie nécessaire pour éliminer l'électron le plus lâchement lié d'un atome gazeux ou une molécule gazeux neutre isolé tandis que l'énergie de liaison est la quantité minimale d'énergie nécessaire pour éliminer une particule d'un système de particules.
L'énergie d'ionisation et l'énergie de liaison des systèmes chimiques sont deux termes différents, décrivant deux phénomènes différents. Discutons de plus de détails ci-dessous dans cet article.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que l'énergie d'ionisation
3. Qu'est-ce que l'énergie de liaison
4. Comparaison côte à côte - énergie d'ionisation vs énergie de liaison dans la forme tabulaire
5. Résumé
Qu'est-ce que l'énergie d'ionisation?
L'énergie d'ionisation est la quantité minimale d'énergie nécessaire pour retirer l'électron le plus lâche d'un atome gazeux ou une molécule gazeux neutre isolé. Nous pouvons désigner cette réaction d'ionisation comme suit:
X(g) + énergie ⟶ x+(g) + e-
Dans cette équation, x est tout atome ou molécule tandis que x+ est l'ion avec l'électron lié sans lien retiré de l'atome ou de la molécule tandis que E- est l'électron supprimé. Généralement, c'est un processus endothermique. En règle générale, l'électron le plus externe est du noyau atomique, abaissez l'énergie d'ionisation et vice versa.

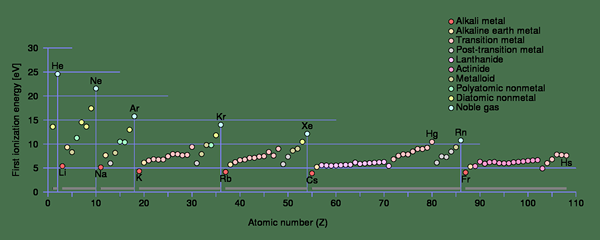
Figure 01: Tendances énergétiques de première ionisation dans le tableau périodique des éléments
En chimie physique, l'énergie d'ionisation est exprimée dans l'unité d'électronvolts (EV). Cependant, cette unité n'est généralement pas utilisée en termes chimiques car nous calculons les valeurs «par mole». Par conséquent, l'unité de mesure de l'énergie d'ionisation est des kilojoules par mole (kj / mol). De plus, il existe des tendances périodiques de l'énergie d'ionisation dans le tableau périodique; L'énergie d'ionisation augmente généralement de gauche à droite dans une période donnée, et l'énergie d'ionisation diminue généralement de haut en bas dans un groupe donné.
Qu'est-ce que l'énergie de liaison?
L'énergie de liaison est la quantité minimale d'énergie nécessaire pour éliminer une particule d'un système de particules. Nous pouvons également le décrire comme la plus petite quantité d'énergie nécessaire pour démonter un système de particules en parties individuelles. Cependant, en physique nucléaire, le terme énergie de séparation est utilisé plutôt que le terme énergie de liaison. En règle générale, un système lié est à un niveau d'énergie inférieur à ses constituants non liés.
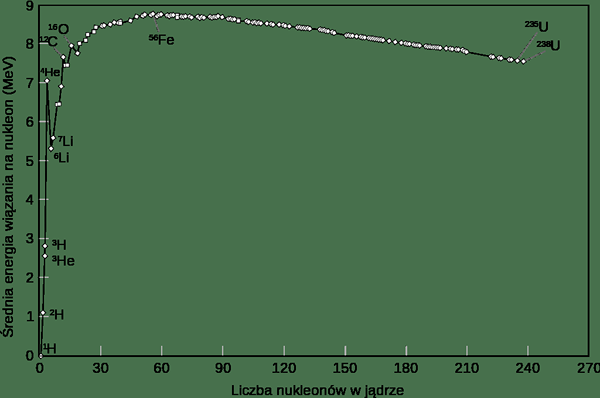
Figure 02: Courbe d'énergie de liaison pour différents éléments chimiques
Il existe différents types d'énergie de liaison: énergie de liaison aux électrons ou énergie d'ionisation, énergie de liaison atomique, énergie de dissociation des liaisons, énergie de liaison nucléaire, énergie de liaison gravitationnelle, etc.
Quelle est la différence entre l'énergie d'ionisation et l'énergie de liaison?
L'énergie d'ionisation est un type d'énergie de liaison. La principale différence entre l'énergie d'ionisation et l'énergie de liaison est que l'énergie d'ionisation est la quantité minimale d'énergie nécessaire pour détacher l'électron ou la molécule gazeux neutre isolé et la molécule de liaison est la quantité minimale d'énergie nécessaire pour éliminer une Particule d'un système de particules.
Vous trouverez ci-dessous un résumé de la différence entre l'énergie d'ionisation et l'énergie de liaison.
Résumé - Énergie d'ionisation vs énergie de liaison
L'énergie d'ionisation est un type d'énergie de liaison. La principale différence entre l'énergie d'ionisation et l'énergie de liaison est que l'énergie d'ionisation est la quantité minimale d'énergie nécessaire pour éliminer l'électron le plus lâche d'un atome gazeux ou une molécule neutre isolé tandis que l'énergie de liaison est la quantité minimale d'énergie nécessaire pour éliminer une particule de Un système de particules.
Référence:
1. "Énergie de liaison." Wikipédia, Fondation Wikimedia, 20 septembre. 2020, disponible ici.
2. "Énergie d'ionisation." Chemistry LibreTexts, LibreTexts, 21 août. 2020, disponible ici.


