Différence entre la caténation et l'allotropie
Le différence clé entre la caténation et l'allotropie est que La caténation se réfère à la vésicule d'un élément pour lui-même, formant des structures de chaîne ou d'anneau, tandis qu'Alllotropy fait référence à l'existence de différentes formes physiques du même élément chimique.
Bien que la caténation et l'allotropy expriment une idée similaire sur les différents arrangements des atomes du même élément chimique, ce sont des termes différents qui décrivent différents états de matière.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que la caténation
3. Qu'est-ce que l'allotropie
4. Comparaison côte à côte - caténation et allotropie sous forme tabulaire
5. Résumé
Qu'est-ce que la caténation
Dans la chimie inorganique, la caténation est la capacité des atomes d'un élément chimique particulier à se lier entre eux, formant une chaîne ou une structure d'anneau. Généralement, l'élément chimique carbone est impliqué dans la caténation car le carbone est capable de former des structures aliphatiques et aromatiques en liant un grand nombre d'atomes de carbone. De plus, il existe d'autres éléments chimiques qui peuvent former ces structures, comme le soufre et le phosphore.
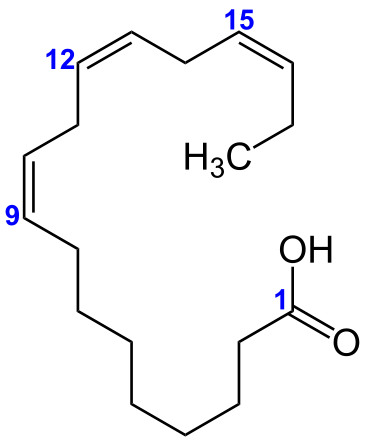
Figure 01: Une longue structure de carbone à longue chaîne
Lorsqu'un certain élément chimique subit une caténation, les atomes de cet élément doivent avoir une valence qui est au moins deux. De plus, cet élément chimique doit être capable de former de fortes liaisons chimiques entre les atomes du genre; e.g. des liaisons covalentes. Nous pouvons également nommer la polymérisation comme un type de réaction de caténation. Des exemples d'éléments chimiques qui peuvent subir une caténation comprennent le carbone, le soufre, le silicium, le germanium, l'azote, le sélénium et le tellurium.
Qu'est-ce que l'allotropie?
Dans la chimie inorganique, l'allotropie est l'existence de deux ou plusieurs formes physiques différentes d'un élément chimique. Ces différentes formes physiques existent dans le même état physique, principalement dans l'état solide. Par conséquent, nous pouvons dire que ce sont des modifications structurelles différentes du même élément chimique. De plus, les allotropes contiennent des atomes du même élément chimique qui se lie entre eux de différentes manières.

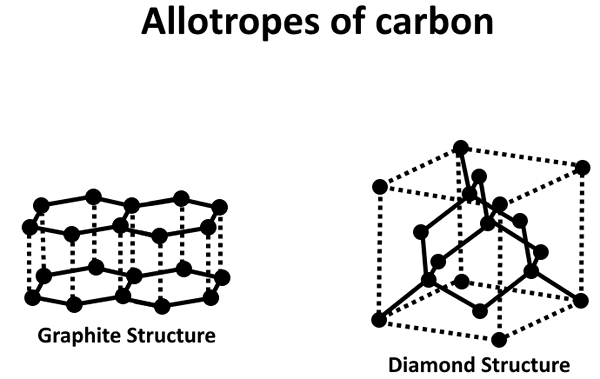
Figure 02: Deux principaux allotropes de carbone
Cependant, ces différentes formes peuvent avoir des propriétés physiques différentes car elles ont différentes structures et comportements chimiques. Un allotrope est capable de convertir en un autre lorsque nous modifions certains facteurs physiques tels que la pression, la lumière, la température, etc. Par conséquent, ces facteurs physiques affectent la stabilité de ces composés. Quelques exemples d'allotropes incluent les suivants:
- Allotropes de carbone - diamant, graphite, fullerènes, etc.
- Allotropes de phosphore - phosphore blanc, phosphore rouge, etc.
- Allotropes d'oxygène - dioxygène, ozone, etc.
- Allotropes d'arsenic - arsenic jaune, arsenic gris, etc.
Quelle est la différence entre la caténation et l'allotropie?
La caténation et l'allotropie sont différentes les unes des autres en fonction de la disposition des atomes. La caténation est la capacité des atomes d'un élément chimique particulier à se lier entre eux, formant une chaîne ou une structure d'anneau. L'allotropie dans la chimie inorganique est l'existence de deux ou plusieurs formes physiques différentes d'un élément chimique. Ainsi, la principale différence entre la caténation et l'allotropie est que la caténation est la bidonnance d'un élément pour lui-même, formant des structures de chaîne ou d'anneaux, tandis que l'allotropie est l'existence de différentes formes physiques du même élément chimique.
Le tableau suivant résume la différence entre la caténation et l'allotropie.

Résumé - Caténation vs Allotropy
La caténation et l'allotropie sont des termes chimiques importants. La principale différence entre la caténation et l'allotropie est que la caténation se réfère à la vésicule d'un élément à elle-même formant une chaîne ou une structure d'anneau alors qu'Alllotropy fait référence à l'existence de différentes formes physiques du même élément chimique.
Référence:
1. Helmenstine, Anne Marie. «Définition de la caténation et exemples."Thoughtco, février. 11, 2020, disponible ici.
Image gracieuseté:
1. «Formules structurelles d'acide alpha-linolénique V.2 ”par Jü - Propre travaux (CC0) via Commons Wikimedia
2. «Allotropes de carbone» par Diepizza - Propre travaux (CC BY-SA 4.0) via Commons Wikimedia


