Différence entre halogénure alkyle et halogénure d'aryle
Différence clé - Halogine alkyle vs halogénure d'aryle
Les halogénures d'alkyle et les halogénures d'aryle sont des composés organiques. Ceux-ci sont également appelés halogénures biologiques. Les types d'halogènes qui peuvent être attachés pour produire ce type de molécule sont le fluor, le chlore, le brome et l'iode. Ces atomes halogènes sont attachés à un atome de carbone dans les halogénures organiques. La principale différence entre l'halogénure alkyle et l'halogénure d'aryle est que L'atome halogène dans les halogénures d'alkyle est attaché à un SP3 Atome de carbone hybridé tandis que l'atome halogène dans les halogénures d'aryle est attaché à un SP2 atome de carbone hybridé.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que l'alkyle Halide
3. Qu'est-ce que l'halogine aryle
4. Comparaison côte à côte - halogénure alkyle vs halogénure d'aryle sous forme tabulaire
5. Résumé
Qu'est-ce que l'alkyle Halide?
L'halogénure alkyle, exprimé par son nom, est un composé ayant un atome halogène attaché à une chaîne d'atomes de carbone. Ici, un atome d'hydrogène de la chaîne de carbone est remplacé par un atome halogène. Selon le type d'halogène qui a été attaché et la structure de la chaîne de carbone, les propriétés des halogénures organiques diffèrent les unes des autres. Les halogénures d'alkyle peuvent être classés en fonction du nombre d'atomes de carbone attachés à l'atome de carbone qui est attaché à l'atome halogène. En conséquence, les halogénures d'alkyle primaires, les halogénures d'alkyle secondaire et les halogénures d'alkyle tertiaires peuvent être observés.
Figure 01: Halogénure d'alkyle primaire
Cependant, les halogénures d'alkyle peuvent parfois être confondus avec les halogénures d'aryle. Par exemple, si l'atome halogène est attaché à un atome de carbone, qui est attaché à un anneau de benzène (CL-CH2-C6H5), on pourrait penser que c'est un halogée d'aryle. Mais c'est un halogénure alkyle parce que l'atome halogène est attaché au carbone qui est SP3 hybridé.
Les halogènes sont plus électronégatifs que le carbone. Ainsi, un moment dipolaire est observé dans la liaison carbone-halogène, c'est-à-dire que la molécule devient une molécule polaire lorsque la liaison devient polaire. L'atome de carbone obtient une petite charge positive et l'halogène obtient une petite charge négative. Cela conduit à des interactions dipol-dipole entre les halogénures alkyle. Mais la force de cette interaction est différente dans les halogénures primaires, secondaires et tertiaires. En effet.
Qu'est-ce que l'halogine aryle?
Un halogénure d'aryle est une molécule ayant un atome halogène attaché à un carbone hybridé SP2 dans un anneau aromatique directement. Il s'agit d'une structure insaturée en raison de la présence de doubles liaisons dans l'anneau aromatique. Les halogénures d'aryle montrent également les interactions dipol-dipole. La liaison carbone-halogène est plus forte que celle des halogénures alkyle en raison de la présence d'électrons annulaires. Cela se produit parce que l'anneau aromatique donne des électrons à l'atome de carbone, réduisant la charge positive. Les halogénures d'aryle peuvent subir une substitution électrophile et peuvent obtenir des groupes alkyle attachés au ortho, para ou méta positions de l'anneau aromatique. Un ou deux halogènes peuvent également s'attacher à l'anneau aromatique. Qui est également dans le ortho, para ou méta positions.
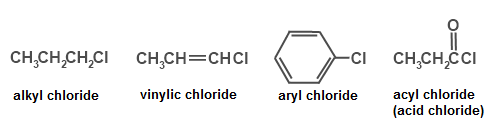
Figure 02: Différence entre halogénure alkyle et halogénure d'aryle
Test chimique pour distinguer les halogénures alkyles et l'halogénure d'aryle
Pour distinguer un halogénure d'alkyle et un halogénure d'aryle, on peut utiliser un test chimique. Tout d'abord, NaOH doit être ajouté suivi d'un chauffage. Ensuite, le mélange est refroidi et HNO3 ID est ajouté, suivi de l'ajout d'Agno3. L'halogénure alkyle peut donner un précipité blanc alors que l'halogénure d'aryle ne. C'est parce que les halogénures d'aryle ne subissent pas de substitution nucléophile, contrairement aux halogénures alkyle. La raison de ne pas subir de substitution nucléophile est que le nuage électronique de l'anneau aromatique provoque une répulsion du nucléophile.
Quelle est la différence entre l'halogénure alkyle et l'halogénure d'aryle?
Halogénure alkyle vs halogénure d'aryle | |
| L'halogénure alkyle est un composé ayant un atome halogène attaché à une chaîne d'atomes de carbone. | L'halogénure aaryl est une molécule ayant un atome halogène attaché à un SP2 Carbone hybridé dans un anneau aromatique directement. |
| Attachement de l'atome halogène | |
| L'atome halogène est attaché à SP3 Atome de carbone hybridé dans les halogénures alkyliques. | L'atome halogène est attaché à un sp2 Atome de carbone hybridé dans les halogénures d'aryle. |
| Structure | |
| Les halogénures alkyles ont une structure linéaire ou ramifiée la plupart du temps. | Les halogénures d'aryle sont toujours des structures ennemies. |
| Densité d'électron | |
| La liaison de carbone-halide des halogénures alkyle a une faible densité d'électrons par rapport aux halogénures d'aryle. | La liaison de carbone-halide des halogénures d'aryle a une forte densité d'électrons. |
| Réactions | |
| Les halogénures alkyles subissent une substitution nucléophile. | Les halogénures d'aryle ne subissent pas de substitution nucléophile. |
Résumé - Halogénure alkyle vs halogénure d'aryle
Les halogénures alkyles et les halogénures d'aryle sont des halogénures organiques. La principale différence entre l'alkyle et l'halogénure d'aryle est que l'atome d'halogène dans les halogénures d'alkyle est attaché à un SP3 Atome de carbone hybridé tandis que dans les halogénures d'aryle, il est attaché à un SP2 atome de carbone hybridé.
Les références:
1. Chasser, D., n.d. Chem.Ucalgaire. [En ligne] Disponible ici. [Consulté 30 05 2017].
2. Clark, J., 2014. LibreTexts. [En ligne] Disponible ici. [Consulté 30 05 2017].
Image gracieuseté:
1. «Halide-Group» par Benjah-BMM27 supposé (basé sur les réclamations du droit d'auteur). (Domaine public) via Commons Wikimedia
2. «Organohalogène-chlorures» Richard-59 - üleslaadija Oma Töö (CC BY-SA 3.0) via Commons Wikimedia


