Quelle est la différence entre l'éthanol et le méthoxyméthane

Le différence clé entre l'éthanol et le méthoxyméthane Est-ce que l'éthanol se produit comme un liquide incolore qui est très volatil à température ambiante, tandis que le méthoxyméthane se produit comme un gaz incolore à température ambiante.
L'éthanol et le méthoxyméthane ont la même formule chimique mais différentes structures chimiques, qui détermine les différentes propriétés chimiques de ces composés. L'éthanol ou l'alcool éthylique est un composé organique ayant la formule chimique C2H5OH. Le méthoxyméthane est un composé éther ayant la formule chimique C2H6O.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que l'éthanol
3. Qu'est-ce que le méthoxyméthane
4. Éthanol vs méthoxyméthane sous forme tabulaire
5. Résumé - Ethanol vs méthoxyméthane
Qu'est-ce que l'éthanol?
L'éthanol ou l'alcool éthylique est un composé organique ayant la formule chimique C2H5OH. C'est utile comme carburant. Cependant, c'est le même composé que nous trouvons dans les boissons alcoolisées. Le plus souvent, ce carburant est utilisé comme carburant, comme additif de biocarburant pour l'essence.

Figure 01: Une bouteille d'éthanol
Il est possible de produire de l'éthanol par des moyens biologiques ou chimiques. Les principales étapes de la production d'éthanol par des moyens biologiques comprennent la fermentation, la distillation et la déshydratation. Pendant la fermentation, les microbes agissent sur le sucre pour le convertir en éthanol. L'étape de distillation implique l'élimination des microbes et la plupart de l'eau. Là, le produit de la fermentation est chauffé, donc la fraction d'éthanol s'évapore. Par la suite, nous devons déshydrater le produit final de la distillation afin d'obtenir une fraction très pure d'éthanol. De plus, la production d'éthanol via des moyens chimiques comprend la réaction de l'éthène avec de la vapeur.
Qu'est-ce que le méthoxyméthane?
Le méthoxyméthane est un composé éther ayant la formule chimique C2H6O. Le nom commun de ce composé est l'éther diméthylique. Ce composé est bien connu pour ses propriétés de solvant. Il a deux groupes méthyle liés via un atome d'oxygène; Les deux groupes méthyle sont liés au même atome d'oxygène.
La masse molaire du méthoxyméthane est 46.07 g / mol. Le point de fusion de cette substance est de -141 degrés Celsius tandis que le point d'ébullition est de -24 degrés Celsius. Il se produit comme un gaz incolore à température ambiante et a une odeur semblable à l'éther. De plus, l'éther diméthylique n'est pas soluble dans l'eau.
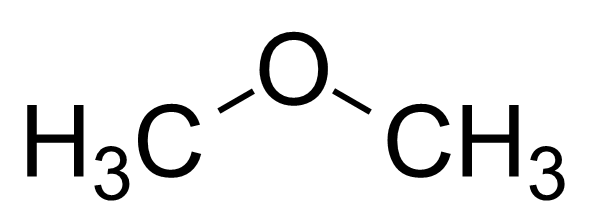
Figure 02: La structure chimique du méthoxyméthane
L'éther diméthylique est un composé non polaire. Cela signifie que l'éther diméthylique n'a pas de polarité. C'est à cause de sa structure moléculaire symétrique. Par conséquent, c'est un bon solvant pour les composés non polaires. Cependant, il n'est pas réactif chimiquement par rapport à d'autres composés organiques.
Quelle est la différence entre l'éthanol et le méthoxyméthane?
L'éthanol et le méthoxyméthane ont la même formule chimique mais différentes structures chimiques, qui détermine les différentes propriétés chimiques de ces composés. La principale différence entre l'éthanol et le méthoxyméthane est que l'éthanol se produit comme un liquide incolore qui est très volatile à température ambiante, tandis que le méthoxyméthane se produit comme un gaz incolore à température ambiante.
De plus, l'éthanol est un alcool avec une odeur alcoolique caractéristique, tandis que le méthoxyméthane est un éther ayant une odeur semblable à l'éther. De plus, l'éthanol et le méthoxyméthane ont des formules chimiques similaires qui sont disposées dans différentes structures; Par exemple, l'éthanol a un groupe hydroxyle (groupe OH) tandis que le méthoxyméthane n'a pas de groupes hydroxyle.
L'infographie ci-dessous présente les différences entre l'éthanol et le méthoxyméthane sous forme tabulaire pour une comparaison côte à côte.
Résumé - Ethanol vs méthoxyméthane
L'éthanol ou l'alcool éthylique est un composé organique ayant la formule chimique C2H5OH. Le méthoxyméthane est un composé d'éther ayant la formule chimique C2H6O. La principale différence entre l'éthanol et le méthoxyméthane est que l'éthanol se produit comme un liquide incolore qui est très volatile à température ambiante, tandis que le méthoxyméthane se produit comme un gaz incolore à température ambiante.
Référence:
1. «L'éther diméthylique." Centre national d'information sur la biotechnologie. Base de données de composés PubChem, U.S. Bibliothèque nationale de médecine.
Image gracieuseté:
1. «Ethanol-Alcohol-Protection-Covid-19» (CC0) via Pixabay
2. «Diméthyl Ether sans paires solitaires» de B Levin13 - Propre travaux (CC BY-SA 3.0) via Commons Wikimedia


