Quelle est la différence entre la constante critique et la constante de van der Waals
Le Différence clé entre la constante critique et la constante de van der Waals Est-ce que la constante critique fait référence aux valeurs de température, de pression et de densité pour une substance au point critique, tandis que les constantes de van der Waals donnent la température, la pression et.
La seule différence entre la constante critique et les valeurs constantes de van der Waals est le point auquel les valeurs sont calculées. Par conséquent, nous pouvons dériver des valeurs constantes critiques en utilisant des valeurs constantes de van der Waals en utilisant les valeurs de points critiques dans l'équation de van der Waals.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que la constante critique
3. Quelle est la constante van der Waals
4. Constante critique vs van der waals constante dans la forme tabulaire
5. Résumé - constante critique vs van der waals constante
Qu'est-ce que la constante critique?
La constante critique est la température critique, la pression critique ou la densité critique de toute substance. Ce terme est généralement considéré comme un nom pluriel car il peut se référer à trois conditions (température, pression ou densité) au même point. Nous pouvons abréger la température critique en tant que TC, la pression critique comme PC et la densité critique comme VC. De plus, nous pouvons calculer les constantes critiques en utilisant les valeurs des constantes de van der Waals.

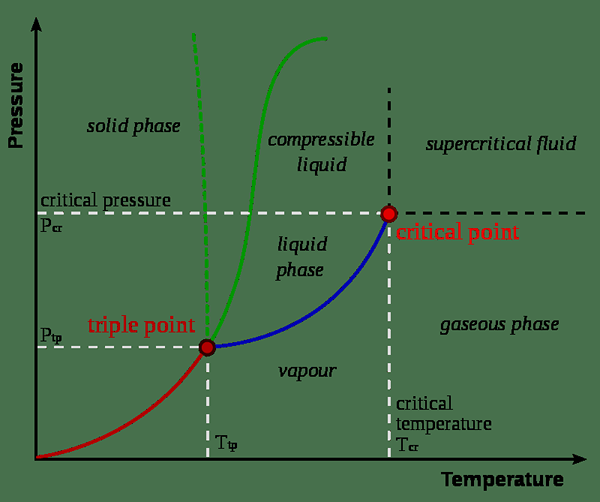
Figure 01: Diagramme de phase
En règle générale, des valeurs constantes critiques sont données pour le point critique d'une substance. Le point critique d'une substance est le point final de la courbe d'équilibre de phase de cette substance. Une courbe d'équilibre de phase ou un diagramme de phase est le graphique de la pression par rapport à la température dans laquelle les changements de phase de la substance sont affichés. Cela montre les températures et la pression à laquelle la substance existe comme un solide, un liquide ou un gaz. Le point critique est la température et la pression à laquelle les phases liquide et vapeur coexistent.
Quelle est la constante van der Waals?
Les constantes de van der Waals sont les valeurs constantes que nous utilisons dans l'équation de van der Waals. L'équation de van der Waal est la version modifiée de la loi sur le gaz idéal. Cette équation peut être utilisée pour les gaz idéaux ainsi que pour les gaz réels. La loi idéale sur le gaz ne peut pas être utilisée pour les gaz réels car le volume de molécules de gaz est considérable par rapport au volume du gaz réel, et il existe des forces d'attraction entre les molécules de gaz réelles (les molécules de gaz idéales ont un volume négligeable par rapport au volume total , et il n'y a pas de forces d'attraction entre les molécules de gaz).
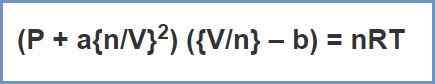
Figure 02: Équation de van der Waals
Ici, «A» est une constante qui dépend du type de gaz et de «B» est également une constante qui donne le volume par mole de gaz (occupé par les molécules de gaz). Ceux-ci sont utilisés comme corrections de l'équation de la loi idéale.
Le volume d'une molécule de gaz réelle n'est pas négligeable (contrairement aux gaz idéaux). Par conséquent, la correction du volume est effectuée. (V-B) est la correction du volume. Cela donne le volume réel disponible pour que la molécule de gaz se déplace (volume réel = volume total - volume effectif).
La pression d'un gaz est la pression exercée par une molécule de gaz sur la paroi du récipient. Puisqu'il y a des forces d'attraction entre les molécules de gaz réelles, la pression est différente de celle du comportement idéal. Alors une correction de pression doit être effectuée. (P + a n / v 2) est la correction de la pression. (Pression idéale = pression observée + correction de pression).
Quelle est la différence entre la constante critique et la constante de van der Waals?
Constante critique et van der waal constante sont des termes légèrement différents les uns des autres. La principale différence entre la constante critique et la constante de van der Waals est que la constante critique fait référence à la température, à la pression et aux valeurs de densité pour une substance au point critique, tandis que les constantes de van der Waals donnent la température, la pression et les valeurs de densité pour une substance à tout moment.
Le tableau suivant résume la différence entre la constante critique et la constante de van der Waals.
Résumé - constante critique vs van der waals constante
Constante critique et van der waal constante sont des termes légèrement différents les uns des autres. La principale différence entre la constante critique et la constante de van der Waals est que le terme constante critique fait référence à la température, à la pression et aux valeurs de densité pour une substance au point critique, tandis que les constantes de van der Waals donnent la température, la pression et les valeurs de densité pour une substance à tout moment.
Référence:
1. Baratuci, William. «Déterminer les constantes de van der Waal." CH2, Leçon F, page 6 - Déterminer les constantes de van der Waal.
Image gracieuseté:
1. «Phase-diag2» par Matthieumarechal (CC By-Sa 3.0) via Commons Wikimedia


