Différence entre le tautomérisme et le métaméririsme

Le différence clé entre le tautomérisme et le métaméritisme Le tautomérisme fait référence à l'équilibre dynamique entre deux composés ayant la même formule moléculaire tandis que le métaméririsme se réfère à l'isomérisme structurel dans lequel différents groupes alkyle sont attachés au même groupe fonctionnel.
L'isomérisme est l'existence de composés chimiques ayant la même formule structurelle mais des arrangements spatiaux différents. Par conséquent, les isomères ont le même nombre d'atomes dans chaque élément, mais leur arrangement est différent. Les isomères peuvent être principalement classés en deux groupes comme isomères structurels et stéréoisomères. Le tautomérisme et le métaméririsme sont deux subdivisions de l'isomérisme structurel.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que le tautomérisme
3. Qu'est-ce que le métaméririsme
4. Comparaison côte à côte - Tautomérisme vs métaméririsme sous forme tabulaire
5. Résumé
Qu'est-ce que le tautomérisme?
Le tautomérisme est un concept de chimie qui décrive l'effet d'avoir plusieurs composés capables d'interconversion via la relocalisation d'un proton. Ce phénomène est le plus fréquent dans les acides aminés et les acides nucléiques. Le processus de cette interconversion est la «tautomérisation». La tautomérisation est en fait une réaction chimique. Dans ce processus, la relocalisation de protons signifie l'échange d'un atome d'hydrogène entre deux autres formes d'atomes. Ici, l'atome d'hydrogène forme une liaison covalente avec le nouvel atome qui reçoit l'atome d'hydrogène. Après la formation, les tautomères existent en équilibre. Ces composés existent toujours dans un mélange de deux formes de composé car elles tentent de préparer une forme tautomérique distincte.

Lorsque la tautomérisation a lieu, le squelette de carbone de la molécule ne change pas. En fait, seule la position des protons et des électrons est modifiée. Nous pouvons classer le processus de tautomérisation comme un processus chimique intramoléculaire de conversion d'une forme de tautomère sous une forme différente. Par exemple, le tautomérisme kéto-énol, qui est une réaction acide ou catalysée par la base, est une réaction commune. Habituellement, la forme céto d'un composé organique est plus stable, mais dans certains États, la forme énol est plus stable que la forme céto.
Qu'est-ce que le métaméririsme?
Le métaméririsme se produit lorsque les groupes alkyle sur les côtés des groupes fonctionnels diffèrent les uns des autres. Cela signifie qu'il s'agit d'une distribution inégale des atomes de carbone. Le métaméririsme appartient à la même série homologue, ce qui signifie que le nombre d'atomes de carbone peut être augmenté progressivement pour obtenir des isomères différents. Par conséquent, les structures ne diffèrent que par le nombre de ch2 groupes dans la chaîne carbone principale.
Les groupes alkyle sont toujours attachés aux côtés d'un atome divalent comme l'oxygène ou le sulfure, ou les groupes alkyle peuvent être attachés à un groupe divalent tel que -nh-. Nous pouvons rarement trouver le métaméririsme en raison de ces limitations. Par conséquent, la plupart des composés que nous pouvons trouver dans le métaméririsme sont des éthers et des amines.
Par exemple, l'éther diéthylique et l'éther méthyl propyl sont des métamères. Ici, le groupe fonctionnel est éther, et l'atome divalent est un atome d'oxygène. L'éther diéthylique a deux groupes éthyliques tandis que l'éther de méthyl propyle a un méthyle et un groupe propyl sur les côtés de l'atome d'oxygène.
Quelle est la différence entre le tautomérisme et le métaméririsme?
La principale différence entre le tautomérisme et le métaméririsme est que le tautomérisme se réfère à l'équilibre dynamique entre deux composés ayant la même formule moléculaire tandis que le métamérise se réfère à l'isomérisme structurel dans lequel différents groupes d'alkyle sont attachés au même groupe fonctionnel. Dans le tautomérisme, les isomères diffèrent les uns des autres en fonction de la position des protons alors que, dans le métaméririsme, les isomères diffèrent les uns des autres en fonction des groupes alkyle attachés au groupe fonctionnel principal.
L'infographie ci-dessous résume la différence entre le tautomérisme et le métaméririsme.
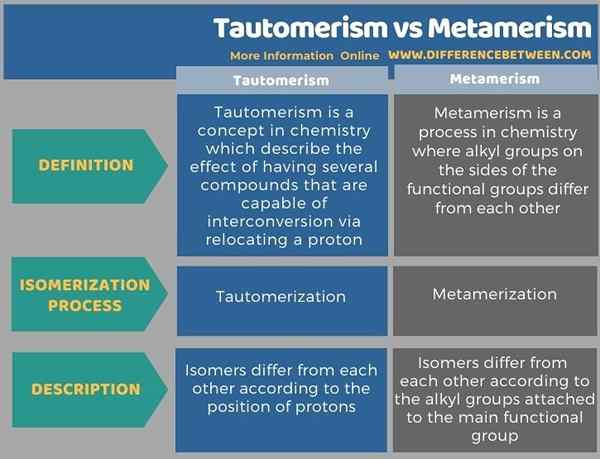
Résumé - Tautomérisme vs métaméririsme
Le tautomérisme et le métaméritisme sont deux concepts en chimie organique. La principale différence entre le tautomérisme et le métaméririsme est que le tautomérisme se réfère à l'équilibre dynamique entre deux composés ayant la même formule moléculaire tandis que le métaméririsme se réfère à l'isomérisme structurel dans lequel différents groupes alkyle sont attachés au même groupe fonctionnel.
Référence:
1. Helmenstine, Anne Marie «Définition des isomères et exemples en chimie."Thoughtco, février. 11, 2020, disponible ici.
Image gracieuseté:
1. «Phénol Tautomers» par Ed (Edgar181) - propre travail (domaine public) via Commons Wikimedia


