Différence entre l'amide et la liaison peptidique
Le différence clé entre l'amide et la liaison peptidique est que Une liaison amide se forme entre un groupe hydroxyle et un groupe amino de deux molécules alors qu'une liaison peptidique se forme entre deux molécules d'acide aminé pendant la formation d'une chaîne peptidique.
Les liaisons amide et les liaisons peptidiques sont des liaisons biochimiques qui se forment entre un atome de carbone et un atome d'azote de deux molécules distinctes. Habituellement, ces liaisons se forment entre deux molécules d'acides aminés.
CONTENU
1. Aperçu et différence clé
2. Que sont les obligations amides
3. Que sont les liaisons peptidiques
4. Comparaison côte à côte - Amide vs liaison peptidique sous forme tabulaire
5. Résumé
Que sont les obligations amides?
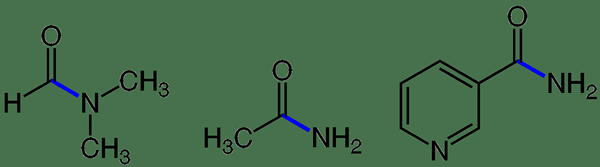
Les liaisons amide sont un type de liaison covalente qui forme un amide comme produit final. Il existe trois principaux types d'amides comme carboxamides, sulfonamides et phosphoramides. Cependant, les amides les plus simples sont des dérivés de l'ammoniac.

Figure 01: Différentes obligations amides
Les amides sont généralement classés comme des bases très faibles par rapport aux amines. Par conséquent, ces substances ne présentent pas de propriétés acides dans l'eau. Une liaison peptidique est un type de liaison amide. Ici, la liaison amide se forme lorsque le groupe d'acide carboxylique d'un acide aminé réagit avec le groupe amine d'un autre acide aminé. Une liaison covalente se forme en éliminant une molécule d'eau. Par conséquent, c'est une réaction de condensation.
Que sont les liaisons peptidiques?
Une liaison peptidique est un type de liaison covalente qui se forme entre deux acides aminés. Une liaison peptidique se forme entre un atome de carbone d'un acide aminé et l'atome d'azote de l'acide aminé qui se produit avec l'élimination d'une molécule d'eau. Lorsque l'on considère la structure de base de l'acide aminé, il se compose d'un atome de carbone central attaché à un groupe carboxylique, un groupe amino, un atome d'hydrogène et un groupe alkyle. Généralement, les acides aminés diffèrent les uns des autres en fonction de la structure du groupe alkyle.
Pendant la formation d'une liaison peptidique, une réaction de condensation se produit entre deux acides aminés. Ici, l'acide carboxylique d'un acide aminé réagit avec le groupe amine d'un autre acide aminé, libérant une molécule d'eau. Le groupe -OH du groupe acide carboxylique forme une molécule d'eau, se combinant avec un hydrogène du groupe amine.
Nous pouvons abréger la liaison peptidique comme -conh- liaison parce que la liaison qui forme implique ces quatre atomes. Lorsque deux acides aminés se lient à travers une liaison peptidique, le produit final est un dipeptide. Cependant, si plusieurs acides aminés se lient les uns aux autres, alors un oligopeptide se forme. Si un nombre élevé d'acides aminés se lie entre eux par des liaisons peptidiques, la molécule complexe est un polypeptide.
Une liaison peptidique peut subir des réactions d'hydrolyse. L'hydrolyse décompose la liaison, séparant les deux acides aminés. Même si le processus est très lent, une hydrolyse peut se produire en présence d'eau.
Quelle est la différence entre l'amide et la liaison peptidique?
Les liaisons amides et peptidiques sont des liaisons biochimiques. La principale différence entre l'amide et la liaison peptidique est qu'une liaison amide se forme entre un groupe hydroxyle et un groupe amino de deux molécules alors qu'une liaison peptidique se forme entre deux molécules d'acide aminé pendant la formation d'une chaîne peptidique.
En dessous de l'infographie résume la différence entre l'amide et la liaison peptidique.
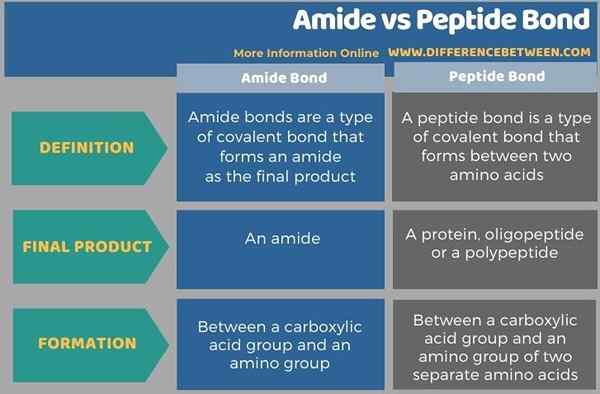
Résumé - Amide vs liaison peptidique
En biochimie, les liaisons amide et les liaisons peptidiques jouent un rôle très important dans la formation d'une molécule protéique. La principale différence entre l'amide et la liaison peptidique est qu'une liaison amide se forme entre un groupe hydroxyle et un groupe amino de deux molécules alors qu'une liaison peptidique se forme entre deux molécules d'acide aminé pendant la formation d'une chaîne peptidique.
Référence:
1. Helmenstine, Anne Marie. «Définition de l'amide et exemples en chimie."Thoughtco, février. 11, 2020, disponible ici.
Image gracieuseté:
1. «Amide Bond Amides V.1 ”par Jü - Propre travaux (CC0) via Commons Wikimedia


