Différence entre l'acide organique et l'acide inorganique
Le différence clé entre l'acide organique et l'acide inorganique est que Les acides organiques contiennent essentiellement des liaisons hydrogène carbone dans leur structure tandis que les acides inorganiques peuvent ou non contenir du carbone.
Les acides sont définis de plusieurs manières par divers scientifiques. Quelles que soient ces différentes définitions, nous identifions normalement un acide comme donneur de protons. Les acides ont un goût aigre. Le jus de citron vert et le vinaigre sont deux acides que nous voyons habituellement dans nos maisons. Ils réagissent avec des bases, produisant de l'eau; Ils réagissent également avec les métaux pour former H2, Augmentation du taux de corrosion des métaux. Les acides peuvent être classés en deux groupes en fonction de leur capacité à dissocier et à produire des protons. Les acides forts sont complètement ionisés dans une solution pour donner des protons. Acides faibles partiellement dissociés et donnent moins de quantités de protons. De plus, nous pouvons également classer les acides comme des acides organiques et inorganiques.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que l'acide organique
3. Qu'est-ce que l'acide inorganique
4. Comparaison côte à côte - acide organique vs acide inorganique sous forme tabulaire
5. Résumé
Qu'est-ce que l'acide organique?
Les acides organiques sont des composés organiques qui peuvent agir comme des acides. Les acides organiques contiennent essentiellement de l'hydrogène et du carbone avec un autre élément / s. Les acides organiques les plus courants sont l'acide acétique, l'acide lactique, l'acide citrique, l'acide formique, etc. Ces acides ont un groupe -cooh.
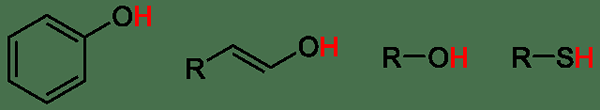
Figure 01: Acides organiques faibles
Parfois, les composés organiques ayant des groupes -oh, -sh peuvent également agir comme des acides. Par exemple, les alcools ont des propriétés acides. L'acétylène peut également donner un proton montrant des propriétés acides. Les hydrogènes attachés au carbone alpha des aldéhydes, et les cétones sont également des protons acides. Souvent, les acides organiques sont des acides faibles et se dissocient partiellement dans l'eau.
Qu'est-ce que l'acide inorganique?
Les acides inorganiques sont les composés acides qui proviennent de sources inorganiques. Un synonyme d'acides inorganiques est les acides minéraux, et ils proviennent de sources minérales.

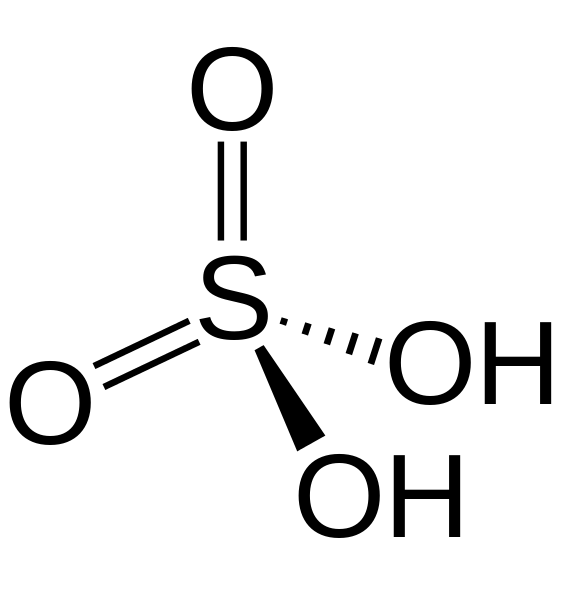
Figure 02: L'acide sulfurique est un acide inorganique
Les acides inorganiques libèrent des protons lorsqu'ils sont dissous dans l'eau. Il y a de forts acides inorganiques comme HCL, HNO3, H2DONC4 et les acides inorganiques faibles comme HCN ou H2S.
Quelle est la différence entre l'acide organique et l'acide inorganique?
La principale différence entre l'acide organique et l'acide inorganique est que les acides organiques contiennent essentiellement des liaisons hydrogène en carbone dans leur structure tandis que les acides inorganiques peuvent ou non contenir du carbone. Généralement, les acides organiques sont des acides plus faibles que les acides inorganiques. La plupart des acides organiques sont insolubles dans l'eau (parfois miscible avec l'eau) mais solubles dans les solvants organiques. Cependant, les acides inorganiques sont généralement bien solubles dans l'eau et non solubles dans les solvants organiques. Les acides organiques ont une origine biologique, alors que les acides inorganiques n'ont pas. Les acides inorganiques sont dérivés de composés inorganiques / sources minérales. De plus, les acides minéraux sont très réactifs avec les métaux, et ils ont une capacité corrosive que les acides organiques.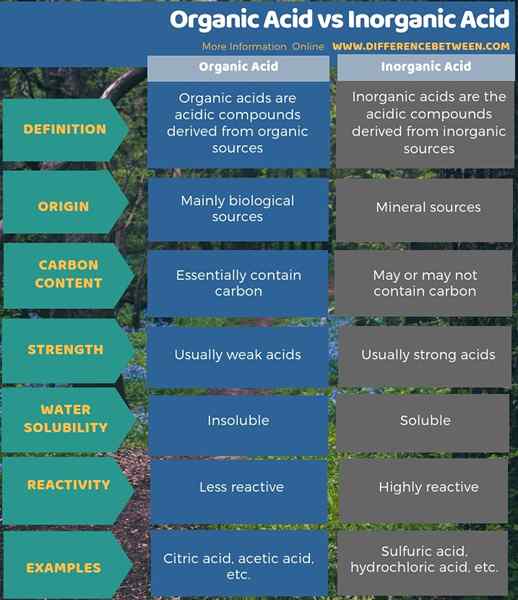
Résumé - Acide organique vs acide inorganique
Les acides peuvent être classés comme acides organiques et inorganiques. La principale différence entre l'acide organique et l'acide inorganique est que les acides organiques contiennent essentiellement des liaisons hydrogène en carbone dans leur structure tandis que les acides inorganiques peuvent ou non contenir du carbone.
Référence:
1. McKenzie, Marian et Virginia Corrigan. «Flavour de la pomme de terre.«Avances en chimie et technologie des pommes de terre, 2016, pp. 339-368., doi: 10.1016 / B978-0-12-800002-1.00012-1.
Image gracieuseté:
1. «Acides organiques faibles» par HBF878 - Propre travaux (CC0) via Commons Wikimedia
2. «Acide sulfurique» par Leyo - Propre travaux (domaine public) via Commons Wikimedia


