Différence entre le diagramme Latimer et le diagramme de gel
Le différence clé entre le diagramme Latimer et le diagramme de gel est que Le diagramme Latimer résume les potentiels d'électrode standard d'un élément chimique tandis que le diagramme de gel résume la stabilité relative de différents états d'oxydation d'une substance.
Le diagramme Latimer et le diagramme de gel sont fondamentalement importants pour montrer les détails sur les réactions redox. De plus, ces diagrammes ont été nommés d'après les scientifiques qui les ont créés à l'origine; Le diagramme Latimer a tiré son nom de Wendell Mitchell Latimer tandis que le diagramme de gel a été nommé d'après Arthur Atwater Frost.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que le diagramme Latimer
3. Qu'est-ce que le diagramme de gel
4. Comparaison côte à côte - Diagramme Latimer vs Diagramme de gel dans la forme tabulaire
5. Résumé
Qu'est-ce que le diagramme Latimer?
Le diagramme Latimer est un résumé des potentiels d'électrode standard d'un élément. Le diagramme est nommé d'après le chimiste américain Wendell Mitchell Latimer. Lors de la construction de ce type de diagrammes, nous devons écrire la forme hautement oxydée de l'élément chimique sur le côté gauche. Ensuite, nous pouvons écrire les états d'oxydation par ordre décroissant à gauche - le coin gauche aura le moins d'oxydation à l'état d'oxydation. Entre ces états d'oxydation, nous utilisons une flèche (pointe de flèche vers la gauche). De plus, sur le dessus de la flèche, nous devons écrire le potentiel d'électrode standard pour la réaction de conversion de l'état d'oxydation sur le côté droit vers le côté gauche. Par exemple,
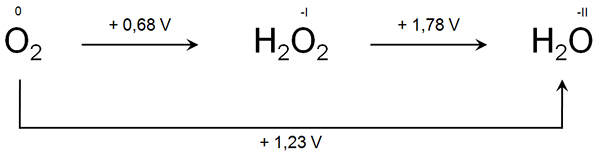
Figure 01: un diagramme Latimer montrant les différents états d'oxydation de l'atome d'oxygène
L'élément chimique que nous avons considéré dans l'exemple ci-dessus est l'oxygène. Il a les espèces chimiques suivantes avec des états d'oxydation correspondants d'oxygène:
- O2 - L'état d'oxydation est nul
- H2O2 - L'état d'oxydation de l'oxygène est -1
- H2O - L'état d'oxydation de l'oxygène est -2
Le diagramme Latimer est important pour construire un diagramme de gel, car nous pouvons obtenir un potentiel d'électrode d'étapes non adjacentes d'une réaction nécessaire au développement du diagramme de gel. De plus, il est important d'indiquer si une certaines espèces chimiques subit une déprotonation dans les conditions dans lesquelles le potentiel d'électrode est donné.
Qu'est-ce que le diagramme de gel?
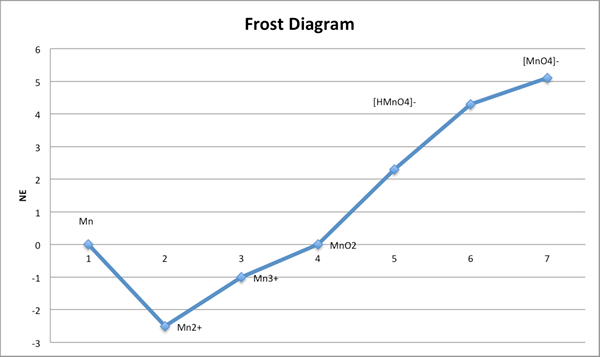
Le diagramme de gel est une illustration qui montre la stabilité relative de différents états d'oxydation d'une substance. Il est important dans la chimie et l'électrochimie inorganiques. De plus, c'est un graphique, et il a l'état d'oxydation à l'axe des x et l'énergie libre à l'axe y. Ici, le graphique dépend du pH. Par conséquent, nous devons inclure le pH auquel nous prenons des mesures. Nous pouvons déterminer l'énergie libre en utilisant des demi-réactions oxydation-réduction. De plus, nous pouvons déterminer facilement les potentiels de réduction en utilisant ce diagramme plutôt que d'utiliser un diagramme Latimer.

Figure 02: un diagramme de gel
Lors de la construction du diagramme, nous devons marquer l'état d'oxydation à l'axe des x et l'énergie libre à l'axe y avec zéro au milieu. Parce que l'énergie libre a des valeurs négatives et positives. De plus, la pente du graphique montre le potentiel d'électrode standard entre les deux états d'oxydation.
Quelle est la différence entre le diagramme Latimer et le diagramme de gel?
Le diagramme de Latimer et le diagramme de gel sont importants pour déterminer les informations sur l'oxydation et la réduction des réactions redox. Cependant, la principale différence entre le diagramme Latimer et le diagramme de gel est que le diagramme Latimer résume les potentiels d'électrode standard d'un élément chimique, mais le diagramme de gel résume la stabilité relative de différents états d'oxydation d'une substance.
L'infographie ci-dessous résume la différence entre le diagramme Latimer et le diagramme de gel sous forme tabulaire.
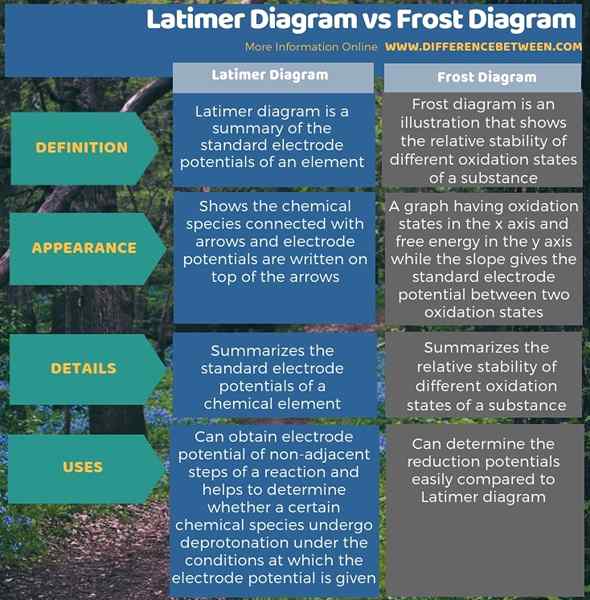
Résumé - Diagramme Latimer vs Diagramme de gel
Dans l'ensemble, le diagramme Latimer et le diagramme de gel nous aident à déterminer les informations sur l'oxydation et la réduction des réactions redox. Mais, la principale différence entre le diagramme Latimer et le diagramme de gel est que le diagramme Latimer résume les potentiels d'électrode standard d'un élément chimique, tandis que le diagramme de gel résume la stabilité relative de différents états d'oxydation d'une substance.
Référence:
1. «Diagrammes utilisés dans la chimie redox. »Université de l'Oregon de l'Ouest, disponible ici.
2. «4.3: Diagrammes Latimer et Frost.”Chemistry LibreTexts, LibreTexts, 5 juin 2019, disponible ici.
Image gracieuseté:
1. «Latimerdiagram Zuurstof» par Dr.T - propre travail (CC BY-SA 3.0) via Commons Wikimedia
2. «Frost Diagram» de JLange1125 - J'ai fait le diagramme dans Excel (CC BY-SA 3.0) via Commons Wikimedia


