Différence entre le taux instantané et le taux moyen
Différence clé - Taux instantané vs taux moyen
Dans les réactions chimiques, la vitesse de réaction peut être déterminée de deux manières en tant que vitesse instantanée et vitesse moyenne. La principale différence entre le taux instantané et le taux moyen est que Le taux instantané mesure le changement de concentration de réactifs ou de produits pendant une période connue tandis que le taux moyen mesure le changement de concentration de réactifs ou de produits pendant tout le temps pris pour l'achèvement de la réaction chimique.
La vitesse de réaction d'une réaction chimique est la mesure de la variation de la concentration des réactifs utilisés ou les produits formés pendant la réaction. Il est également connu comme la vitesse de réaction.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que le taux instantané
3. Quel est le taux moyen
4. Comparaison côte à côte - Taux instantané vs taux moyen de la forme tabulaire
5. Résumé
Qu'est-ce que le taux instantané?
Le taux instantané est la vitesse d'une réaction chimique qui est mesurée comme le changement de concentration des réactifs ou des produits pendant une période connue. Dans cette méthode, la vitesse de la réaction pendant un instant spécifique dans le temps est mesurée. Il peut également être mesuré comme la vitesse de la réaction à un moment particulier. Le taux instantané est également connu sous le nom de taux différentiel.
La vitesse de réaction d'une réaction chimique est souvent différente d'un point à l'autre pendant la progression de la réaction (la vitesse de réaction change en continu). La vitesse de réaction ralentit lorsque les réactifs sont utilisés pour la réaction. En effet, la concentration de réactifs diminue avec la progression de la réaction (les réactifs sont consommés par la réaction chimique).
Formule instantanée du taux de changement
Le taux instantané est donné comme ci-dessous.
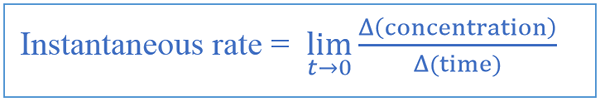

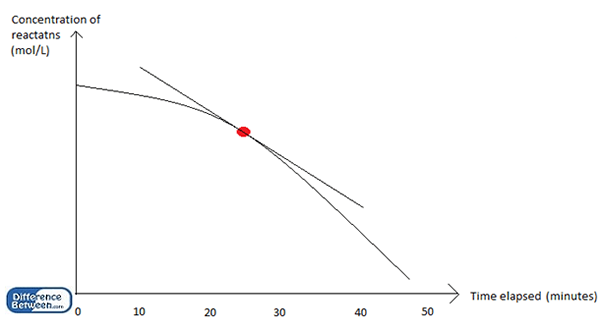
Le graphique ci-dessus montre la diminution de la concentration des réactifs avec le temps dans une réaction chimique; La vitesse instantanée est la vitesse de la réaction à un point particulier (point de couleur rouge); Le taux moyen est calculé en divisant la concentration totale de réactifs (au début) à partir du temps total (50 minutes).
Quel est le taux moyen?
La vitesse moyenne est le taux d'une réaction chimique qui est mesurée comme le changement de concentration des réactifs ou des produits pendant toute la période de la progression de la réaction chimique. La vitesse de réaction est différente d'un point particulier à un autre point pendant la progression d'une réaction chimique puisque la vitesse de réaction change en continu. Mais le taux moyen donne le taux moyen de tous ces points, mais il ne donne aucune information sur le point entre l'initiation et l'achèvement de la réaction.
Taux de changement moyen de changement
Le taux de variation moyen est donné comme ci-dessous.
Taux moyen = Δ (concentration de réactif ou de produit) / Δ (temps)
La vitesse moyenne ne donne que le taux moyen de toute la réaction, mais ce taux moyen n'est pas le taux réel tout au long de la réaction, car la vitesse de réaction diminue avec la consommation de réactifs.
Quelle est la différence entre le taux instantané et le taux moyen?
Taux instantané vs taux moyen | |
| Le taux instantané est le taux d'une réaction chimique qui est mesurée comme le changement de concentration de réactifs ou de produits pendant une période connue. | Le taux moyen est la vitesse d'une réaction chimique qui est mesurée comme le changement de concentration de réactifs ou de produits pendant toute la période de progression de la réaction chimique. |
| Temps | |
| Le taux instantané est mesuré pour un moment particulier ou pour une période de temps très courte. | Le taux moyen est mesuré pendant une période plus longue. |
| Formule de calcul | |
| Taux de changement instantané = LIM (T → 0) [δ (concentration de réactif ou de produit) / δ (temps)] | Taux de changement moyen = δ (concentration de réactif ou de produit) / Δ (temps) |
Résumé - Taux instantané vs taux moyen
Le taux de réaction d'une réaction chimique est le taux de variation de concentration de réactifs ou de produits. La vitesse de réaction peut être déterminée sous deux formes comme un taux instantané et un taux moyen. La principale différence entre le taux instantané et le taux moyen est que le taux instantané mesure la variation de la concentration de réactifs ou de produits pendant une période connue tandis que le taux moyen mesure la variation de la concentration de réactifs ou de produits pendant tout le temps pour la fin de la fin de réaction chimique.
Référence:
1. Laidler, Keith J. "Taux de réaction.»Encyclopædia Britannica, Encyclopædia Britannica, Inc., 23 avril. 2014, disponible ici.
2. «Trouver un taux de changement instantané." Étude.com, disponible ici.
3. LibreTexts. "Taux de réaction.”Chemistry LibreTexts, LibreTexts, 21 juillet 2016, disponible ici.


