Différence entre l'hydrolyse et la déshydratation

Hydrolyse vs déshydratation
L'eau est très importante pour la survie des êtres vivants. Il a de nombreux usages. Lorsque l'eau n'est pas en quantité suffisante, elle affecte de nombreuses réactions importantes dans le corps.
Hydrolyse
Ceci est une réaction où une liaison chimique est rompue à l'aide d'une molécule d'eau. Au cours de cette réaction, une molécule d'eau se divise en proton et en ion hydroxyde. Ensuite, ces deux ions sont ajoutés à deux parties de la molécule où la liaison est cassée. Par exemple, ce qui suit est un ester. La liaison ester est entre -co et -o.
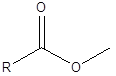
Dans l'hydrolyse, le proton de l'eau s'ajoute du côté -o, et l'ion hydroxyde s'ajoute au côté -co. Par conséquent, à la suite de l'hydrolyse, un alcool et un acide carboxylique se forment qui étaient les réactifs lors de la formation de l'ester.
L'hydrolyse est importante pour décomposer les polymères qui ont été fabriqués par polymérisation de condensation. Les polymérisations de condensation sont un type de réaction chimique où les petites molécules se réunissent pour former une grande molécule unique. La réaction se déroule dans deux groupes fonctionnels dans les molécules. Une autre caractéristique d'une réaction de condensation est que, pendant la réaction, une petite molécule comme l'eau est perdue. Ainsi, l'hydrolyse est le processus réversible de la polymérisation de la condensation. L'exemple ci-dessus montre une hydrolyse d'une molécule organique.
La plupart des réactions d'hydrolyse des molécules organiques doivent être catalysées avec de forts acides et bases. Cependant, simplement, lorsqu'un sel d'un acide faible ou d'une base faible est dissous dans l'eau, il subit également une hydrolyse. Les ionides d'eau et aussi le sel se dissocient en cation et anion. Par exemple, lorsque l'acétate de sodium est dissous dans l'eau, l'acétate réagit avec les protons et forme de l'acide acétique tandis que le sodium interagit avec les ions hydroxyles.
Dans les systèmes vivants, les réactions d'hydrolyse sont très courantes. Dans le système digestif, cela a lieu pour digérer la nourriture que nous apprenons. La génération d'énergie à partir de l'ATP est également due à une réaction d'hydrolyse des liaisons pyrophosphates. La plupart de ces réactions d'hydrolyse biologique sont catalysées avec des enzymes.
Déshydratation
La déshydratation est la condition dans laquelle il n'y a pas le niveau normal d'eau nécessaire. Lorsqu'il est référé à des systèmes biologiques, cela est causé par une grave perte de liquide corporel (par exemple, le sang). Il existe trois types de déshydratation comme hypotonique, hypertonique et isotonique. Étant donné que le niveau d'électrolytes affecte directement le niveau d'eau, il est important de maintenir l'équilibre des électrolytes dans le corps afin de maintenir l'équilibre osmotique.
La déshydratation peut être causée de plusieurs manières. Excès de passage d'urine, de diarrhée, de perte de sang due aux accidents et d'une transpiration excessive sont quelques-unes des façons courantes. La déshydratation peut provoquer des maux de tête, une diminution de la tension artérielle, des étourdissements, des évanouissements. Dans un état extrême de déshydratation, il provoque l'inconscience et la mort.
La déshydratation peut être évitée en buvant suffisamment d'eau. Lorsque beaucoup d'eau est perdue du corps, elle doit être réapprochée (réhydratation orale, injection, etc.).
| Quelle est la différence entre l'hydrolyse et la déshydratation? • La déshydratation est la condition d'avoir moins d'eau que le niveau normal. • L'hydrolyse est une réaction où une liaison chimique est rompue à l'aide d'une molécule d'eau. • La déshydratation affecte les réactions d'hydrolyse car pour que les réactions d'hydrolyse se produisent, il devrait y avoir de l'eau. |


