Différence entre l'hydrogénation et l'hydrogénolyse
Le différence clé entre l'hydrogénation et l'hydrogénolyse est que L'hydrogénation comprend l'ajout d'hydrogène sans clivage des liaisons, tandis que l'hydrogénolyse comprend l'ajout d'hydrogène avec le clivage des liaisons.
L'hydrogénation et l'hydrogénolyse sont des processus industriels importants dans l'industrie alimentaire et l'industrie pétrochimique.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que l'hydrogénation
3. Qu'est-ce que l'hydrogénolyse
4. Comparaison côte à côte - hydrogénation vs hydrogénolyse sous forme tabulaire
5. Résumé
Qu'est-ce que l'hydrogénation?
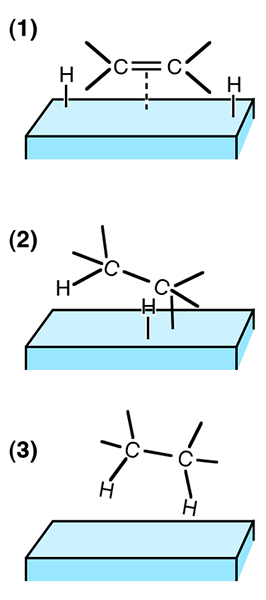
L'hydrogénation est une réaction chimique où l'hydrogène gazeux est ajouté à un composé organique. De plus, ce processus implique principalement la formation de liaisons. De plus, cette réaction nécessite généralement un catalyseur tel que le nickel, le platine ou le palladium. De plus, le processus d'hydrogénation est très important dans les composés organiques saturés.

Figure 01: Processus d'hydrogénation en trois étapes
De plus, le mécanisme de réaction comprend l'ajout de paires d'atomes d'hydrogène à une molécule à la surface du catalyseur. Généralement, les réactifs de cette réaction sont des alcènes (composés insaturés ayant des liaisons doubles entre les atomes de carbone). De plus, pour une réaction d'hydrogénation stable, nous avons besoin de catalyseurs. Cependant, s'il n'y a pas de catalyseur, nous devons fournir des températures très élevées à la réaction pour continuer.
Qu'est-ce que l'hydrogénolyse?
L'hydrogénolyse est une réaction chimique dans laquelle les liaisons chimiques subissent un clivage par des molécules d'hydrogène gazeux. De plus, ce processus comprend le clivage des liaisons C-C et des liaisons C-Heteroatom.
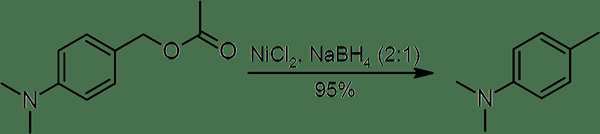
Figure 02: Hydrogénolyse de l'ester benzylique
Ici, l'hétéroatome est généralement de l'oxygène, du soufre, de l'azote, etc. Cette réaction nécessite également des catalyseurs tels que le palladium, les métaux Raney tels que le nickel Raney, etc.
Quelle est la différence entre l'hydrogénation et l'hydrogénolyse?
La principale différence entre l'hydrogénation et l'hydrogénolyse est que l'hydrogénation comprend l'ajout d'hydrogène sans clivage des liaisons, tandis que l'hydrogénolyse comprend l'ajout d'hydrogène avec le clivage des liaisons. L'hydrogénation se produit via l'ajout d'hydrogène pour réduire la saturation sans rompre aucune liaison tandis que l'hydrogénolyse se produit via des liaisons uniques subissent un clivage par l'hydrogène pour réduire les hétéroatomes dans un composé.
L'infographie ci-dessous montre plus d'informations sur la différence entre l'hydrogénation et l'hydrogénolyse.

Résumé - Hydrogénation vs hydrogénolyse
La principale différence entre l'hydrogénation et l'hydrogénolyse est que l'hydrogénation comprend l'ajout d'hydrogène sans clivage des liaisons, tandis que l'hydrogénolyse comprend l'ajout d'hydrogène avec le clivage des liaisons.
Référence:
1. Morales-delarosa, s., et J.m. Campos-martin. «Processus catalytiques et développement du catalyseur dans la biorfinie.”Advances in Biorefineries, 2014, pp. 152-198., doi: 10.1533/9780857097385.1.152.
Image gracieuseté:
1. «Hydrogénation sur Catalyst» de Michael Schmid - Drawing Created Mysel (CC par 1.0) via Commons Wikimedia
2. «Hydrogénolyse d'un ester benzylique par le nickel borure» par lhchem - propre travail (CC by-sa 3.0) via Commons Wikimedia


