Différence entre les isomères géométriques et les isomères structurels

Isomères géométriques vs isomères structurels
Les isomères sont des composés différents avec la même formule moléculaire. Il existe différents types d'isomères. Les isomères peuvent être principalement divisés en deux groupes en tant qu'isomères constitutionnels et stéréoisomères. Les isomères constitutionnels sont des isomères où la connectivité des atomes diffère en molécules. Dans les stéréoisomères, les atomes sont connectés dans la même séquence, contrairement aux isomères constitutionnels. Les stéréoisomères ne diffèrent que par la disposition de leurs atomes dans l'espace. Les stéréoisomères peuvent être de deux types, énantiomères et diastéréomères. Les diastéréomères sont des stéréoisomères, dont les molécules ne sont pas des images miroir les unes des autres. Les énantiomères sont des stéréoisomères, dont les molécules sont des images miroir non superposables les unes des autres. Les énantiomères ne se produisent qu'avec des molécules chirales. Une molécule chirale est définie comme celle qui n'est pas identique à son image miroir. Par conséquent, la molécule chirale et son image miroir sont des énantiomères les uns des autres. Par exemple, la molécule de 2-butanol est chirale, et elle et ses images miroir sont des énantiomères.
Isomères géométriques
Les isomères géométriques sont un type de stéréoisomères. Ce type d'isomères en résulte, lorsque les molécules ont une rotation restreinte, fondamentalement, en raison d'une double liaison. Lorsqu'il y a une seule liaison en carbone, la rotation est possible. Par conséquent, cependant, nous dessions les atomes, leur arrangement sera le même. Mais quand il y a une double liaison en carbone, nous pouvons tirer deux dispositions d'atomes dans une molécule. Les isomères résultants sont connus sous le nom de cis, isomères trans ou isomères E-Z. Dans l'isomère cis, les mêmes types d'atomes sont du même côté de la molécule. Mais dans l'isomère trans, les mêmes types d'atomes se trouvent du côté opposé de la molécule. Par exemple, les structures cis et trans pour le 1,2-dichloroéthane sont les suivantes.
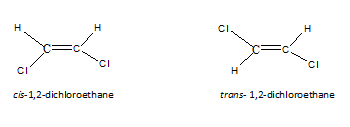
Pour qu'une molécule ait des isomères géométriques, il n'est pas seulement suffisant d'avoir une double liaison uniquement. Les deux atomes ou groupes attachés à une extrémité de la double liaison doivent être différents. Par exemple, la molécule suivante n'a pas d'isomères géométriques, les deux atomes à l'extrémité gauche sont des hydrogènes. À cause de cela, si nous le dessinons en CIS ou en trans, les deux molécules sont les mêmes.
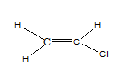
Mais peu importe si les quatre groupes ou atomes attachés sont différents. À cette occasion, nous pouvons les nommer comme e ou z.
Isomères structurels
Ceux-ci sont également appelés isomères constitutionnels. Les isomères constitutionnels sont des isomères, où la connectivité des atomes diffère en molécules. Le butane est l'alcane le plus simple pour montrer l'isomérisme constitutionnel. Butane a deux isomères constitutionnels, le butane lui-même et l'isobutène.
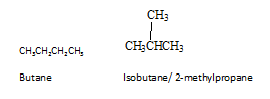
Étant donné que leurs connectivités sont différentes, deux molécules ont des propriétés physiques et chimiques différentes. Les isomères structurels peuvent être formés par des hydrocarbures où ils ont au moins quatre atomes de carbone. Il existe trois types d'isomères structurels comme isomères squelettiques, positionnels et fonctionnels. Dans l'isomérisme squelettique, comme indiqué dans l'exemple ci-dessus, le squelettique est réorganisé pour donner différents isomères. En position isomères, un groupe fonctionnel ou un autre groupe change la position. Dans les isomères de groupe fonctionnel, bien qu'ils aient la même formule, les molécules diffèrent de la difficulté de groupes fonctionnels.
| Quelle est la différence entre Isomères géométriques et isomères structurels? • Les isomères géométriques sont des stéréoisomères. Par conséquent, les connectivités sont également identiques par rapport aux isomères structurels, où les isomères diffèrent en raison des connectivités des atomes. Dans les isomères géométriques, ils diffèrent en raison de la disposition tridimensionnelle dans l'espace. • Souvent, pour une molécule, il y a deux isomères géométriques comme cis, trans ou e, z, mais pour une molécule, il peut y avoir un grand nombre d'isomères structurels. • L'isomérisme géométrique est essentiellement montré par la molécule avec des doubles liaisons en carbone-carbone. L'isomérisme structurel est montré par les alcanes, les alcènes, les alcynes et les composés aromatiques, ainsi que. |


