Différence entre la fusion et la vaporisation
Le différence clé entre la fusion et la vaporisation est que La fusion est la conversion d'un solide en liquide, tandis que la vaporisation est la conversion d'un liquide en vapeur.
Le terme fusion a des définitions différentes dans différents domaines, mais en chimie physique, nous l'utilisons pour décrire le processus de fusion. C'est-à-dire; La fusion est la conversion d'une phase solide en sa phase liquide. D'un autre côté, la conversion d'un liquide en son solide est connue sous le nom de congélation ou de solidification. Si la phase liquide d'une substance se transforme en phase gazeuse, alors nous l'appelons vaporisation. De plus, les énergies requises pour chaque conversion sont appelées «chaleur de fusion» et «chaleur de vaporisation».
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que la fusion
3. Qu'est-ce que la vaporisation
4. Comparaison côte à côte - fusion vs vaporisation sous forme tabulaire
5. Résumé
Qu'est-ce que la fusion?
La fusion est le processus de fusion où une phase solide se transforme en sa phase liquide. Par conséquent, ce terme fait référence à une transition de phase. Il se produit au point de fusion de la substance. L'énergie requise pour ce processus est appelée «chaleur de fusion». Pendant la fusion, l'entropie du système augmente parce que les particules qui étaient dans des endroits fixes dans le solide ont tendance à se déplacer dans la phase liquide (cela augmente le hasard, augmentant l'entropie).
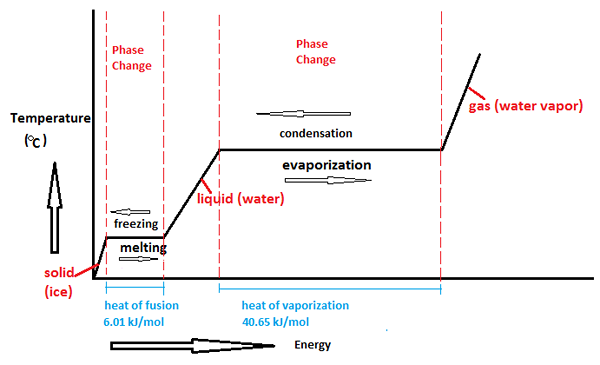
Figure 01: Changement de phase dans l'eau
La chaleur de fusion ou l'enthalpie de la fusion est le changement d'enthalpie. Fournir une énergie thermique à une substance pour passer sa phase de la phase solide à la phase liquide à une pression constante entraîne un changement d'enthalpie. L'enthalpie de la solidification est les phénomènes opposés, et il a la même valeur pour la quantité d'énergie requise. Essentiellement,
Chaleur de fusion = énergie thermique / masse
Qu'est-ce que la vaporisation?
La vaporisation est le processus de conversion d'une phase liquide en sa phase de vapeur. L'entropie du système augmente encore plus car les particules de la phase liquide obtiennent la capacité de se déplacer librement à la phase de vapeur. La chaleur de vaporisation ou l'enthalpie de vaporisation est le changement d'enthalpie lorsqu'un liquide se transforme en vapeur et c'est une fonction de pression.

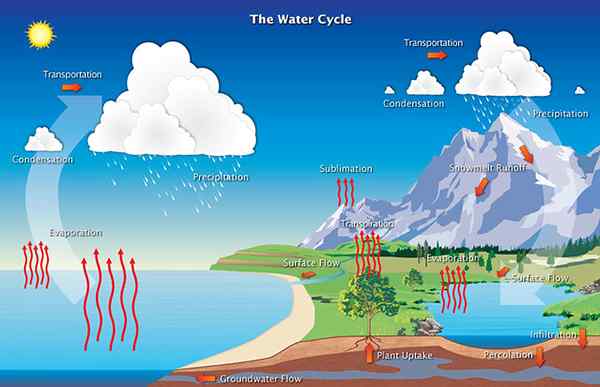
Figure 02: La vapeur d'eau se condense pour former des nuages pendant le cycle de l'eau
La vaporisation peut se produire de deux manières principales:
Évaporation
L'évaporation se produit à la surface du liquide. Il se produit à des températures sous le point d'ébullition du liquide à la même pression. De plus, il ne se produit que lorsque la pression partielle de vapeur est inférieure à la pression de vapeur d'équilibre.
Ébullition
L'ébullition est la formation de vapeur comme des bulles à l'intérieur du liquide. Contrairement à la vaporisation, les formes bouillantes vapeur sous la surface du liquide. Il se produit lorsque la pression de vapeur d'équilibre est égale ou supérieure à la pression environnementale.
Quelle est la différence entre la fusion et la vaporisation?
La fusion est un autre terme pour le processus de fusion. La vaporisation est le processus de formation de vapeur à partir d'un liquide, qui peut se produire de l'une des deux manières: l'évaporation et l'ébullition. La principale différence entre la fusion et la vaporisation est que la fusion est la conversion d'un solide en liquide, tandis que la vaporisation est la conversion d'un liquide en vapeur. Lorsque vous envisagez le changement d'enthalpie, nous appelons le changement d'enthalpie pendant le processus de fusion comme la chaleur de la fusion tandis que le changement d'enthalpie pendant la vaporisation est la chaleur de la vaporisation.

Résumé - Fusion vs vaporisation
La fusion et la vaporisation sont deux concepts chimiques importants qui décrivent deux changements de phases. La principale différence entre la fusion et la vaporisation est que la fusion est la conversion d'un solide en liquide, tandis que la vaporisation est la conversion d'un liquide en vapeur.
Référence:
1. Helmenstine, Anne Marie, «Définition de fusion (physique et chimie)."Thoughtco, mar. 9, 2019, disponible ici.
2. «Enthalpie de fusion.»Wikipedia, Wikimedia Foundation, 5 avril. 2019, disponible ici.
Image gracieuseté:
1. «Diagramme de changement de phase de l'eau» par Cawang - Propre travaux (CC By-SA 3.0) via Commons Wikimedia
2. «Le cycle de l'eau» par AIRS (CC par 2.0) via Flickr


