Différence entre l'éther et la cétone
Le différence clé entre l'éther et le cétone est que une éther contient deux groupes alkyles liés au même atome d'oxygène alors qu'une cétone contient un atome d'oxygène lié à un atome de carbone via une double liaison.
Les éthers et les cétones sont des composés organiques. Ces deux composés ont des atomes C, H et O dans leur structure moléculaire. Cependant, en déterminant leurs groupes fonctionnels, on peut différencier un éther d'une cétone.

CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que l'éther
3. Qu'est-ce que le cétone
4. Comparaison côte à côte - éther vs cétone sous forme tabulaire
5. Résumé
Qu'est-ce que l'éther?
Un éther est un composé organique ayant la formule chimique R-O-R. Ici, les groupes R peuvent être soit des groupes alkyle ou des groupes aryl. Si les groupes alkyl ou aryle sont identiques des deux côtés des atomes d'oxygène, alors c'est un éther symétrique. S'ils sont différents, alors c'est un éther asymétrique.
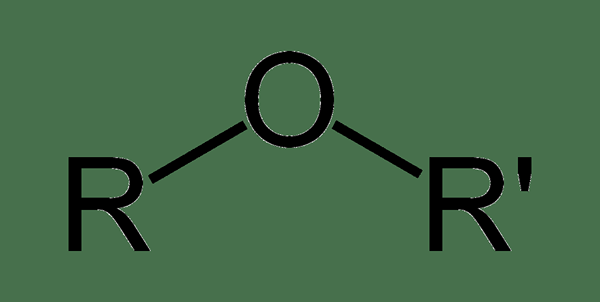
Figure 01: Structure générale d'un éther
La liaison chimique C-O-C qui a un angle de liaison de 110 ° décide des caractéristiques d'un éther. Par conséquent, il agit comme le groupe fonctionnel. L'hybridation de chaque carbone de ce groupe fonctionnel est SP3.
Étant donné que l'atome d'oxygène est plus électronégatif que l'atome de carbone, l'hydrogène alpha d'un éther est très acide par rapport à un hydrocarbure. Cela signifie que l'atome d'hydrogène lié à l'atome de carbone et est adjacent à la liaison C-O-C se libère facilement dans le provenant d'un proton. Cependant, il est moins acide que celui des composés carbonyle comme les cétones.
Les éthers ne peuvent pas former des liaisons hydrogène les unes avec les autres. Il en résulte des points d'ébullition inférieurs car il n'y a pas de forces d'interaction fortes entre ses molécules. Cependant, ils peuvent former des liaisons hydrogène avec des molécules d'eau car il y a des paires d'électrons solitaires sur l'atome d'oxygène. Et les éthers sont également légèrement polaires en raison de l'angle de liaison de la liaison C-O-C.
Qu'est-ce que le cétone?
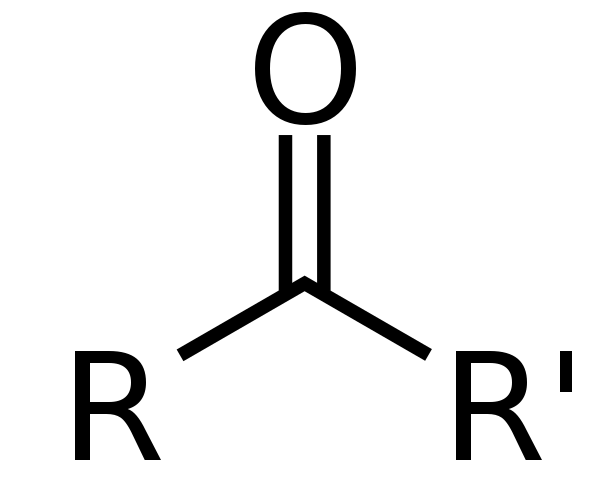
Une cétone est une molécule organique ayant la formule chimique R-C - (= o) R. Ici, la liaison entre l'atome d'oxygène et l'atome de carbone est une double liaison. Les groupes R indiquent les groupes alkyle ou aryle. L'atome de carbone central ainsi que l'atome d'oxygène à double liaison forme le groupe carbonyle. Cet atome de carbone est SP2 hybridé.

Figure 02: Structure générale d'une cétone
De plus, la liaison -c = o est très polaire. Par conséquent, les cétones sont des molécules polaires. L'atome d'oxygène attire les électrons de liaison entre cette liaison C et O en raison de sa haute électronégativité. Ensuite, l'atome de carbone obtient une charge positive partielle en raison du manque d'électrons. Et l'atome d'oxygène obtient une charge négative partielle. Par conséquent, cet atome d'oxygène provoque la formation de liaisons hydrogène entre les cétones et les molécules d'eau. Ainsi, les cétones sont miscibles avec de l'eau.
En plus de cela, l'atome de carbone du groupe carbonyle est sensible aux attaques de nucléophiles. Un nucléophile est un composé riche avec des électrons. Étant donné que l'atome de carbone du groupe carbonyle est partiellement positif chargé, le nucléophile peut interagir avec l'atome de carbone. Par conséquent, les cétones subissent des réactions d'addition nucléophile.
Quelle est la différence entre l'éther et le cétone?
Éther vs cétone | |
| Éther est un composé organique qui contient deux groupes alkyles liés au même atome d'oxygène. | Cétone est un composé organique qui contient un atome d'oxygène lié à un atome de carbone via une double liaison. |
| Formule chimique | |
| R-o-r | R-c - (= o) r |
| Groupe fonctionnel | |
| C-O-C. | -C (= o)-. |
| Acidité des carbones alpha | |
| Moins acide qu'une cétone mais est très acide que les hydrocarbures. | Très acide que les éthers. |
| Hybridation des carbones | |
| L'hybridation du carbone dans la liaison C-O-C est SP3. | L'hybridation du carbone dans le groupe carbonyle est SP2. |
Résumé - Ether vs Ketone
Les éthers et les cétones sont des molécules organiques. Ces deux molécules contiennent des atomes C, H et O. La différence entre l'éther et la cétone est qu'un éther contient deux groupes alkyles liés au même atome d'oxygène alors qu'une cétone contient un atome d'oxygène lié à un atome de carbone via une double liaison.
Référence:
1. "Éther.»Wikipedia, Wikimedia Foundation, 14 avril. 2018. Disponible ici
2. «Cétone.»Wikipedia, Wikimedia Foundation, 14 avril. 2018. Disponible ici
Image gracieuseté:
1.«Ether- (Général)» par aucun auteur lisible par machine fourni. (Domaine public) via Commons Wikimedia
2.`` Ketone-Groupe-2D-Skeletal '' (domaine public) via Commons Wikimedia


