Différence entre l'acide formique et l'acide acétique
La principale différence entre l'acide formique et l'acide acétique est que acide formique (ou acide méthanoïque, Hcooh) contient un groupe d'acide carboxylique attaché à un atome d'hydrogène tandis que l'acide acétique (ou acide éthanoïque, Ch3COOH) a un groupe méthyle attaché à un acide carboxylique.
L'acide formique et l'acide acétique sont des acides carboxyliques simples. Cependant, l'acide formique est l'acide carboxylique le plus simple tandis que l'acide acétique est le deuxième acide carboxylique le plus simple. Ces deux composés sont des composés acides.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que l'acide formique
3. Qu'est-ce que l'acide acétique
4. Similitudes entre l'acide formique et l'acide acétique
5. Comparaison côte à côte - acide formique vs acide acétique sous forme tabulaire
6. Résumé
Qu'est-ce que l'acide formique?
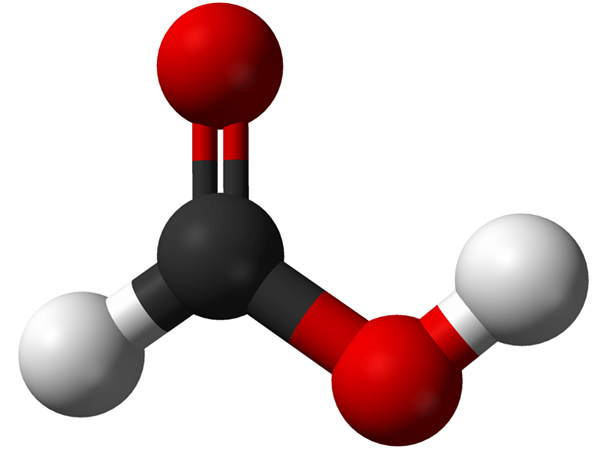
L'acide formique est l'acide carboxylique le plus simple dans lequel un groupe d'acide carboxylique est attaché à un atome d'hydrogène. La formule chimique en est Hcooh ou Ch2O2. Le nom IUPAC de ce composé est acide méthanoïque. Ce composé se produit naturellement dans certaines fourmis.
Certains faits chimiques sur l'acide formique sont les suivants:
- Formule chimique - ch2O2 / / Hcooh
- Masse molaire - 46.03 g / mol
- État physique - liquide à température ambiante
- Couleur - incolore
- Odeur - odeur piquante
- Point de fusion - 8.4 ° C
- Point d'ébullition - 100.8 ° C
- Solubilité dans l'eau - Miscible avec l'eau
La phase de vapeur de l'acide formique a des dimères en raison de la liaison hydrogène entre ses molécules. Deux molécules d'acide formique peuvent former deux liaisons hydrogène entre elles pour former un dimère. En raison de cette capacité à former des liaisons hydrogène avec des molécules d'eau, elle est miscible avec l'eau .

Figure 1: Structure chimique de l'acide formique
Production d'acide formique
La production d'acide formique utilise principalement du formiate de méthyle et du formamide. L'hydrolyse du formate méthyle produit de l'acide formique. Le formiate de méthyle est le résultat de la réaction entre le méthanol et le dioxyde de carbone en présence d'une base forte comme le méthoxyde de sodium. Parfois, le formate de méthyle se transforme d'abord en formamide (en réagissant au formate de méthyle avec de l'ammoniac), qui hydrolyse ensuite avec de l'acide sulfurique pour produire de l'acide formique.
Qu'est-ce que l'acide acétique?
L'acide acétique est le deuxième acide carboxylique le plus simple qui a un groupe méthyle attaché à un groupe d'acide carboxylique. Le nom IUPAC de ce composé est acide éthanoique. La formule chimique de l'acide acétique est Ch3COOH. Certains faits chimiques sur l'acide acétique sont les suivants:
- Formule chimique - ch3COOH
- Masse molaire - 60.05 g / mol
- État physique - liquide à température ambiante
- Couleur - incolore
- Odeur - odeur de vinaigre
- Point de fusion - 16.6 ° C
- Point d'ébullition - 118.1 ° C
- Solubilité dans l'eau - Miscible avec l'eau
L'acide acétique est un constituant majeur du vinaigre. Il a un goût aigre caractéristique et une odeur piquante. L'atome d'hydrogène du groupe d'acide carboxylique d'acide acétique peut se séparer de la molécule via l'ionisation de la molécule. Par conséquent, c'est une molécule acide. C'est aussi un composé monoprotique faible. L'acide acétique solide a les molécules disposées dans une structure en forme de chaîne en raison des liaisons hydrogène présentes entre les molécules. Mais a des dimères dans sa phase de vapeur.
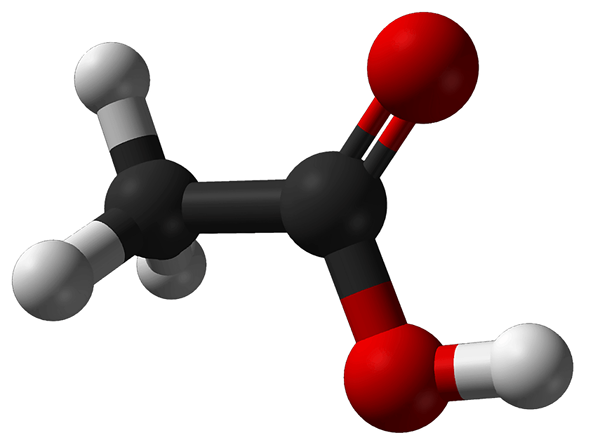
Figure 2: Structure chimique de l'acide acétique
Production d'acide acétique
Il existe deux voies pour produire de l'acide acétique: la production synthétique et la fermentation bactérienne. Le processus utilisé dans la synthèse est principalement la carbonylation du méthanol. Cette méthode implique la réaction entre le méthanol et le monoxyde de carbone.
Quelles sont les similitudes entre l'acide formique et l'acide acétique?
- L'acide formique et l'acide acétique sont des acides carboxyliques
- Les deux sont des liquides incolores à température ambiante
- Les deux acides ont une forte odeur
- Ils sont tous deux capables de former des dimères
- Avec des molécules d'eau, les deux peuvent former des liaisons hydrogène
- De plus, les deux acides sont miscibles avec de l'eau
Quelle est la différence entre l'acide formique et l'acide acétique?
Acide formique vs acide acétique | |
| Acide formique est l'acide carboxylique le plus simple qui a un groupe d'acide carboxylique attaché à un atome d'hydrogène. | Acide acétique est le deuxième acide carboxylique le plus simple, qui a un groupe méthyle attaché à un groupe d'acide carboxylique. |
| Nom IUPAC | |
| Acide méthanoïque | Acide éthanoique |
| Formule chimique | |
| Ch3COOH. | Hcooh. |
| Chimique Structure | |
| Contient un atome d'hydrogène lié au groupe carboxylique. | Contient un groupe méthyle lié au groupe carboxylique. |
| Masse molaire | |
| 46.03 g / mol. | 60.05 g / mol. |
| Point d'ébullition | |
| 100.8 ° C. | 118.1 ° C. |
| Point de fusion | |
| 8.4 ° C. | 16.6 ° C. |
Résumé - acide formique vs acide acétique
L'acide formique et l'acide acétique sont les composés d'acide carboxylique les plus simples. La principale différence entre l'acide formique et l'acide acétique est que l'acide formique contient un groupe d'acide carboxylique attaché à un atome d'hydrogène alors que l'acide acétique a un groupe méthyle attaché à un acide carboxylique.
Référence:
1. "Acide formique.»Wikipedia, Wikimedia Foundation, 14 avril. 2018, disponible ici.
2. "Acide formique.»Information du Centre national pour la biotechnologie. Base de données de composés PubChem, u.S. Bibliothèque nationale de médecine, disponible ici.
3. "Acide acétique.»Wikipedia, Wikimedia Foundation, 24 avril. 2018, disponible ici.


