Différence entre l'élément et la molécule
Le différence clé entre l'élément et la molécule est que Les éléments sont des substances pures qui se composent uniquement d'un seul type d'atome et ne peuvent pas être décomposées par des moyens chimiques tandis que les molécules peuvent contenir deux ou plusieurs atomes du même élément ou des éléments différents.
Les atomes sont les petites unités qui se rassemblent pour former toutes les substances chimiques existantes. Les atomes peuvent se joindre à d'autres atomes de diverses manières et former des milliers de molécules et d'autres composés. Selon leurs capacités de don ou de retrait d'électrons, ils peuvent former des obligations covalentes ou des obligations ioniques. Parfois, il y a des attractions très faibles entre les atomes. Les molécules et les éléments sont constitués d'atomes.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce qu'un élément
3. Qu'est-ce qu'une molécule
4. Comparaison côte à côte - élément vs molécule sous forme tabulaire
5. Résumé
Qu'est-ce qu'un élément?
Nous connaissons le mot «élément», car nous les apprenons dans le tableau périodique. Il y a environ 118 éléments dans le tableau périodique, organisé en fonction de leur numéro atomique. Un élément est une substance chimique qui ne se compose qu'un seul type d'atomes, donc ils sont purs. Le plus petit élément est l'hydrogène et l'argent, l'or et le platine sont quelques-uns des éléments précieux communément connus. Chaque élément a une masse atomique, un numéro atomique, un symbole, une configuration électronique, etc. Bien que la plupart des éléments se produisent naturellement, il existe des éléments synthétiques comme Californium, Americium, Einsteinium et Mendelevium.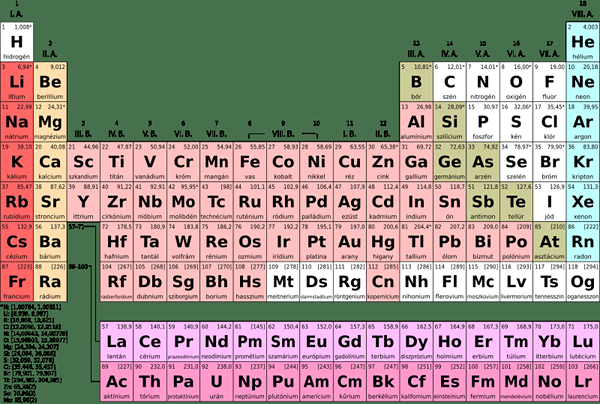
Tous les éléments peuvent être largement classés en trois catégories: métal, métalloïdes et non-métaux. De plus, ils sont classés en groupes et périodes en fonction de caractéristiques plus spécifiques. Les éléments du même groupe ou des mêmes périodes partagent certaines caractéristiques communes, et certaines propriétés peuvent changer séquentiellement lorsque vous passez par un groupe ou une période. Les éléments peuvent être soumis à des changements chimiques pour former divers composés; Cependant, les éléments ne peuvent pas être davantage décomposés par de simples méthodes chimiques. Il y a des atomes du même élément avec un nombre différent de neutrons; Ceux-ci sont appelés isotopes d'un élément.
Qu'est-ce qu'une molécule?
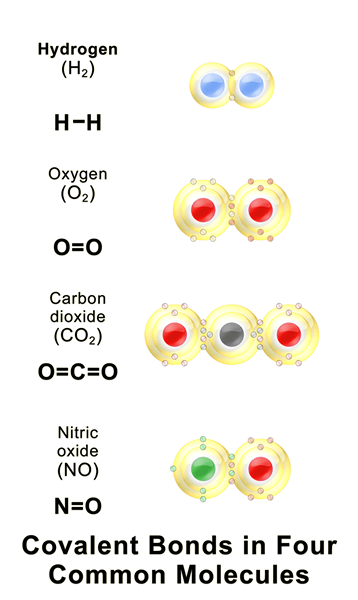
Les molécules sont composées en liant chimiquement deux atomes ou plus du même élément (e.g.: O2, N2) ou différents éléments (h2O, NH3). Les molécules n'ont pas de charge et les atomes sont liés par les liaisons covalentes. Les molécules peuvent être très grandes (hémoglobine) ou très petites (H2), selon le nombre d'atomes connectés. Le type et le nombre d'atomes dans une molécule sont représentés par la formule moléculaire.

Le rapport entier le plus simple d'atomes présents dans une molécule est donné par la formule empirique. Par exemple, C6H12O6 est la formule moléculaire du glucose et ch2O est la formule empirique. La masse moléculaire est la masse calculée compte tenu du nombre total d'atomes donnés dans la formule moléculaire. Chaque molécule a sa propre géométrie. Les atomes d'une molécule sont disposés de la manière la plus stable avec un angle de liaison et des longueurs de liaison spécifiques pour minimiser les répulsions et les forces de contrainte.
Quelle est la différence entre l'élément et la molécule?
Les éléments sont des substances pures qui se composent uniquement d'un seul type d'atome et ne peuvent pas être décomposées par des moyens chimiques tandis que les molécules peuvent contenir deux ou plusieurs atomes du même élément ou des éléments différents. Ainsi, la principale différence entre l'élément et la molécule est que les éléments ne se composent que d'un seul type d'atomes tandis que les molécules peuvent contenir deux ou plusieurs atomes du même élément ou des éléments différents. Certains exemples d'éléments incluent l'hydrogène, l'azote, l'oxygène, le sodium, le cuivre et le zinc tandis que certains exemples de molécules incluent le dioxyde de carbone, l'eau et l'ozone. De plus, les propriétés d'un élément changent souvent complètement lorsqu'ils font partie d'une molécule.
Ci-dessous l'info-graphique montre les différences entre l'élément et la molécule sous forme tabulaire.
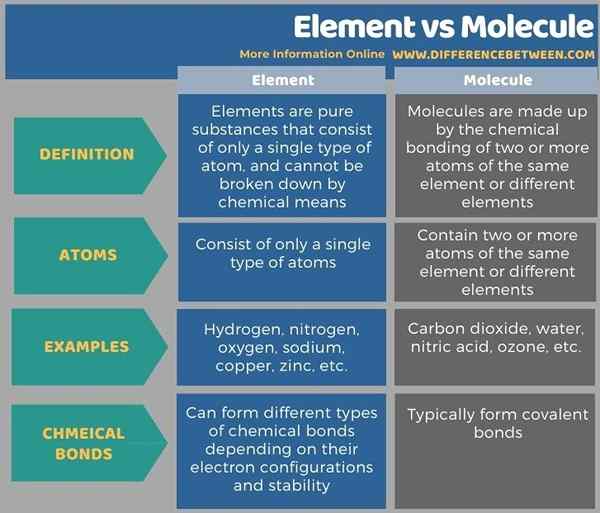
Résumé - élément vs molécule
La principale différence entre l'élément et la molécule est que les éléments ne consistent en un seul type d'atomes tandis que les molécules peuvent contenir deux ou plusieurs atomes du même élément ou des éléments différents. Les propriétés d'un élément changent souvent complètement lorsqu'ils font partie d'une molécule.
Image gracieuseté:
1. «Tableau périodique Simple Hu» par László Németh - Propre travaux, CC0) via Commons Wikimedia
2. «Obligations covalentes» par Bruceblaus - Propre travaux (CC BY-SA 4.0) via Commons Wikimedia


