Différence entre la chimisorption et la physisorption
Le différence clé entre la chimisorption et la physisorption La chimisorption est un type de adsorption dans laquelle la substance adsorbée est tenue par des liaisons chimiques tandis que la physisorption est un type d'adsorption dans lequel la substance adsorbée est détenue par les forces intermoléculaires.
La chimisorption et la physisorption sont généralement des concepts chimiques importants que nous pouvons utiliser pour décrire le mécanisme d'adsorption d'une substance à une surface. La chimisorption est l'adsorption par des moyens chimiques tandis que la physisorption est l'adsorption par des moyens physiques.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que la chimisorption
3. Qu'est-ce que la physisorption
4. Comparaison côte à côte - chimisorption vs physisorption sous forme tabulaire
5. Résumé
Qu'est-ce que la chimisorption?
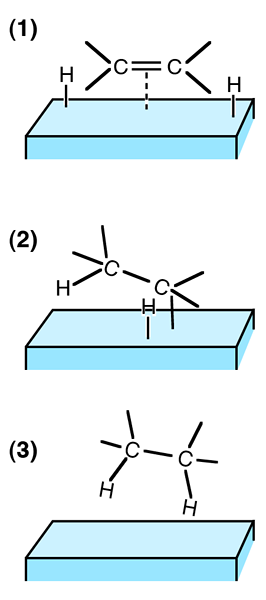
La chimisorption est le processus dans lequel l'adsorption d'une substance à une surface est entraînée par des moyens chimiques. Ici, l'adsorbat se fixe avec la surface via des liaisons chimiques. Par conséquent, ce mécanisme implique une réaction chimique entre l'adsorbat et la surface. Ici, les liaisons chimiques peuvent se décomposer et se former en même temps. De plus, les espèces chimiques qui accumulent l'adsorbat et la surface subissent des changements en raison de la rupture et de la formation de cette liaison.

Figure 01: Trois étapes pour la chimisorption
Un exemple courant est la corrosion, qui est un phénomène macroscopique que nous pouvons observer de l'œil nu. De plus, les types de liaisons qui peuvent se former entre l'adsorbat et la surface comprennent les liaisons covalentes, les liaisons ioniques et les liaisons hydrogène.
Qu'est-ce que la physisorption?
La physisorption est le processus dans lequel l'adsorption d'une substance à une surface est motivée par des moyens physiques. Cela signifie; Il n'y a pas de formations de liaisons chimiques, et ce processus implique des interactions intermoléculaires telles que les forces van der Waal. L'adsorbat et la surface existent intacts. Par conséquent, il n'y a aucune implication de la structure électronique des atomes ou des molécules.
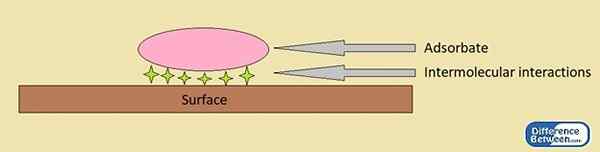
Un exemple courant est les forces de van der Waals entre les surfaces et les poils des geckos, qui les aident à gravir les surfaces verticales.
Quelle est la différence entre la chimisorption et la physisorption?
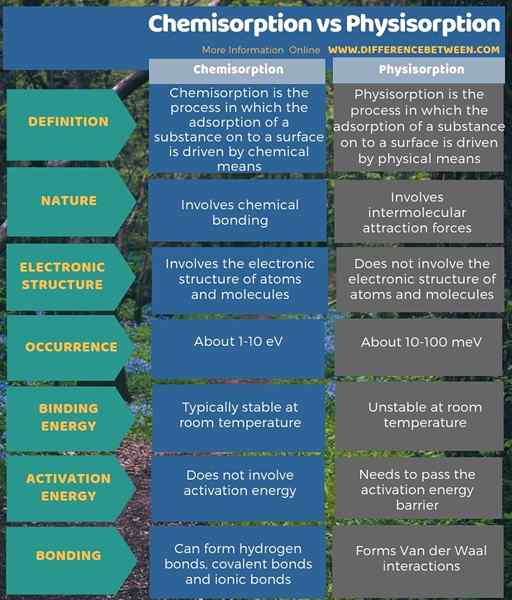
La principale différence entre la chimisorption et la physisorption est que dans la chimisorption, les liaisons chimiques détiennent la substance adsorbée alors que, en physisorption, les forces intermoléculaires tiennent la substance adsorbée. De plus, la chimisorption peut former des liaisons hydrogène, des liaisons covalentes et des liaisons ioniques, mais la physisorption ne forme que les interactions van der Waal. Nous pouvons donc considérer cela également comme une différence entre la chimisorption et la physisorption. L'énergie de liaison pour la chimisorption varie de 1 à 10 eV alors qu'en physisorption, elle est d'environ 10 à 100 MEV.
L'infographie ci-dessous montre plus de comparaisons concernant la différence entre la chimisorption et la physisorption.
Résumé - Chemisorption vs physisorption
La principale différence entre la chimisorption et la physisorption est que la chimisorption est un type d'adsorption dans laquelle les liaisons chimiques maintiennent la substance adsorbée, tandis que la physisorption est un type d'adsorption dans lequel les forces intermoléculaires maintiennent la substance adsorbée.
Référence:
1. Murr, L.e. «Systèmes d'imagerie et caractérisation des matériaux.”Caractérisation des matériaux, Vol. 60, non. 5, 2009, pp. 397-414., doi: 10.1016 / J.Matchar.2008.dix.013.
Image gracieuseté:
1. «Hydrogénation sur Catalyst» de Michael Schmid - Drawing Created Mysel (CC par 1.0) via Commons Wikimedia


