Différence entre la RMN en carbone et la RMN de protons
Le différence clé entre le RMN en carbone et la RMN de proton est que RMN en carbone détermine le type et le nombre d'atomes de carbone dans une molécule organique tandis que le proton RMN détermine le type et le nombre d'atomes d'hydrogène dans une molécule organique.
La RMN est un terme chimique que nous utilisons en chimie analytique pour indiquer une résonance magnétique nucléaire. Ce terme relève de la spectroscopie subtopique en chimie analytique. Cette technique est très importante pour déterminer le type et le nombre d'atomes particuliers dans un échantillon donné. La technique RMN est principalement utilisée avec des composés organiques.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que RMN en carbone
3. Qu'est-ce que Proton RMN
4. Comparaison côte à côte - RMN en carbone vs RMN proton sous forme tabulaire
5. Résumé
Qu'est-ce que RMN en carbone?
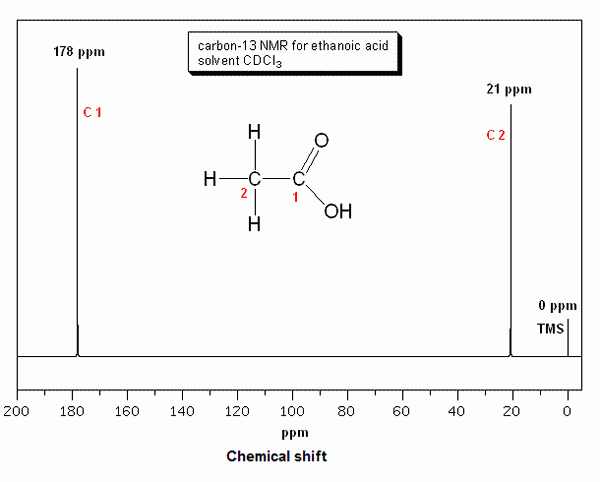
RMN en carbone est important pour déterminer le type et le nombre d'atomes de carbone dans une molécule. Dans cette technique, nous devons d'abord dissoudre l'échantillon (molécule / composé) dans un solvant approprié, puis il peut être placé à l'intérieur du spectrophotomètre RMN. Ensuite, le spectrophotomètre nous donne une image ou un spectre montrant certains pics pour les atomes de carbone présents dans l'échantillon. Contrairement à la RMN de protons, les liquides contenant des protons peuvent être utilisés comme solvant car cette méthode ne détecte que les atomes de carbone, pas les protons.

Figure 01: RMN en carbone pour l'acide éthanoïque
RMN en carbone est utile dans l'étude des changements de spin dans les atomes de carbone. La plage de décalage chimique pour la RMN 13C est de 0 à 240 ppm. Pour obtenir le spectre RMN, nous pouvons utiliser la méthode de transformation de Fourier. Il s'agit d'un processus rapide où un pic de solvant peut être observé.
Qu'est-ce que Proton RMN?
Le RMN proton est une méthode spectroscopique qui est importante pour déterminer les types et le nombre d'atomes d'hydrogène présents dans une molécule. Par conséquent, il est également abrégé comme RMN 1H. Cette technique analytique particulière comprend des étapes de dissolution de l'échantillon (molécule / composé) dans un solvant approprié et plaçant l'échantillon avec un solvant à l'intérieur du spectrophotomètre RMN. Ici, le spectrophotomètre nous donne un spectre contenant certains pics pour les protons présents dans l'échantillon et dans le solvant également.
Cependant, la détermination des protons présents dans l'échantillon est difficile en raison de l'interférence provenant des protons dans les molécules de solvant. Par conséquent, un solvant qui ne contient aucun protons est utile dans cette méthode. Par exemple, les solvants contenant du deutérium au lieu de protons tels que l'eau deutérée (D2O), acétone deutérée ((CD3)2CO), CCL4, etc. peut être utilisé.
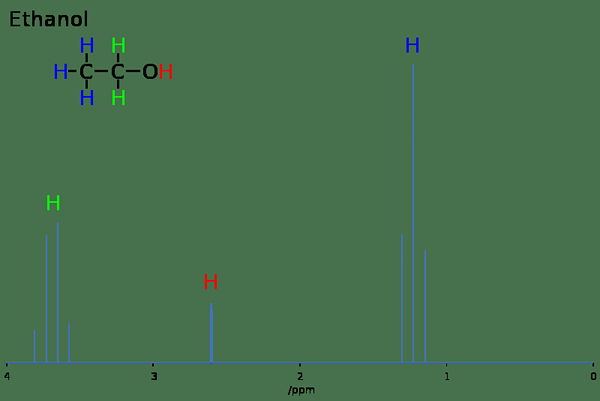
Figure 02: RMN Proton pour l'éthanol
La plage de décalage chimique de 1H RMN est de 0 à 14 ppm. Dans l'obtention des spectres RMN pour la RMN 1H, la méthode d'onde continue est utilisée. Cependant, c'est un processus lent. Étant donné que le solvant ne contient aucun protons, les spectres RMN 1H n'ont pas de pics pour le solvant.
Quelle est la différence entre le RMN en carbone et la RMN de proton?
La principale différence entre le RMN en carbone et la RMN de protons est que la RMN en carbone détermine le type et le nombre d'atomes de carbone dans une molécule organique tandis que le proton RMN détermine le type et le nombre d'atomes d'hydrogène dans une molécule organique.
Le tableau suivant résume la différence entre la RMN en carbone et la RMN de proton.
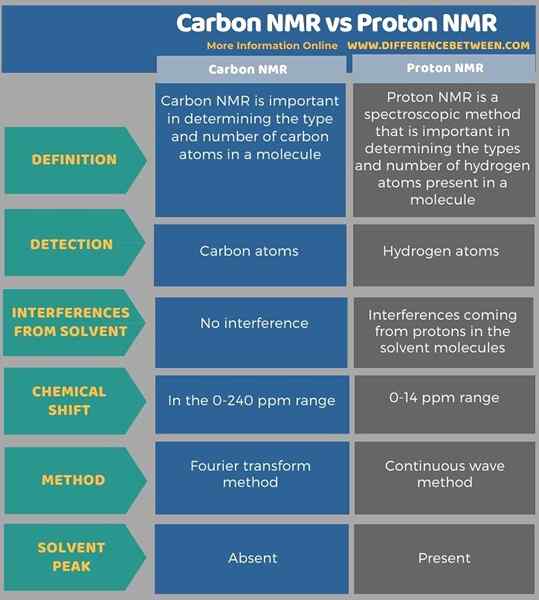
Résumé - RMN en carbone vs proton RMN
RMN en carbone et RMN de protons sont deux principaux types de résonance magnétique nucléaire. La principale différence entre le RMN en carbone et la RMN de protons est que la RMN en carbone détermine le type et le nombre d'atomes de carbone dans une molécule organique tandis que le proton RMN détermine le type et le nombre d'atomes d'hydrogène dans une molécule organique.
Référence:
1. «Progrès dans la spectroscopie de résonance magnétique nucléaire.»Progrès dans la spectroscopie de résonance magnétique nucléaire, Vol. 40, non. 2, 2002, doi: 10.1016 / S0079-6565 (01) 00046-2.
2. Groves, Patrick, et al. «Investigations RMN sur les interactions de lectine-carbo-hydrate.»Lectines, 2007, pp. 51-73., doi: 10.1016 / B978-044453077-6 / 50004-1.
Image gracieuseté:
1. «Acid éthanoïque RMN 13C» par Chris Evans - D: \ My Webs \ index.HTM, CC0) via Commons Wikimedia
2. «Couplage de l'éthanol RMN 1H montré» par Andel - Propre travaux, données de SDBSWEB: (National Institute of Advanced Industrial Science and Technology, consulté 2019-08-03) (CC0) via Commons Wikimedia


