Différence entre le chlorure de calcium et le chlorure de sodium

Le différence clé entre le chlorure de calcium et le chlorure de sodium est que La molécule de chlorure de calcium a deux atomes de chlore tandis que la molécule de chlorure de sodium a un atome de chlore. De plus, le chlorure de calcium est une poudre de couleur blanche avec des propriétés hygroscopiques tandis que le chlorure de sodium est un cristal incolore et le chlorure de sodium pur n'est pas hygroscopique.
Le chlorure de calcium et le chlorure de sodium sont des composés alcalins inorganiques. La formule chimique du chlorure de calcium est Cacl2. La formule chimique du chlorure de sodium est NaCl.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que le chlorure de calcium
3. Qu'est-ce que le chlorure de sodium
4. Comparaison côte à côte - chlorure de calcium vs chlorure de sodium sous forme tabulaire
5. Résumé
Qu'est-ce que le chlorure de calcium?
Le chlorure de calcium est cacl2 qui a une masse molaire de 110.98 g / mol. Il apparaît comme un composé solide blanc qui est hygroscopique. Cela signifie qu'il peut absorber la vapeur d'eau de l'air lorsqu'il est exposé à l'atmosphère. Ce composé est inodore. Il relève de la catégorie des sels; Nous l'appelons un sel de calcium.
Ce composé est très soluble dans l'eau. En raison de sa nature hygroscopique, ce composé se produit couramment comme un complexe hydraté. La formule de ce complexe hydraté est cacl2.(H2O) x dans lequel x = 0, 1, 2, 4 et 6. Ces composés hydratés sont utiles dans les processus de désactivation et le contrôle de la poussière. La forme anhydre (dans laquelle x = 0) est importante comme un descendant en raison de la nature hygroscopique.

Figure 01: Aspect du chlorure de calcium
Le point de fusion du chlorure de calcium anhydre est d'environ 772-775◦C tandis que le point d'ébullition est de 1935◦C. Lorsque nous dissolvons ce composé dans l'eau, il forme un complexe hexaaqua; [CA (H2O)6]]2+. Cela convertit les ions de calcium et de chlorure dans la solution en un état «libre». Par conséquent, si nous ajoutons une source de phosphate à cette solution aqueuse, elle donne un précipité solide au phosphate de calcium.
Qu'est-ce que le chlorure de sodium?
Le chlorure de sodium est du NaCl qui a une masse molaire de 58.44 g / mol. À température ambiante et à la pression, ce composé apparaît sous forme de cristaux solides et incolores. C'est sans odeur. Dans sa forme pure, ce composé ne peut pas absorber la vapeur d'eau. Par conséquent, ce n'est pas hygroscopique.
Le chlorure de sodium est également un sel; Nous l'appelons un sel de sodium. Il y a un atome de chorine pour chaque atomes de sodium de la molécule. Ce sel est responsable de la salinité de l'eau de mer. Le point de fusion est 801◦C tandis que le point d'ébullition est 1413◦C. Dans les cristaux de chlorure de sodium, chaque cation sodium est entouré de six ions chlorure et vice versa. Par conséquent, nous appelons le système cristallin comme un système cubique centré sur le visage.

Figure 02: cristaux de sel
Ce composé se dissout dans des composés polaires élevés tels que l'eau. Là, les molécules d'eau entourent chaque cation et anion. Chaque ion a, la plupart du temps, six molécules d'eau autour d'eux. Cependant, le pH d'un chlorure de sodium aqueux se situe autour de PH7 en raison de la basité faible de l'ion chlorure. Nous disons qu'il n'y a aucun effet de chlorure de sodium sur le pH d'une solution.
Quelle est la différence entre le chlorure de calcium et le chlorure de sodium?
Le chlorure de calcium est un sel de calcium ayant la formule chimique CACL2 tandis que le chlorure de sodium est un sel de sodium ayant la formule chimique NaCl. Ce sont des composés de sel. De plus, chaque molécule de chlorure de calcium a deux atomes de chlore par ion calcium tandis que chaque molécule de chlorure de sodium a un atome de chlore par ion sodium. De plus, leurs masses molaires sont également différentes les unes des autres; La masse molaire du chlorure de calcium est 110.98 g / mol, et la masse molaire de chlorure de sodium est 58.44 g / mol.
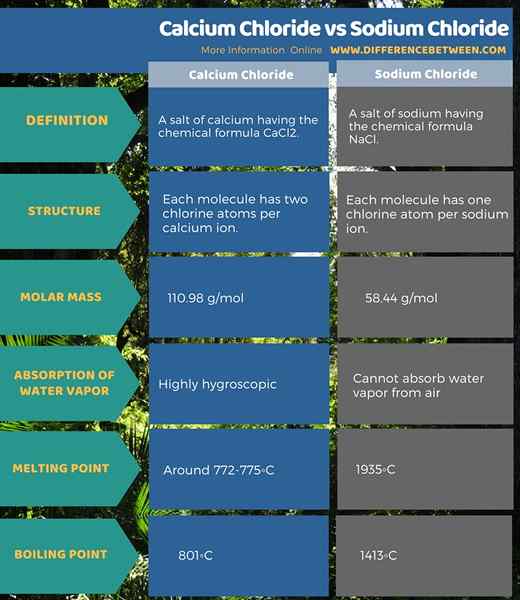
Résumé - chlorure de calcium vs chlorure de sodium
Le chlorure de calcium et le chlorure de sodium sont des composés de sel qui sont alcalins. Ces deux composés contiennent des ions de chlorure dans leur structure, mais dans différents rapports. La principale différence entre le chlorure de calcium et le chlorure de sodium est qu'une molécule de chlorure de calcium a deux atomes de chlore alors qu'une molécule de chlorure de sodium a un atome de chlore.
Référence:
1. «Dichlorure de calcium.»Information du Centre national pour la biotechnologie. Base de données de composés PubChem. U.S. Bibliothèque nationale de médecine. Disponible ici
2. "Chlorure de sodium.»Information du Centre national pour la biotechnologie. Base de données de composés PubChem, u.S. Bibliothèque nationale de médecine. Disponible ici
Image gracieuseté:
1.'Chlorure de calcium cacl2'by Aucun auteur lisible par machine fourni. (CC BY-SA 3.0) via Commons Wikimedia
2.'Halit-kristalle'by w.J.Pilsak chez allemand Wikipedia (CC BY-SA 3.0) via Commons Wikimedia


