Différence entre le nitrite alkyle et l'alcane nitro
Le différence clé Entre le nitrite alkyle et l'alcane nitro est que Dans le nitrite alkyle, le groupe alkyle est lié à un atome d'oxygène, tandis que dans le nitro alcane, le groupe alkyle se lie à l'atome d'azote.
Bien que les noms alkyl nitrite et nitro alcane semblent similaires, ce sont deux types distincts de composés organiques. Ces deux composés ont un groupe nitro et un groupe alkyle en combinaison, mais ils diffèrent les uns des autres en fonction de la position où les deux groupes s'attachent les uns aux autres; Dans le nitrite alkyle, le groupe alkyle s'attache à travers l'atome d'oxygène, tandis qu'à Nitro Alcane, le groupe alkyle se fixe à travers l'atome d'azote.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que le nitrite alkyle
3. Qu'est-ce que Nitro Alcane
4. Comparaison côte à côte - Nitrite alkyle vs alcane nitro sous forme tabulaire
5. Résumé
Qu'est-ce que le nitrite alkyle?
Les nitrites alkyl sont un groupe de composés organiques ayant la structure r-ono. Ce sont des esters alkyles d'acide nitreux. Les petits composés de nitrite alkyle sont des composés volatils et ils existent à l'état liquide. Mais le nitrite de méthyle et l'éthyl nitrite (les plus petits nitrites alkyle) sont des gaz à température ambiante.
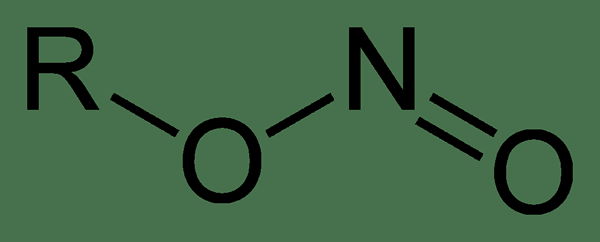
Figure 01: Structure chimique du nitrite alkyle
En dehors de cela, les nitrites alkyl ont une odeur fruitée. Lorsque vous envisagez la préparation, nous pouvons les produire à partir d'alcools et de nitrite de sodium. Ici, nous devons utiliser un milieu acide, la plupart de l'acide sulfurique est utilisé. Cependant, après la préparation, le composé a tendance à se décomposer lentement dans des oxydes d'azote et d'eau avec l'alcool. La principale application du nitrite alkyle est comme médicament; pour le soulagement de l'angine de poitrine et des maladies cardiaques.
Qu'est-ce que Nitro Alcane?
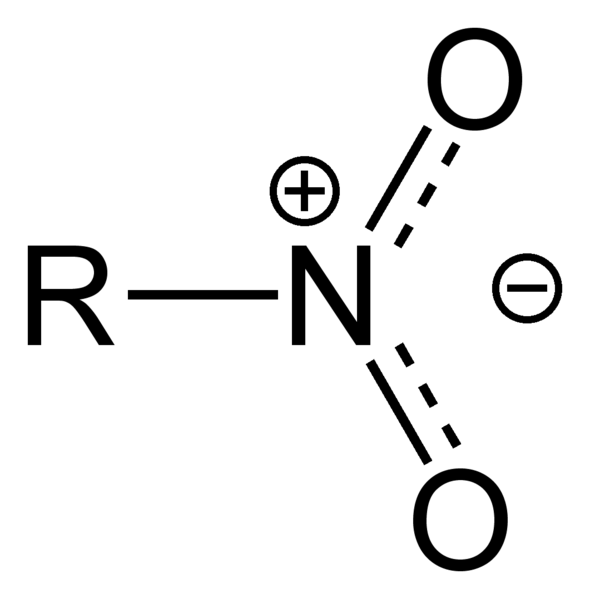
Les alcanes nitro sont un groupe de composés organiques ayant la structure r-no2. Dans ce composé, le groupe alkyle se lie à l'atome d'azote du groupe nitro. Puisqu'un groupe nitro (-NO2) est fortement à la détention d'électrons, les liaisons C-H adjacentes sont acides.

Figure 02: Structure de Nitro Alcane
En règle générale, nous pouvons produire des alcanes nitro via une nitration radicale libre d'alcanes. Lorsque vous envisagez les applications, l'alcane nitro est importante en tant que précurseurs efficaces pour la production d'alcanes et d'alcènes très substitués. De plus, ce composé est important pour la production de molécules complexes, y compris les acides carboxyliques, les aldéhydes, les cétones, les structures hétérocycliques complexes, etc.
Quelle est la différence entre le nitrite alkyle et l'alcane nitro?
Bien que les noms alkyl nitrite et nitro alcane semblent similaires, ce sont deux types distincts de composés organiques. La principale différence entre le nitrite alkyle et l'alcane nitro est que, dans le nitrite alkyle, le groupe alkyle est lié à un atome d'oxygène, tandis que dans le nitro alcane, le groupe alkyle se lie à l'atome d'azote. Les nitrites alkyle ont principalement une odeur fruitée mais Nitro Alcane a une odeur distinctive. De plus, les petits nitrites alkyle existent en phase gazeuse tandis que d'autres nitrites alkyle sont en phase liquide; Cependant, les alcanes nitro existent sous forme de liquides incolores qui se transforment en une légère couleur jaune lorsqu'ils sont stockés pendant un certain temps.
Lorsque vous envisagez les applications, les nitrites alkyl sont utiles comme médicament pour les maladies cardiaques et comme réactifs chimiques pour la production de différents composés organiques. Les alcanes nitro sont importants pour la production d'alcanes et d'alcènes hautement substitués, des molécules complexes, notamment des acides carboxyliques, des aldéhydes, des cétones, des structures hétérocycliques complexes, etc.
Ci-dessous, l'info-graphique résume la différence entre le nitrite alkyle et l'alcane nitro.
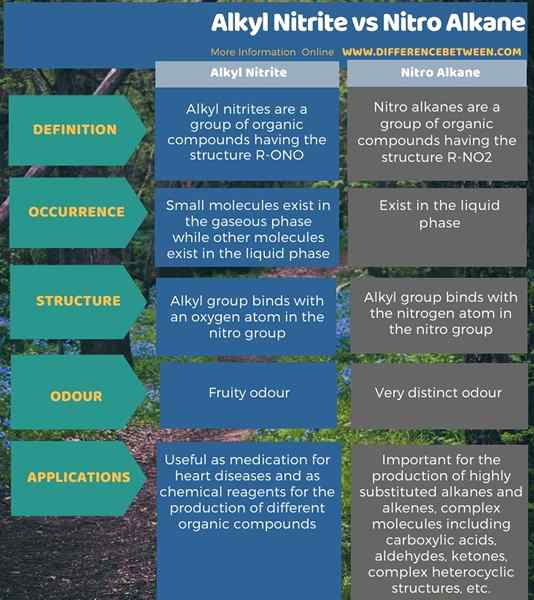
Résumé - Nitrite alkyle vs alcane nitro
Bien que les noms alkyl nitrite et nitro alcane semblent similaires, ce sont deux types distincts de composés organiques. La principale différence entre le nitrite alkyle et l'alcane nitro est que dans le nitrite alkyle, le groupe alkyle est lié à un atome d'oxygène tandis que dans l'alcane nitro, le groupe alkyle se lie à l'atome d'azote.
Référence:
1. «Nitrites alkyle.»Wikipedia, Wikimedia Foundation, 11 septembre. 2019, disponible ici.
2. «Composé nitro.»Wikipedia, Wikimedia Foundation, 20 octobre. 2019, disponible ici.
3. Moldoveanu, serban c. «Pyrolyse d'autres composés contenant de l'azote.”Pyrolyse of Organic Molecules, 2019, pp. 349-390., doi: 10.1016 / B978-0-444-64000-0.00009-3.
Image gracieuseté:
1. «Nitrite-Eester-2d» (domaine public) via Commons Wikimedia
2. «Nitro-Groupe-2d» (domaine public) via les communes Wikimedia


