Quelle est la différence entre le potentiel d'électrode standard et le potentiel de réduction standard
Le Différence clé entre le potentiel d'électrode standard et le potentiel de réduction standard est que le potentiel d'électrode standard est la tendance d'une électrode à perdre ou à gagner des électrons, tandis que le potentiel de réduction standard est la tendance d'une espèce chimique à être réduite.
Les termes potentiel d'électrode standard et potentiel de réduction standard sont généralement utilisés de manière interchangeable car il est difficile de mesurer le potentiel précis d'une électrode seul plutôt que de mesurer le potentiel global. Cependant, le potentiel d'électrode standard peut se référer à l'oxydation ou à la réduction, tandis que le potentiel de réduction standard se réfère principalement à la réduction de la demi-réaction.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que le potentiel d'électrode standard
3. Qu'est-ce que le potentiel de réduction standard
4. Potentiel d'électrode standard vs potentiel de réduction standard de la forme tabulaire
5. Résumé - Potentiel d'électrode standard vs potentiel de réduction standard
Qu'est-ce que le potentiel d'électrode standard?
Le potentiel d'électrode standard peut être décrit comme la mesure du potentiel d'équilibre. En d'autres termes, c'est la différence de potentiel entre l'électrode et l'électrolyte nommé comme le potentiel de l'électrode. Il mesure la puissance réductrice de tout élément ou composé. Selon le livre d'or IUPAC, le potentiel d'électrode standard est la valeur de l'EMF standard (force électromotive) d'une cellule où l'hydrogène moléculaire sous pression standard est oxydé en protons solvatés à l'électrode gauche.
Habituellement, la base d'une cellule électrochimique est une réaction redox qui se compose de deux demi-réactions. Ce sont l'oxydation à l'anode et la réduction de la cathode. Par conséquent, l'électricité se forme en raison de la différence de potentiel électrique entre les potentiels individuels des deux électrodes métalliques en ce qui concerne l'électrolyte.

Nous pouvons simplement mesurer le potentiel global d'une cellule. Mais la mesure précise du potentiel d'électrode isolément est très difficile. Ce phénomène varie avec la température, la concentration et la pression. Le potentiel d'oxydation d'une demi-réaction peut être décrit comme le négatif du potentiel de réduction d'une réaction redox. Par conséquent, ce potentiel est suffisant pour calculer l'un des potentiels. Cela conduit à l'utilisation des termes potentiel d'électrode standard et au potentiel de réduction standard à utiliser de manière interchangeable.
Qu'est-ce que le potentiel de réduction standard?
Le potentiel de réduction standard peut être décrit comme le potentiel de volts généré par la réduction de la réaction de réaction des réactions redox en comparaison avec l'électrode hydrogène standard à 25 degrés Celsius, 1 pression d'atomes et 1M concentration. En d'autres termes, nous pouvons définir ce terme par rapport à une électrode d'hydrogène standard. Cette électrode hydrogène est attribuée comme le 0.00 V Norme potentielle. La dénotation du potentiel de réduction standard peut être effectuée en utilisant «e0".
Généralement, le potentiel de réduction standard est calculé pour la demi-réaction qui se produit à la cathode en tant que demi-réaction de réduction. Le potentiel de réduction standard est très utile en chimie. Parfois, le terme potentiel d'électrode standard est également utilisé de manière interchangeable avec ce terme. La mesure de la réduction standard est effectuée en utilisant Volts (V). Le potentiel de réduction standard nous donne des informations sur la probabilité qu'un élément ou un ion doit être réduit en gagnant des électrons.
Quelle est la différence entre le potentiel d'électrode standard et le potentiel de réduction standard?
La principale différence entre le potentiel d'électrode standard et le potentiel de réduction standard est que le potentiel d'électrode standard est la tendance d'une électrode à perdre ou à gagner des électrons, tandis que le potentiel de réduction standard est la tendance d'une espèce chimique donnée. Cependant, ces deux termes sont utilisés de manière interchangeable parce que le terme potentiel d'électrode standard peut être utilisé pour la réduction et l'oxydation des demi-réactions.
L'infographie ci-dessous présente les différences entre le potentiel d'électrode standard et le potentiel de réduction standard de la forme tabulaire pour la comparaison côte à côte.
Résumé - Potentiel d'électrode standard vs potentiel de réduction standard
Le potentiel d'électrode standard est la mesure du potentiel d'équilibre, tandis que le potentiel de réduction standard est le potentiel de volts généré par la réduction de la réaction des réactions redox. La principale différence entre le potentiel d'électrode standard et le potentiel de réduction standard est que le potentiel d'électrode standard est la tendance d'une électrode à perdre ou à gagner des électrons, tandis que le potentiel de réduction standard est la tendance d'une espèce chimique donnée.
Référence:
1. Helmenstine, Anne Marie. «Définition du potentiel de réduction standard."Thoughtco, août. 28, 2020.
Image gracieuseté:
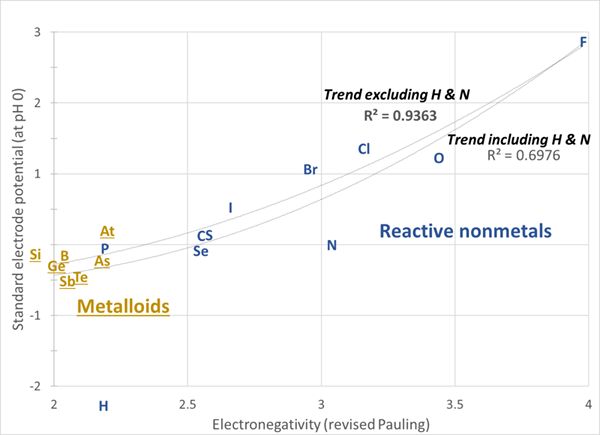
1. «En & Sep of Nonmetallic Elementsf» par SandBH (version originale d'avril 2018); YBG (Versions de juin 2018) - Propre travaux (CC BY-SA 4.0) via Commons Wikimedia