Quelle est la différence entre l'oxyde de manganèse et le dioxyde de manganèse
Le Différence clé entre l'oxyde de manganèse et le dioxyde de manganèse Est-ce que l'oxyde de manganèse apparaît sous forme de cristaux verts, tandis que le dioxyde de manganèse apparaît comme un solide brun ou noir.
L'oxyde de manganèse et le dioxyde de manganèse sont des composés d'oxyde inorganiques ayant des atomes de manganèse attachés aux atomes d'oxygène. Ces deux composés ont des applications importantes différentes.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que l'oxyde de manganèse
3. Qu'est-ce que le dioxyde de manganèse
4. Oxyde de manganèse vs dioxyde de manganèse sous forme tabulaire
5. Résumé - Oxyde de manganèse vs dioxyde de manganèse
Qu'est-ce que l'oxyde de manganèse?
L'oxyde de manganèse est un composé chimique ayant la formule chimique MNO. Cependant, nous pouvons utiliser ce terme pour faire référence à tout oxyde ou hydroxyde de manganèse, y compris l'oxyde de manganèse (II), le manganèse (II, III), le dioxyde de manganèse et l'oxyde de manganèse (VI).

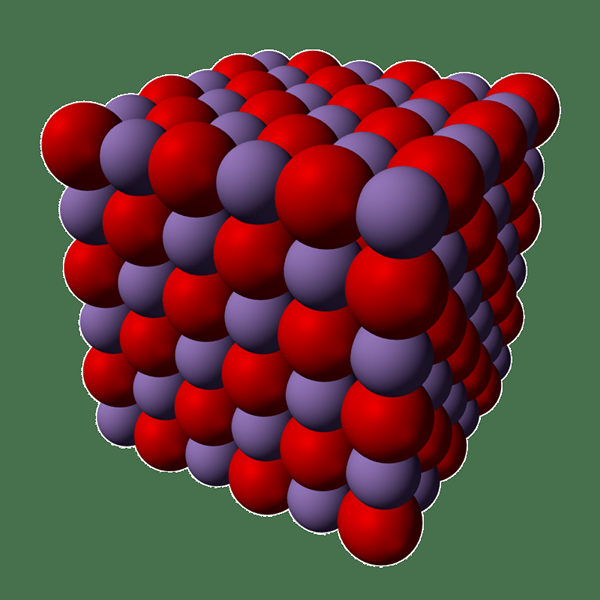
Figure 01: oxyde de manganèse
L'oxyde de manganèse apparaît sous forme de cristaux verts, et il est produit à grande échelle à utiliser comme composant des engrais et des additifs alimentaires. Semblable à d'autres monoxydes, MNO adopte également la structure du sel de roche, qui est donnée dans l'image ci-dessus. Il a des cations et des anions, tous deux coordonnés octaédriquement. De plus, similaire à de nombreux oxydes, le MNO est souvent non stoichiométrique et peut avoir une composition variable (varie du MNO à MNO1.045).
La masse molaire d'oxyde de manganèse est 70.93 g / mol. Il a une densité d'environ 5.43 g / mol. Le point de fusion est de 1945 degrés Celsius, et il est insoluble dans l'eau. Cependant, le MNO est soluble dans les acides. La structure cristalline de ce composé peut être décrite comme une structure d'halite.
Qu'est-ce que le dioxyde de manganèse?
Le dioxyde de manganèse est un composé inorganique ayant la formule chimique MNO2. Il apparaît comme une substance solide brun noir et se produit naturellement sous forme de pyrolusite minéral. C'est le principal minerai de manganèse, et il se produit également comme une composante des nodules de manganèse.

Figure 02: Dioxyde de manganèse
La masse molaire du dioxyde de manganèse est 86.93 g / mol, et la densité est 5.026 g / cm3. Le point de fusion est d'environ 535 degrés Celsius, et à des températures plus élevées, elle a tendance à se décomposer. Cependant, c'est insoluble dans l'eau. La structure cristalline du dioxyde de manganèse est tétragonale.
Il existe plusieurs polymorphes de MNO2 ainsi qu'une forme hydratée. Semblable à de nombreux autres dioxydes, cette substance se cristallise dans la structure cristalline rutile, ayant 3 centres de coordonnées d'oxyde et de métal octaédrique. Cette substance est caractéristiquement non stoichiométrique car elle manque d'oxygène. De plus, dans les réactions de synthèse organique, nous avons besoin de cette substance dans un état fraîchement préparé. La structure cristalline de ce composé a une structure très ouverte composée de canaux qui s'adaptent aux atomes métalliques, y compris de l'argent et du baryum.
Quelle est la différence entre l'oxyde de manganèse et le dioxyde de manganèse?
L'oxyde de manganèse et le dioxyde de manganèse sont des composés inorganiques importants formés à partir de l'oxydation des éléments chimiques du manganèse. La principale différence entre l'oxyde de manganèse et le dioxyde de manganèse est que l'oxyde de manganèse apparaît sous forme de cristaux verts, tandis que le dioxyde de manganèse apparaît comme un solide brun ou noir. Dans l'oxyde de manganèse, l'état d'oxydation du manganèse est de +2, tandis que dans le dioxyde de manganèse, l'état d'oxydation du manganèse est +4. De plus, l'oxyde de manganèse a une structure cristalline tétragonale tandis que le dioxyde de manganèse a une structure cristalline d'halite.
L'infographie ci-dessous présente les différences entre l'oxyde de manganèse et le dioxyde de manganèse sous forme tabulaire pour une comparaison côte à côte.
Résumé - Oxyde de manganèse vs dioxyde de manganèse
L'oxyde de manganèse et le dioxyde de manganèse sont des oxydes de manganèse. Cependant, le terme oxyde de manganèse est parfois utilisé comme nom collectif pour désigner tous les oxydes et hydroxydes fabriqués par des éléments chimiques du manganèse. La principale différence entre l'oxyde de manganèse et le dioxyde de manganèse est que l'oxyde de manganèse apparaît sous forme de cristaux verts, tandis que le dioxyde de manganèse apparaît comme un solide brun ou noir.
Référence:
1. «Oxyde de manganèse." Un aperçu | Sujets ScienceDirect.
Image gracieuseté:
1. «Manganais (II) -oxyde-xtal-3d-sf» par ccoil (talk) - propre travail (cc by-sa 3.0) via Commons Wikimedia
2. «Oxyde de manganèse (IV)» par Walkerma supposé - aucune source lisible par machine fournie. Propre travail assumé (sur la base des réclamations du droit d'auteur). (Domaine public) via Commons Wikimedia


