Quelle est la différence entre le processus isentropique et polytropique
Le Différence clé entre le processus isentropique et polytropique Est-ce que le processus isentropique montre toujours une efficacité plus faible, tandis que le processus polytropique montre toujours une efficacité plus élevée.
Le processus isentropique est un processus thermodynamique dans lequel des natures adiabatiques et réversibles peuvent être observées. Le processus polytropique, en revanche, est tout processus réversible sur tout système de gaz ou de vapeur ouvert ou fermé impliquant à la fois la chaleur et le transfert de travail de manière à ce qu'une combinaison spécifiée de propriétés soit maintenue tout au long du processus.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce qu'un processus isentropique
3. Qu'est-ce qu'un processus polytropique
4. Isentropic vs processus polytropique sous forme tabulaire
5. Résumé - processus polytropique vs polytropique
Qu'est-ce qu'un processus isentropique?
Un processus isentropique est un processus thermodynamique dans lequel des natures adiabatiques et réversibles peuvent être observées. Dans ce processus, les transferts de travaux du système ont tendance à être sans friction et à se produire sans le transfert de chaleur ni de matière. Il s'agit d'un processus idéalisé qui est utile dans l'ingénierie en tant que modèle de comparaison avec des processus réels. Nous pouvons l'idéaliser comme un processus réversible qui ne se produit pas en réalité. En effet. Cependant, nous pouvons interpréter ce terme d'une autre manière, je.e., Un système qui a son entropie inchangé.

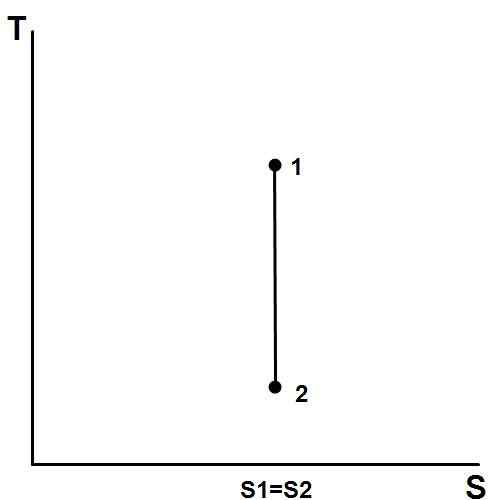
Figure 01: Dans un T-S (entropie vs. Température) Diagramme d'un processus isentropique. Ici, l'entropie reste constante
Les processus spontanés augmentent l'entropie de l'univers. Lorsque cela se produit, l'entropie du système ou l'entropie environnante peut augmenter. Un processus isentropique se produit lorsque l'entropie du système reste constante.
Un processus adiabatique réversible est un exemple de processus isentropique. De plus, les paramètres constants dans un processus isentropique sont l'entropie, l'équilibre et l'énergie thermique.
Qu'est-ce qu'un processus polytropique?
Un processus polytropique peut être décrit comme tout processus réversible sur tout système de gaz ou de vapeur ouvert ou fermé impliquant à la fois la chaleur et le transfert de travail de telle manière qu'une combinaison spécifiée de propriétés est maintenue tout au long du processus. Il se produit avec un transfert de chaleur. Cependant, le transfert de chaleur se produit de manière réversible dans ce processus. Lorsqu'un gaz subit ce type de transfert de chaleur, l'équation suivante est vraie pour un processus polytropique.
PVN = constant
Ici, P est la pression, V est le volume, et n est une constante. Par conséquent, pour maintenir PV constant dans le processus d'expansion / compression de gaz polytropique, l'échange de chaleur et de travail se déroule entre le système et son environnement. Par conséquent, le polytropique est un processus non adiabatique.
Quelle est la différence entre le processus isentropique et polytropique?
Un processus isentropique est un processus thermodynamique dans lequel des natures adiabatiques et réversibles peuvent être observées. Un processus polytropique est un processus réversible sur tout système de gaz ou de vapeur ouvert ou fermé impliquant à la fois la chaleur et le transfert de travail. La principale différence entre le processus isentropique et polytropique est qu'un processus isentropique montre toujours une efficacité plus faible, tandis qu'un processus polytropique montre toujours une efficacité plus élevée.
L'infographie ci-dessous présente les différences entre le processus isentropique et polytropique sous forme tabulaire pour une comparaison côte à côte.
Résumé - processus polytropique vs polytropique
Les processus isentropiques et les processus polytropiques sont importants en chimie physique. Un processus isentropique est un processus thermodynamique dans lequel des natures adiabatiques et réversibles peuvent être observées. Un processus polytropique est un processus réversible sur tout système de gaz ou de vapeur ouvert ou fermé impliquant à la fois la chaleur et le transfert de travail. La principale différence entre le processus isentropique et polytropique est qu'un processus isentropique montre toujours une efficacité plus faible qu'un processus polytropique.
Référence:
1. Kirkby, n.F. «Processus polytropique." Thermopdie, Begel House Inc.
Image gracieuseté:
1. «Isentropic» par Tyler.Neysmith - Propre travaux (CC BY-SA 3.0) via Commons Wikimedia


