Différence entre le perborate de sodium et le percarbonate
Le différence clé entre le perborate de sodium et le percarbonate est que Le perborate de sodium contient un anion perborate composé d'un -B-O-o-noyau cyclique avec deux groupes hydroxyle attachés à chaque atome de bore tandis que le percarbonate de sodium est simplement un adduit avec du peroxyde d'hydrogène.
Le perborate de sodium et le percarbonate de sodium sont des composés inorganiques ayant du sodium comme cations.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que le perborate de sodium
3. Qu'est-ce que le percarbonate de sodium
4. Comparaison côte à côte - Perborate de sodium vs percarbonate sous forme tabulaire
5. Résumé
Qu'est-ce que le perborate de sodium?
Le perborate de sodium est un composé chimique inorganique ayant la formule chimique NAH2BO4 ou NA2H4B2O8. Nous pouvons abréger le nom de ce composé en tant que PBS. Ce composé se trouve couramment sous sa forme anhydre ou sous la forme de l'hexahydrate; e.g. La forme monohydrate de perborate de sodium est nommée PBS-1, et la forme tétrahydrate est appelée PBS-4. Ces deux formes hydratées de perborate de sodium sont des solides blancs, inodores et solubles dans l'eau. Le sel de perborate de sodium est principalement utilisé dans la fabrication de détergents à linge. Là, il agit comme l'une des plages à base de peroxyde.
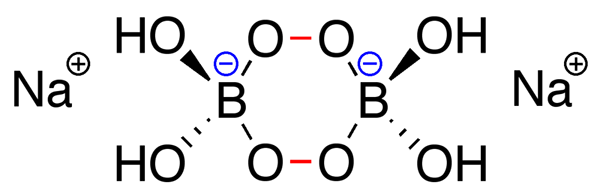
Figure 01: Structure du perborate de sodium
Lorsque l'on considère la structure de base du perborate de sodium, elle est différente des structures chimiques du percarbonate de sodium et du perphosphate de sodium car il a un anion perborate composé d'un -B-O-o-noyau cyclique avec deux groupes hydroxyle attachés à chaque atome de bore et chaque boron. Cette structure annulaire adopte généralement une conformation de chaise.
En règle générale, le perborate de sodium subit facilement une hydrolyse lorsqu'il est ajouté à l'eau, qui produit du peroxyde d'hydrogène et du borate. Dans une solution de perborate de sodium aqueux, l'anion cyclique subit une hydrolyse en deux anions de [B (OH) 3 (OOH)]-. De plus, la forme monohydrate de ce composé peut facilement se dissoudre dans l'eau par rapport à la forme du tétrahydrate, et il a également une stabilité thermique plus élevée. Par conséquent, nous pouvons former un monohydrate du chauffage du tétrahydrate de sodium perborate.
Lorsque vous envisagez les utilisations du perborate de sodium, il sert de source stable d'oxygène actif dans de nombreux détergents, détergent à lessive, produits de nettoyage et blanchisserie. De plus, il est présent dans certaines formules de blanchiment dentaires pour les dents traitées par racine non vitales.
Qu'est-ce que le percarbonate de sodium?
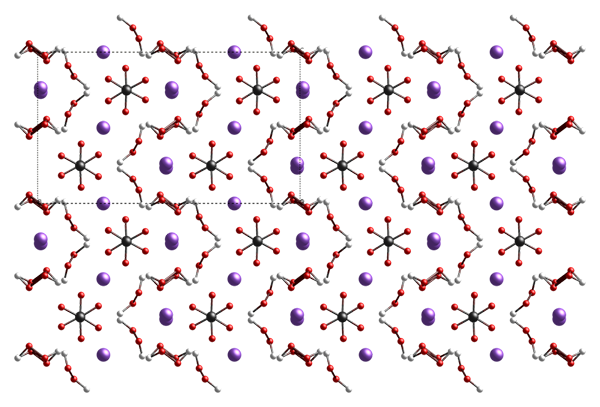
Le percarbonate de sodium est un composé inorganique ayant la formule chimique NA2H3CO6. Nous pouvons observer ce composé comme un adduit de carbonate de sodium et de peroxyde d'hydrogène, dont la formule peut être correctement écrite comme 2NA2CO3.3h2o. Le percarbonate de sodium est un solide hygroscopique incolore, cristallin et hygroscopique qui est soluble dans l'eau. Nous pouvons abréger ce composé en SPC. Habituellement, cette substance contient 32.5% en poids de peroxyde d'hydrogène.

Figure 02: Structure du percarbonate de sodium
Lorsque le percarbonate de sodium est dissous dans l'eau, il donne un mélange de peroxyde d'hydrogène (qui subit finalement une décomposition pour former de l'eau à l'oxygène), des cations de sodium et des anions carbonatés.
Lorsque vous envisagez les utilisations du percarbonate de sodium, il est important en tant qu'agent oxydant dans les produits à linge, les produits de nettoyage, etc. Il est également utile comme agent de nettoyage dans de nombreux homebrewers. De plus, nous pouvons utiliser ce composé en synthèse organique comme source pratique de peroxyde d'hydrogène anhydre dans des solvants particuliers.
Quelle est la différence entre le perborate de sodium et le percarbonate?
Le perborate de sodium et le percarbonate de sodium sont des composés inorganiques ayant du sodium comme cations. La principale différence entre le perborate de sodium et le percarbonate est que le perborate de sodium contient un anion perborate composé d'un -B-O-o-noyau cyclique avec deux groupes hydroxyle attachés à chaque atome de bore tandis que le percarbonate de sodium est simplement un adduit avec le perroxyde d'hydrogène.
Ci-dessous, l'infographie tabule plus de différences entre le perborate de sodium et le percarbonate pour une comparaison côte à côte.

Résumé - Perborate de sodium vs percarbonate
Le perborate de sodium et le percarbonate de sodium sont des composés inorganiques ayant du sodium comme cation. La principale différence entre le perborate de sodium et le percarbonate est que le perborate de sodium contient un anion perborate composé d'un -B-O-o-noyau cyclique avec deux groupes hydroxyle attachés à chaque atome de bore tandis que le percarbonate de sodium est simplement un adduit avec le perroxyde d'hydrogène.
Référence:
1. «Percarbonate de sodium.”Wikipedia, disponible ici.
Image gracieuseté:
1. «Perborate Dimer» (domaine public) via Commons Wikimedia
2. «Sodium-Percarbonate-XTAL-100K-2003-CM-3D-BALLS» par Ben Mills - Propre travaux (domaine public) via Commons Wikimedia


