Différence entre la solution saturée et concentrée
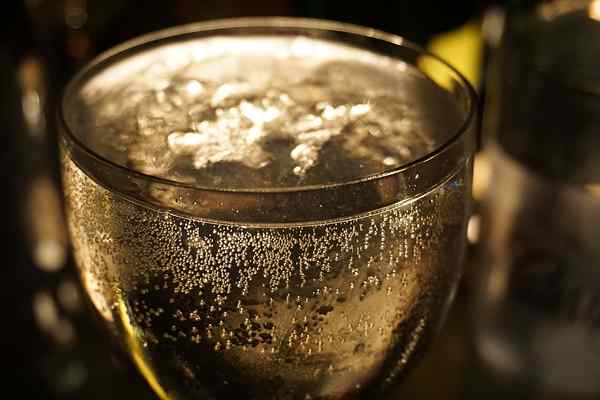
Différence clé - saturée contre Concentré Solution
Une solution est une phase liquide de la matière formée en dissolvant un soluté dans un solvant. Une solution peut être convertie en une solution saturée en ajoutant plus de solutés jusqu'à ce qu'aucun plus de solutés ne puisse être dissous. Une solution concentrée contient une quantité considérablement élevée de solutés, mais ce montant n'est pas le maximum. Le différence clé entre une solution saturée et concentrée est que Les solutés supplémentaires ne peuvent pas être dissous dans une solution saturée car il contient la quantité maximale de solutés tandis que des solutés supplémentaires peuvent être dissous dans une solution concentrée car elle ne contient pas la quantité maximale de solutés (non saturée de soluté).
CONTENU
1. Aperçu et différence clé
2. Quelle est la solution saturée
3. Qu'est-ce que la solution concentrée
4. Similitudes entre la solution saturée et concentrée
5. Comparaison côte à côte - solution saturée vs concentrée sous forme tabulaire
6. Résumé
Quelle est la solution saturée?
Une solution saturée est une solution chimique contenant la concentration maximale d'un soluté dissous dans le solvant. Les solutés supplémentaires ne peuvent pas être dissous dans une solution saturée car il contient la quantité maximale de solutés. La forme opposée de la solution saturée est la solution insaturée. La solution insaturée n'est pas saturée de soluté. Une solution insaturée peut être une solution concentrée ou une solution diluée.
Il existe plusieurs facteurs qui affectent la saturation d'une solution. Ces facteurs affectent la dissolution des solutés dans le solvant.
- Température - La solubilité des composés solides augmente avec l'augmentation de la température du solvant. Par conséquent, plus de solutés peuvent être dissous dans le solvant chaud plutôt que dans le solvant froid.
- Pression - Plus de solutés peuvent être des forces pour se dissoudre dans le solvant en appliquant une pression. Par conséquent, la dissolution des solutés peut être augmentée en augmentant la pression du système. Ex: gaz.
- Composition chimique - Si d'autres solutés sont déjà présents dans la solution, cela affecte la solubilité des solutés.
Une solution saturée peut être produite en ajoutant un soluté au solvant jusqu'à ce que plus de solutés ne se dissolvent. Ou bien, cela peut être fait en évaporant le solvant de la solution jusqu'à ce que le soluté commence à former des cristaux. Une autre méthode, bien que ce n'est pas très courant est d'ajouter des graines de cristaux à une solution sursaturée. Une solution sursaturée contient de nombreux solutés qui restent dissous même si la solution est refroidie. Lorsque des graines de cristaux sont ajoutées à cette solution sursaturée, les solutés commencent à cristalliser, donnant une solution saturée.
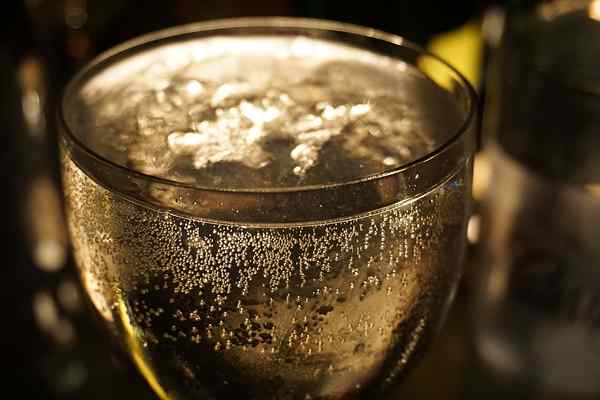
Figure 01: Les jus étincelants sont des solutions saturées
Certains exemples de solutions saturées comprennent l'eau gazeuse (saturée de carbone), les solutions de sucre saturées (plus de sucre ne peut être dissous), la bière ou les jus étincelants sont saturés de dioxyde de carbone, etc.
Qu'est-ce que la solution concentrée?
Une solution concentrée est une solution chimique contenant une quantité élevée d'un soluté dissous dans le solvant. Des solutés supplémentaires peuvent être dissous dans une solution concentrée car elle ne contient pas la quantité maximale de solutés (non saturée de soluté). La forme opposée de la solution concentrée est une solution diluée. Une solution diluée contient une quantité relativement faible de solutés dissous dans un solvant.

Figure 02: Une solution concentrée (à droite) a une couleur forte par rapport à une solution diluée (à gauche)
Les solutions concentrées d'acides ou de bases sont reconnues comme des acides forts ou des bases fortes. En revanche, les acides ou les bases dilués sont des acides ou des bases faibles. Le terme concentré est utilisé pour donner une idée quantitative d'une solution. Une solution concentrée peut être formée en dissolvant plus de solutés dans une solution ou en évaporant une solution jusqu'à ce qu'une quantité considérable de solvant soit évaporée en laissant des solutés dans la solution. La concentration d'une solution peut être donnée comme ci-dessous. Là, la concentration est donnée par l'unité mol / L.
Concentration = nombre de moles de solutés / volume de la solution
Quelles sont les similitudes entre la solution saturée et concentrée?
- La solution saturée et concentrée sont des solutions contenant une quantité élevée de solutés
- Les termes de solutions saturées et concentrées expriment une idée quantitative des solutions.
Quelle est la différence entre la solution saturée et concentrée?
Solution saturée vs concentrée | |
| Une solution saturée est une solution chimique contenant la concentration maximale d'un soluté dissous dans le solvant. | Une solution concentrée est une solution chimique contenant une quantité élevée d'un soluté dissous dans le solvant. |
| Quantité de solutés | |
| La solution saturée contient la quantité maximale de solutés qu'il peut contenir. | La solution concentrée contient une quantité considérablement élevée de solutés. |
| Ajout de plus de solutés | |
| Les solutés supplémentaires ne peuvent pas être dissous dans une solution saturée car elle contient le maximum. | Des solutés supplémentaires peuvent être dissous dans une solution concentrée car elle ne contient pas la quantité maximale de solutés (non saturée de soluté). |
| Forme opposée | |
| La forme opposée de solution saturée est une solution insaturée. | La forme opposée de solution concentrée est une solution diluée. |
| Exemples | |
| Certains exemples de solutions saturées comprennent de l'eau gazeuse, des solutions de sucre saturées, de la bière ou des jus étincelants sont saturés de dioxyde de carbone, etc. | Certains exemples de solutions concentrées comprennent des acides concentrés et des bases concentrées utilisées dans les laboratoires. |
Résumé - saturé contre Concentré Solution
Une solution saturée est une forme d'une solution concentrée, mais il contient la quantité maximale de solutés qui peuvent maintenir. La différence entre la solution saturée et concentrée est que les solutés supplémentaires ne peuvent pas être dissous dans une solution saturée car il contient la quantité maximale de solutés tandis que des solutés supplémentaires peuvent être dissous dans une solution concentrée car elle ne contient pas la quantité maximale de solutés (non saturée de saturation de saturation le soluté).
Référence:
1.«13.2: Solutions saturées et solubilité.”Chemistry LibreTexts, LibreTexts, 8 octobre. 2017. Disponible ici
2.«Comment concentrer une solution.”Science. Disponible ici
3.Helmenstine, Anne Marie, D. «Définition de solution saturée et exemples.”Thoughtco, Jun. 20, 2017. Disponible ici
Image gracieuseté:
1.'2980956' par Nicole_80 (domaine public) via Pixabay
2.'Riboflavinsolution' par sbharris - propre travail, (cc by-sa 3.0) via Commons Wikimedia


