Différence entre le pont salé et la liaison hydrogène
Le différence clé entre le pont salé et la liaison hydrogène est que Le pont salé est un tube avec un électrolyte reliant deux demi-cellules dans une cellule électrochimique, tandis que la liaison hydrogène est une force d'attraction entre deux atomes de deux molécules différentes.
Le pont salé est très utile pour maintenir la connectivité entre deux demi-cellules d'une cellule électrochimique. Il est visible à l'œil nu. Cependant, la liaison hydrogène est une liaison chimique qui maintient la connectivité entre deux molécules, qui peuvent former des liaisons hydrogène.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce qu'un pont de sel
3. Qu'est-ce qu'une liaison hydrogène
4. Comparaison côte à côte - Bridge de sel vs liaison hydrogène sous forme tabulaire
5. Résumé
Qu'est-ce qu'un pont de sel?
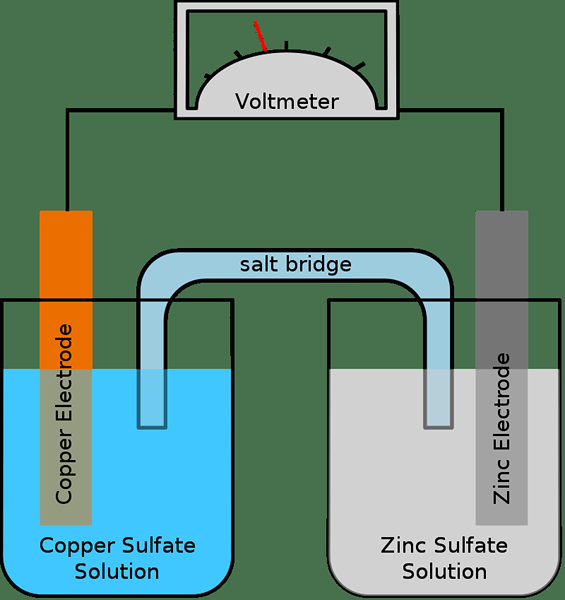
Salt Bridge est un tube qui contient un électrolyte (généralement sous la forme d'un gel), fournissant un contact électrique entre deux solutions. Par conséquent, ce tube est important pour connecter les réactions d'oxydation et de réduction de la cellule galvanique. Le but de l'utilisation d'un pont de sel est de faciliter rapidement la réaction électrochimique atteignant l'équilibre. S'il n'y a pas de pont de sel, une demi-cellule accumulera des charges positives, et l'autre demi-cellule accumule les charges négatives. Par conséquent, la production d'électricité s'arrête.
Il existe deux principaux types de ponts de sel: pont de tube en verre et pont en papier filtre. Le pont de sel en verre est un tube U en verre et il contient l'électrolyte. Dans le pont de sel en papier filtre, il y a un papier filtre trempé avec l'électrolyte.
Qu'est-ce que la liaison hydrogène?
Une liaison hydrogène est un type de force d'attraction entre deux atomes de deux molécules différentes. C'est une faible force d'attraction. Mais, par rapport à d'autres types de forces intramoléculaires telles que les interactions polaires polaires, les interactions non polaires-nonpolaires comme les forces de Vander Waal, la liaison hydrogène est plus forte.
Habituellement, les liaisons hydrogène se forment entre les molécules covalentes polaires. Ces molécules contiennent des liaisons covalentes polaires, qui se forment à la suite de la différence dans les valeurs d'électronégativité des atomes qui sont dans la liaison covalente. Si cette différence est élevée, l'atome hautement électronégatif a tendance à attirer les électrons de la liaison vers lui-même. Ainsi, cela crée un moment dipolaire où cet atome hautement électronégatif obtient une charge négative partielle, tandis que l'autre atome obtient une charge positive partielle. Alors la liaison devient une liaison covalente polaire. Lorsque cette molécule rencontre une autre molécule qui a un moment dipolaire comme celui-ci, les charges négatives et positives ont tendance à s'attirer. Et, cette force d'attraction est appelée liaison hydrogène.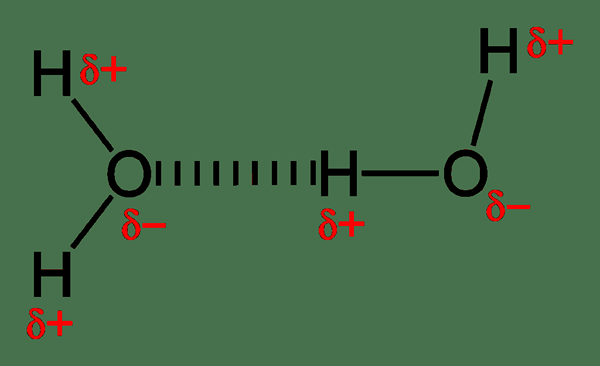
De plus, des liaisons hydrogène se forment entre des atomes hautement électronégatifs et des atomes moins électronégatifs. De plus, ils existent lorsque nous avons O, N et F dans une molécule et Host positif chargé dans l'autre molécule. C'est parce que F, N et O sont les atomes les plus électronégatifs capables de former des liaisons hydrogène.
Quelle est la différence entre le pont de sel et la liaison hydrogène?
Le pont salé et la liaison hydrogène sont importants dans la connectivité de la ligne de ligne entre les objets souhaités. Par exemple, un pont de sel relie deux demi-cellules d'une cellule électrochimique, tandis que Hydrogène Bond relie deux molécules. La principale différence entre le pont de sel et la liaison hydrogène est qu'un pont de sel est un tube avec un électrolyte reliant deux demi-cellules dans une cellule électrochimique. Mais, une liaison hydrogène est une force d'attraction entre deux atomes de deux molécules différentes.
En dessous de l'infographie résume la différence entre le pont de sel et la liaison hydrogène.

Résumé - Bridge de sel vs liaison hydrogène
Le pont salé et la liaison hydrogène sont importants pour maintenir la connectivité entre les objets souhaités. Par exemple, le pont de sel relie deux demi-cellules d'une cellule électrochimique, tandis que la liaison hydrogène relie deux molécules. La principale différence entre le pont de sel et la liaison hydrogène est qu'un pont de sel est un tube composé d'un électrolyte, et il relie deux demi-cellules dans une cellule électrochimique, tandis que la liaison hydrogène est une force d'attraction entre deux atomes de deux molécules différentes.
Référence:
1. Helmenstine, Anne Marie. «Définition du pont salé."Thoughtco, juil. 3, 2019, disponible ici.
Image gracieuseté:
1. «Galvanic Cell» par Gringer - Fichier: Galvanische Zelle.png, par tinux (cc by-sa 3.0) via Commons Wikimedia
2. «Hydrogène-liaison dans l'eau-2D» (domaine public) via Commons Wikimedia


