Différence entre monatomique et polyatomique
Monatomique vs polyatomique
Le nombre d'atomes présents dans un ion ou une molécule particulier est ce qui contribue à la différence entre monatomique et polyatomique. Les deux mots «mono» et «poly» donnent l'idée générale de la molécule; «Mono» signifie «célibataire» et «poly» signifie «beaucoup.”Monatomic fait référence aux ions ou molécules ayant un seul atome. Le polyatomique fait référence aux molécules ou aux ions ayant deux atomes ou plus. Il y a tellement de différences physiques et chimiques entre monatomique et polyatomique en raison de la différence de nombre d'atomes. Les éléments chimiques généralement monatomiques sont moins abondants par rapport à l'existence de molécules polyatomiques.
Qu'est-ce que monatomique?
Le mot monatomique dérive de deux mots «mono» et «atomique», donnant le sens de «atome unique.«Les espèces chimiques monatomiques ne contiennent qu'un seul atome et elles sont stables même si elles existent seules. Cela peut être appliqué aux gaz et aux ions. La plupart des gaz nobles existent sous forme d'espèces chimiques monatomiques.
Ions monatomiques: Ces ions sont formés en perdant (ions positifs) ou en gagnant des électrons (ions négatifs).
Ions positifs: N / A+, K+, Ca2 +, Al3+
Ions négatifs: CL-, S2-, BR-, F-
Molécules monatomiques: Les gaz nobles entrent dans cette catégorie et ils sont très stables; Par conséquent, chimiquement inactif.

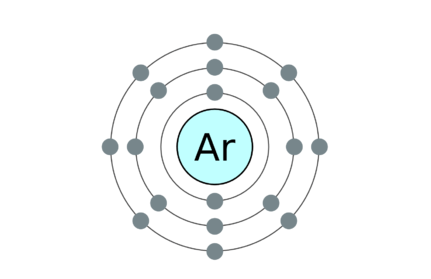
18: Argon 2, 8, 8
Qu'est-ce que le polyatomique?
Le mot polyatomique dérive de deux mots «poly» et «atomique», signifie Beaucoup d'atomes. Il peut s'agir d'atomes homogènes (o2, HG22+, O3, O22-) ou une combinaison d'atomes hétérogènes (CN-, H2DONC4, CLO3-). La plupart des molécules et des ions existent comme nature polyatomique.
Ions polyatomiques: «Ions moléculaires» est un autre nom pour les ions polyatomiques. La plupart des ions polyatomiques sont soit des espèces chimiques liées de manière covalente, soit des complexes métalliques.
Ions positifs: NH4+, H3O+, PH4+
Ions négatifs: Cro42-, CO32-, Ch3ROUCOULER-, DONC42-, NON3-
Molécules polyatomiques: Ce sont les molécules avec deux atomes ou plus. Ils n'ont pas de charge positive ou négative. En d'autres termes, ces molécules sont électriquement neutres. (H2DONC4, Ch3COOH, NA2CO3, Nacl, c2H4)
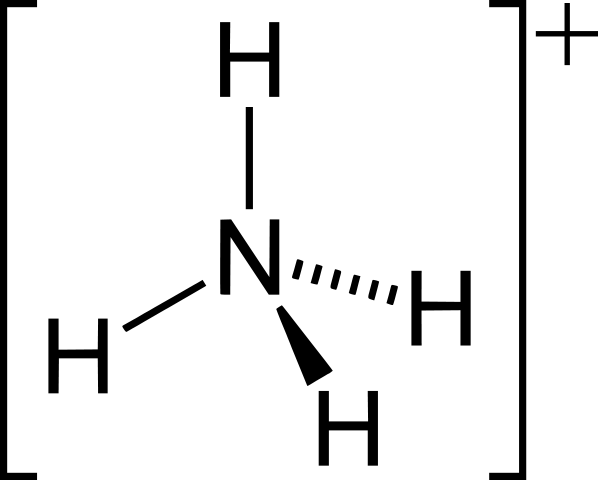
Ammonium
Quelle est la différence entre monatomique et polyatomique?
• Nombre d'atomes:
• Les éléments chimiques monatomiques contiennent Un seul atome.
• Les composés chimiques polyatomiques ont deux atomes ou plus.
• État:
• Les espèces chimiques monatomiques peuvent être des ions ou des gaz inertes.
• Certaines espèces polyatomiques sont des ions et certaines sont des molécules.
• Propriétés
• La plupart des ions monatomiques sont stables dans l'eau.
• Les molécules monatomiques sont très stables; Par conséquent, chimiquement inactif.
• La plupart des ions polyatomiques sont des complexes liés de manière covalente ou métalliques.
• Les molécules polyatomiques sont électriquement neutres.
• Exemples de monatomique et de polyatomique:
• Exemples pour ions monatomiques sont na+, Californie2+, K+, Al3+ et Fe3+.
• Exemples pour molécules monatomiques sont des gaz nobles. Ce sont l'hélium (He), le néon (NE), l'argon (AR), Krypton (KR), le xénon (XE) et le radon (RA).
• Exemples pour ions polyatomiques sont cro42-, CO32-, NH4+, H3O+.
• Exemples pour molécules polyatomiques sont KCL, KBRO3, C6H5COOH.
• Taille:
• La taille des espèces chimiques monatomiques diffère selon la façon dont ils se forment. Par exemple, lorsque des ions positifs sont formés, leurs tailles diminuent et lorsque des ions négatifs sont formés, la taille augmente que l'atome d'origine. Les gaz nobles ont la plus petite taille par rapport aux autres éléments de leur période dans le tableau périodique.
• Lorsque des composés chimiques polyatomiques se forment, la taille de l'ion polyatomique ou de la molécule polyatomique devient plus grande que tous les atomes d'origine du composé. Parce que deux atomes ou plus se combinent pour former un ion / molécule polyatomique.
• Forme:
• Les molécules et ions généralement monatomiques sont sphériques dans leur géométrie.
• La géométrie des espèces chimiques polyatomiques varie en fonction du nombre de molécules et des paires solitaires présentes dans la molécule. Comme le nombre d'atomes augmente des structures plus complexes pour atteindre la stabilité.
Images gracieuseté:
- Argon par Greg Robson (CC BY-SA 2.0 UK)
- Ammonium via Wikicommons (domaine public)