Différence entre la métathèse et les réactions redox
Le différence clé entre la métathèse et les réactions redox est que Dans les réactions de métathèse, l'échange de deux espèces ioniques entre deux molécules se produit alors que, dans les réactions redox, l'échange d'électrons entre deux espèces chimiques se produit.
La métathèse et les réactions redox sont deux types de réactions chimiques. Mais ils ont des mécanismes d'action différents. La métathèse est une réaction en une seule étape, tandis qu'une réaction redox a deux demi-réactions parallèles requises pour le processus d'échange d'électrons.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que la métathèse
3. Quelles sont les réactions redox
4. Similitudes entre la métathèse et les réactions redox
5. Comparaison côte à côte - Métathèse vs réactions redox sous forme tabulaire
6. Résumé
Qu'est-ce que la métathèse?
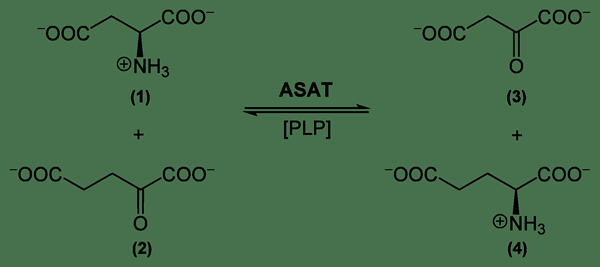
La métathèse ou les réactions à double déplacement sont un type de réaction chimique dans laquelle un échange de deux espèces ioniques entre deux molécules se produit. La formule générale est la suivante:
A-B + C-D ⟶ A-C + B-D
La liaison qui se casse et se forme pendant cette réaction peut être des liaisons ioniques ou covalentes. Certains exemples de ce type de réaction comprennent les réactions de précipitation, les réactions acides, l'alkylation, etc.
Dans l'équation ci-dessus, les composants A et C de chaque réactif ont changé leur place. Généralement, ces réactions se produisent dans des solutions aqueuses. De plus, nous pouvons classer ces réactions comme suit;
- Réactions de précipitation - Un précipité se forme à la fin de la réaction. Par exemple, la réaction entre le nitrate d'argent et le chlorure de sodium forme un précipité en chlorure d'argent et du nitrate de sodium aqueux.
- Réactions de neutralisation - Un acide neutralise lors de la réaction avec une base. Par exemple, une solution HCl (acide) peut être neutralisée à partir d'une solution de NaOH (base).

Figure 01: Un exemple de réaction à double déplacement
Qu'est-ce que la réaction redox?
La réaction redox est un type de réaction chimique dans laquelle l'oxydation et la réduction des demi-réactions se produisent simultanément. Dans cette réaction, nous considérons l'oxydation et la réduction comme des processus complémentaires. Ici, l'oxydation est la perte d'électrons ou l'augmentation de l'état d'oxydation tandis que la réduction est le gain d'électrons ou la diminution de l'état d'oxydation.
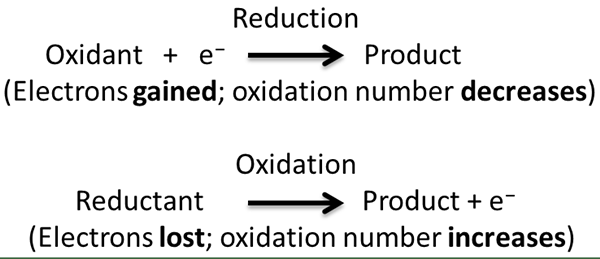
Figure 02: Mécanisme des réactions d'oxydation et de réduction
De plus, la vitesse d'une réaction redox peut varier de processus très lents tels que la rouille à des processus rapides tels que la combustion de carburant.
Quelles sont les similitudes entre la métathèse et les réactions redox?
- La métathèse et les réactions redox sont des réactions chimiques où les produits sont complètement différents des réactifs.
- Les deux réactions impliquent l'échange de quelque chose entre les réactifs pour donner au (s) produit le (s). e.g échange d'électrons, fragments chimiques.
- Ces réactions impliquent deux réactions complémentaires. E.g. Réactions d'oxydation-réduction dans les réactions redox, réactions de formation de liaison des liaisons dans les réactions de métathèse.
Quelle est la différence entre la métathèse et les réactions redox?
La métathèse et les réactions redox sont deux types de réactions chimiques. La principale différence entre la métathèse et les réactions redox est que dans les réactions de métathèse, l'échange de deux espèces ioniques entre deux molécules se produit alors que, dans les réactions redox, l'échange d'électrons entre deux espèces chimiques se produit. Une réaction ou une métathèse à double déplacement est une réaction en une seule étape, mais une réaction redox a deux demi-réactions parallèles requises pour le processus d'échange d'électrons. De plus, les états d'oxydation des atomes changent nécessairement lors d'une réaction redox mais, dans les réactions de métathèse, elle peut ou non changer.
En dessous de l'infographie résume la différence entre la métathèse et les réactions redox.

Résumé - Métathèse vs réactions redox
La métathèse et les réactions redox sont deux types de réactions chimiques. La principale différence entre la métathèse et les réactions redox est que dans les réactions de métathèse, l'échange de deux espèces ioniques entre deux molécules se produit alors que, dans les réactions redox, l'échange d'électrons entre deux espèces chimiques se produit. De plus, la métathèse est une réaction en une seule étape, tandis qu'une réaction redox a deux demi-réactions parallèles requises pour le processus d'échange d'électrons.
Référence:
1. «Réactions de métathèse.”Chemistry LibreTexts, LibreTexts, 5 juin 2019, disponible ici.
2. «Réactions d'oxydation-réduction.”Chemistry LibreTexts, LibreTexts, 5 juin 2019, disponible ici.
Image gracieuseté:
1. «Aspartate Transaminase Reaction» par Yikrazuul - Propre travaux (domaine public) via Commons Wikimedia
2. «Redox Halves» par Cameron Garnham - Propre travaux (CC By-SA 3.0) via Commons Wikimedia


