Différence entre le carbonate métallique et le carbonate d'hydrogène métallique
Le différence clé entre le carbonate métallique et le carbonate d'hydrogène métallique est que Les carbonates métalliques contiennent un cation métallique et un anion carbonate tandis que les carbonates d'hydrogène métallique contiennent un cation métal.
Le carbonate métallique et l'hydrogène métallique carbonate sont des composés inorganiques. Les carbonates métalliques contiennent des cations métalliques car un ion carbonate a -2 charge électrique. Les carbonates d'hydrogène métallique ou les bicarbonates métalliques contiennent des cations métalliques car l'anion bicarbonate a -1 charge électrique.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que le carbonate de métal
3. Qu'est-ce que le carbonate d'hydrogène métallique
4. Comparaison côte à côte - carbonate de métal vs métal hydrogène carbonate sous forme tabulaire
5. Résumé
Qu'est-ce que le carbonate de métal?
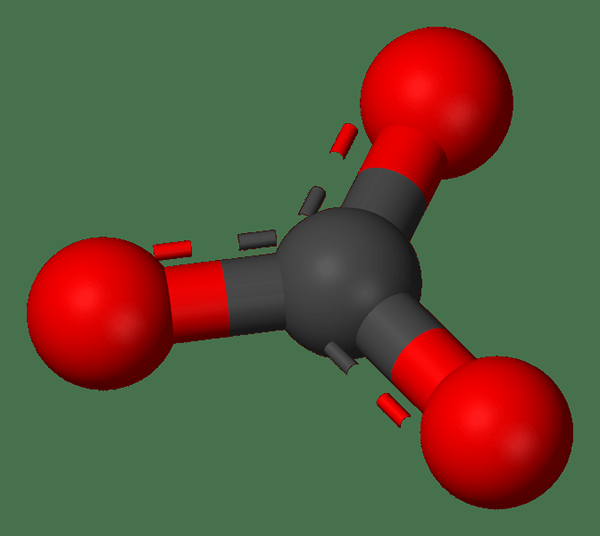
Les carbonates métalliques sont des composés inorganiques contenant un cation métallique et un anion carbonate. Le carbonate, en chimie, est un sel d'acide carbonique. L'ion carbonate est un ion polyatomique ayant la formule chimique CO32-. Le composé qui se forme à partir de l'association de l'anion carbonate et du cation métallique est nommé en sel de carbonate.

Figure 01: Structure de l'anion carbonate
Généralement, les composés de carbonate métallique subissent une décomposition sur un traitement thermique. Le carbonate de métal a tendance à libérer le dioxyde de carbone, laissant derrière lui un composé d'oxyde du métal. Nous pouvons appeler ce processus calcinant; Ce nom est dérivé du mot latin «calx» utilisé pour la chaux rapide ou l'oxyde de calcium, Cao, que nous pouvons obtenir du processus de torréfaction du calcaire dans un four à chaux.
Les carbonates métalliques se forment lorsque les ions métalliques de chargement positivement interagissent avec les anions carbonatés. Les ions métalliques ou les ions métalliques chargés positivement peuvent être sous la forme de m+, M2+, et M3+. Ces ions métalliques ont des ions métalliques monovalents, divalents et trivalents, respectivement. Ils peuvent s'associer à des atomes d'oxygène chargés négativement dans l'anion carbonate via les forces d'attraction électrostatique entre l'ion métallique et l'anion carbonate. Cette interaction forme le composé ionique du carbonate métallique.
Généralement, les carbonates métalliques sont insolubles dans l'eau à des conditions de température et de pression standard. Cependant, il y a quelques exceptions, comme le lithium, le sodium et les carbonates de potassium. Bien que la plupart des carbonates métalliques soient insolubles dans l'eau, la plupart des bicarbonates sont des composés solubles dans l'eau.
Qu'est-ce que le carbonate d'hydrogène métallique?
Les carbonates d'hydrogène métallique ou les bicarbonates métalliques sont des composés inorganiques contenant un cation métallique et un anion bicarbonate. La formule chimique de l'anion bicarbonate est HCO3-. Le bicarbonate est le nom commun de ces composés tandis que les carbonates d'hydrogène sont le nom recommandé de la nomenclature IUPAC. Selon cette méthode de nomenclature, le préfixe «bi-» fait référence à la présence d'un seul ion hydrogène. Un exemple similaire est le bisulfite, où l'anion est HSO3-.
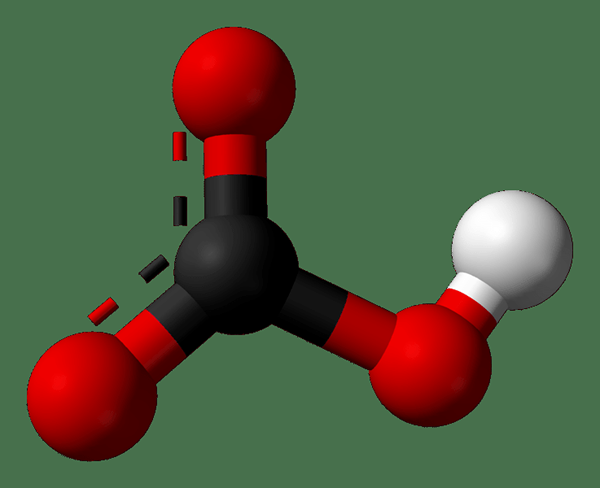
Figure 02: Structure de l'anion bicarbonate
Les composés de carbonate d'hydrogène métallique se forment lorsque des cations métalliques chargées positivement s'associent à un anion bicarbonate chargé négativement. Ceci est une attraction électrostatique où un composé ionique se forme. De nombreux composés de bicarbonate sont solubles dans l'eau aux conditions de température et de pression standard.
Quelle est la différence entre le carbonate métallique et le carbonate d'hydrogène métallique?
Le carbonate métallique et l'hydrogène métallique carbonate sont des composés inorganiques. La principale différence entre le carbonate métallique et l'hydrogène métallique carbonate est que les carbonates métalliques contiennent des anions carbonatés tandis que les composés de carbonate d'hydrogène métallique contiennent des anions bicarbonate. La plupart des carbonates métalliques sont insolubles dans l'eau tandis que la plupart des carbonates d'hydrogène métallique sont des composés solubles dans l'eau. De plus, le carbonate de métal agit comme un tampon dans le sang tandis que le carbonate d'hydrogène métallique agit comme un composant dans un système de tampon de pH dans le corps humain.
L'infographie ci-dessous résume les différences entre le carbonate de métal et le carbonate d'hydrogène métallique sous forme tabulaire.

Résumé - Carbonate de métal vs carbonate d'hydrogène métallique
Le carbonate métallique et l'hydrogène métallique carbonate sont des composés inorganiques. La principale différence entre le carbonate métallique et l'hydrogène métallique carbonate est que les carbonates métalliques contiennent des anions carbonatés tandis que les composés de carbonate d'hydrogène métallique contiennent des anions bicarbonate.
Référence:
1. "Bicarbonate." Encyclopædia Britannica, Encyclopædia Britannica, Inc., Disponible ici.
2. "Carbonate." Wikipédia, Fondation Wikimedia, 11 octobre. 2020, disponible ici.
Image gracieuseté:
1. «Carbonate-3D-balls» par Benjah-Bmm27 - Propre travaux (domaine public) via Commons Wikimedia
2. «Bicarbonate-ion-3d-balls» par Ben Mills et Jynto - recolour de fichier: nitric-acid-3d-balls-b.PNG (domaine public) via Commons Wikimedia


