Différence entre l'état liquide et l'état gazeux

Le différence clé entre l'état liquide et l'état gazeux est que le L'état liquide a des forces intermoléculaires plus fortes entre les molécules par rapport à l'état gazeux. En fait, l'état gazeux a moins ou pas de forces intermoléculaires.
Il existe trois principaux états ou phases de matière en phase gazeuse, phase liquide et phase solide. Ces états de matière ont de nombreuses différences entre eux, y compris l'apparence, les propriétés physiques et les propriétés chimiques. Ici, nous discuterons spécifiquement de la différence entre l'état liquide et l'état gazeux basé sur les propriétés caractéristiques de chacun.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que l'état liquide
3. Qu'est-ce que l'état gazeux
4. Comparaison côte à côte - état liquide vs état gazeux sous forme tabulaire
5. Résumé
Qu'est-ce que l'état liquide?
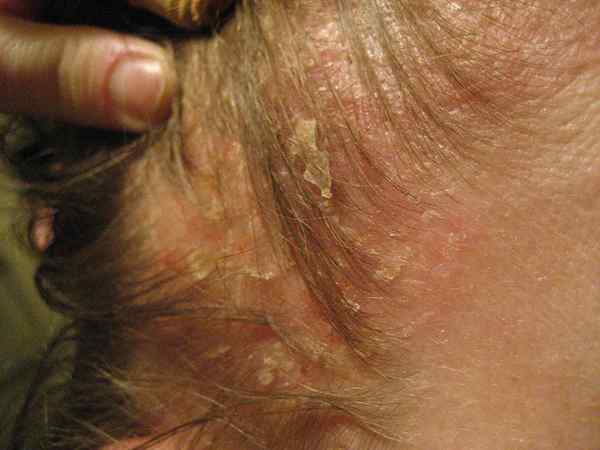
L'état liquide est un état ou une phase de matière qui a des forces intermoléculaires plus fortes entre les molécules que celles d'un gaz et de faibles forces intermoléculaires que celles d'un solide. Bien qu'il existe des forces intermoléculaires considérables, un liquide n'a pas de forme définie. Il obtient la forme du récipient dans lequel le liquide existe. Ceci, principalement parce que les forces intermoléculaires entre molécules ne sont pas assez fortes pour garder une forme définie. Cependant, un liquide a un volume définitif.

Figure 01: État liquide
Par rapport aux solides et aux gaz, les espaces intermoléculaires entre les molécules liquides sont modérés. Cependant, il existe des espaces intermoléculaires qui permettent aux molécules de se déplacer ici et là. De plus, la compressibilité d'un liquide est presque difficile. La disposition des molécules dans un liquide est aléatoire, et la molécule s'organise peu. En dehors de cela, un liquide peut passer d'un niveau supérieur à un niveau inférieur. En particulier, nous ne pouvons pas stocker un liquide sans conteneur. Lorsque vous envisagez le mouvement moléculaire, il existe un mouvement brownien dans un liquide.
Qu'est-ce que l'état gazeux?
L'état gazeux est un état ou une phase de matière qui a des forces intermoléculaires faibles ou pas entre les molécules que celle d'un liquide ou d'un solide. Un gaz n'a aucune forme; Il remplit tout le monde à l'intérieur du conteneur où il existe. De plus, il n'a pas de volume définitif. Aussi, contrairement aux liquides et aux solides, nous pouvons facilement comprimer les gaz.
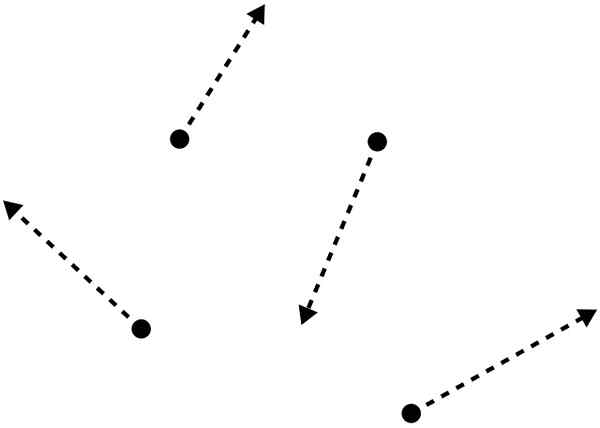
Figure 02: molécules à l'état gazeux
Lorsque l'on considère la disposition des molécules à l'état gazeux, les molécules s'organisent de manière aléatoire et plus peu que les liquides. Plus précisément, les substances à l'état gazeux ont une fluidité considérablement élevée, ce qui le permet de s'écouler dans toutes les directions. L'état gazeux montre des mouvements moléculaires libres et aléatoires. Cela est dû à la présence de grands espaces intermoléculaires entre les molécules. En particulier, les substances à l'état gazeux nécessitent des conteneurs fermés pour le stockage.
Quelle est la différence entre l'état liquide et l'état gazeux?
L'état liquide est un état ou une phase de matière qui a des forces intermoléculaires plus fortes entre les molécules que celles d'un gaz et des forces intermoléculaires faibles que celles d'un solide tandis que l'état gazeux est un état ou une phase de matière qui a des forces intermoléculaires faible celui d'un liquide ou d'un solide. C'est la principale différence entre l'état liquide et l'état gazeux.
Outre cette différence clé entre l'état liquide et l'état gazeux, il existe plusieurs différences entre les deux états de matière dans leur forme, leur volume, leur fluidité, leur mouvement moléculaire, sa compressibilité, etc. L'infographie ci-dessous résume plus en détail la différence entre l'état liquide et l'état gazeux.
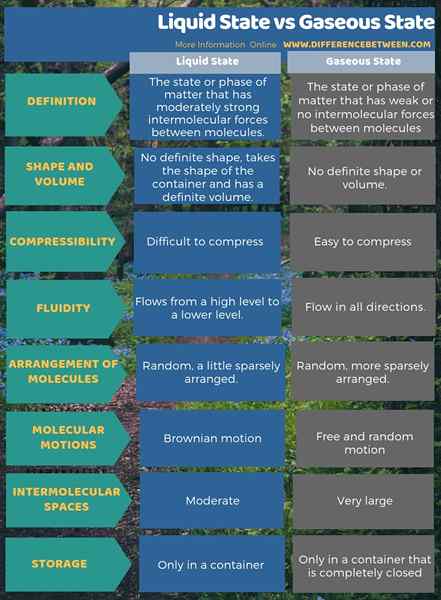
Résumé - État liquide vs état gazeux
Parmi les trois principaux états de la matière, nous avons discuté de l'état liquide et de l'État gazeux dans cet article. Résumer; La principale différence entre l'état liquide et l'état gazeux est que l'état liquide a des forces intermoléculaires plus fortes entre les molécules par rapport à l'état gazeux. Tandis que l'état gazeux a moins ou pas de forces intermoléculaires.
Référence:
1. "Gaz.»Wikipedia, Wikimedia Foundation, 9 octobre. 2018. Disponible ici
Image gracieuseté:
1."Drop d'eau 001" par José Manuel Suárez, (CC par 2.0) via Commons Wikimedia
2.«Mouvement des particules de gaz» par le travail de Closeapple (domaine public) via les communes Wikimedia