Différence entre la batterie d'acide de plomb et la batterie alcaline

Le différence clé entre la batterie d'acide de plomb et la batterie alcaline est que Les batteries à l'acide de plomb sont rechargeables tandis que les batteries alcalines sont principalement non recordables.
Une batterie est un appareil qui a une ou plusieurs cellules électrochimiques. Il a des connexions externes que nous pouvons nous connecter à des périphériques d'alimentation tels que les smartphones, les lampes de poche, etc. De plus, il a un terminal / cathode positif et une anode terminale négative. La batterie d'acide à plomb et la batterie alcaline sont deux de ces batteries qui peuvent fournir à ces appareils l'électricité requise.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que la batterie d'acide plomb
3. Qu'est-ce que la batterie alcaline
4. Comparaison côte à côte - batterie d'acide de plomb vs batterie alcaline sous forme tabulaire
5. Résumé
Qu'est-ce que la batterie d'acide plomb?
La batterie d'acide de plomb est l'une des premières batteries rechargeables et est toujours largement utilisée. Il a un rapport énergétique / poids très faible. De plus, il a un faible rapport énergie / volume. De plus, cette batterie est capable de fournir un courant de surtension élevé; Ainsi, il a un grand rapport puissance / poids. Ces batteries sont des appareils à faible coût.

Dans l'état complètement chargé de la batterie, sa plaque négative est plomb et la plaque positive est l'oxyde de plomb. Ici, nous utilisons de l'acide sulfurique concentré comme électrolyte. L'électrolyte stocke la majeure partie de l'énergie chimique. Cependant, lors de la charge, la surcharge entraînera la génération d'oxygène et de gaz hydrogène en raison de l'électrolyse de l'eau. C'est une perte pour la cellule.
Lors de la décharge de la batterie, les ions hydrogène se forment à la plaque négative et ces ions se déplacent vers une solution d'électrolyte et sont consommés à la plaque positive. HSO4- La consommation d'ions se produit dans les deux plaques. Pendant le processus de charge, l'inverse de ces réactions se produisent.
Dans l'état déchargé de la batterie, les plaques positives et négatives deviennent du sulfate de plomb (II). L'électrolyte perd la majeure partie de son acide sulfurique dissous et devient de l'eau. Un diagramme montrant l'état entièrement déchargé de la batterie d'acide de plomb est le suivant:

Figure 02: État déchargé
Qu'est-ce que la batterie alcaline?
La batterie alcaline est un type de batterie primaire, et son énergie est générée via la réaction entre le métal zinc et l'oxyde de manganèse. Le nom de batterie alcaline provient de son électrolyte alcalin: hydroxyde de potassium. Certaines de ces batteries sont rechargeables, mais la tentative de recharge de la batterie la rompre souvent.

Figure 03: Batterie alcaline rompue
Dans cette batterie, l'électrode négative est en métal de zinc et l'électrode positive est l'oxyde de manganèse (MNO2). Cependant, l'électrolyte alcalin ne participe pas à la réaction. Il reste inchangé car des quantités égales d'ions hydroxyde sont consommées et formées pendant la décharge. Ici, l'énergie chimique est stockée dans le métal de zinc.
Quelle est la différence entre la batterie d'acide de plomb et la batterie alcaline?
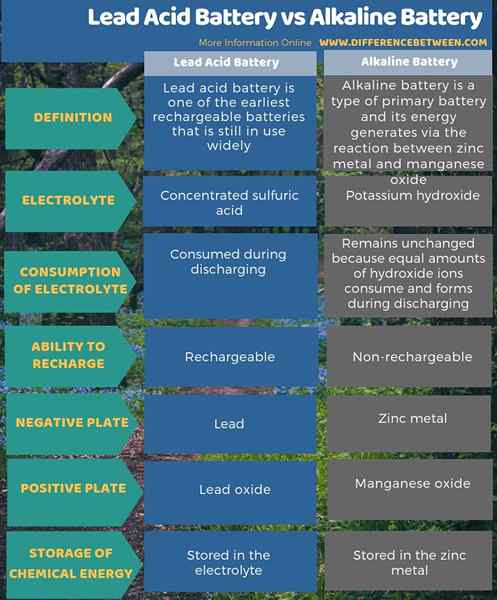
La batterie d'acide de plomb est l'une des premières batteries rechargeables encore largement utilisées. Pendant ce temps, la batterie alcaline est un type de batterie primaire, et son énergie est générée via la réaction entre le métal zinc et l'oxyde de manganèse. La principale différence entre la batterie d'acide de plomb et la batterie alcaline est que les batteries à l'acide de plomb sont rechargeables tandis que les batteries alcalines sont principalement non recordables.
De plus, la majeure partie de l'énergie chimique de la batterie est stockée dans l'électrolyte dans la batterie d'acide de plomb, mais dans les batteries alcalines, l'énergie est stockée dans le métal de zinc. Une autre différence entre la batterie d'acide de plomb et la batterie alcaline est que la batterie d'acide de plomb consomme l'électrolyte pendant la décharge, mais la batterie alcaline ne fait pas.
Résumé - Batterie d'acide en plomb vs batterie alcaline
La batterie d'acide de plomb est l'une des premières batteries rechargeables encore largement utilisées. Mais, la batterie alcaline est un type de batterie primaire, et son énergie génère via la réaction entre le métal zinc et l'oxyde de manganèse. La principale différence entre la batterie d'acide de plomb et la batterie alcaline est que les batteries à l'acide de plomb sont rechargeables tandis que les batteries alcalines sont principalement non recordables.
Référence:
1. "Batterie au plomb." Batteries au plomb, Disponible ici.
Image gracieuseté:
1. «Photo-Carbattery» par Shaddack supposé (basé sur les réclamations du droit d'auteur). - Aucune source lisible par machine fournie. Propre travail assumé (basé sur les réclamations du droit d'auteur) (domaine public) via Commons Wikimedia
2. «Déchargé» (CC par 3.0) via Commons Wikimedia
3. «BEAKEDBATTERY 2701A» par © Túrelio (via Wikimedia-Commons), 2009 (CC BY-SA 3.0 de) via Commons Wikimedia


