Différence entre l'hélium et l'oxygène

Différence clé - Helium vs oxygène
L'hélium et l'oxygène sont deux éléments chimiques dans le tableau périodique, bien qu'une différence significative puisse être observée entre eux en fonction de leurs propriétés chimiques. Ce sont les deux gaz à température ambiante; Mais, l'hélium est un gaz noble chimiquement inerte. Les propriétés chimiques de ces deux éléments sont complètement différentes les unes des autres. Par exemple; L'oxygène réagit rapidement avec de nombreux éléments et composés, alors que L'hélium ne réagit pas avec aucun. Cela peut être identifié comme le différence clé entre l'hélium et l'oxygène. Cependant, le comportement inerte de l'hélium a tant d'applications commerciales, et l'oxygène est également l'un des gaz les plus inestimables pour l'homme et les animaux.
Qu'est-ce que l'hélium?
L'hélium est le deuxième élément le plus abondant de l'univers, et c'est le deuxième élément le plus léger du tableau périodique. C'est un gaz monatomique insipide, inodore et incolore à température ambiante avec un faible point d'ébullition. L'hélium est le premier membre de la famille Noble Gas, et c'est l'élément le moins réactif. Il n'a que deux électrons fortement attirés par le noyau. De grandes quantités d'hélium sont naturellement produites dans les réactions de fusion productrices d'énergie dans les étoiles. La désintégration radioactive des minéraux produit également de l'hélium. De plus, les dépôts de gaz naturel contiennent également l'hélium gazeux.
L'hélium possède des propriétés inhabituelles; il devient un superfluide à des températures très basses. Un superfluide peut s'écouler contre la gravité. L'hélium a le point de fusion le plus bas de tous les autres éléments. C'est le seul élément qui ne peut pas être solidifié en abaissant la température.

Qu'est-ce que l'oxygène?
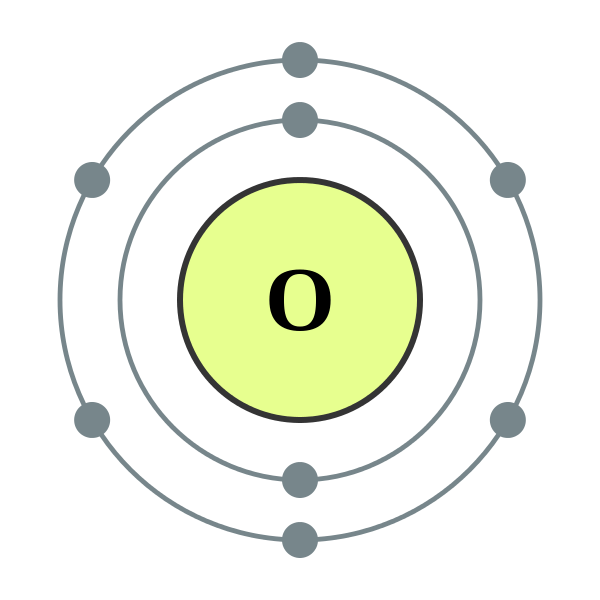
L'oxygène est un membre du groupe chalcogène (groupe VI A) dans le tabage périodiquee. C'est un gaz diatomique, hautement réactif, incolore, inodore. L'oxygène est le troisième élément le plus abondant de l'univers par la masse. Dans la plupart des réactions chimiques; L'oxygène agit comme un agent oxydant, mais il peut également réduire certains composés chimiques. L'oxygène a deux types d'allotropes; dioxygène (o2) et le trioxygène (o3), qui est appelé ozone.
Quelle est la différence entre l'hélium et l'oxygène?
Propriétés de l'hélium et de l'oxygène:
Réactivité:
Hélium:
L'hélium est un gaz inerte; C'est l'élément le moins réactif de la famille de gaz noble. En d'autres termes, l'hélium est complètement inerte, il ne réagit pas avec aucun autre élément.
Oxygène:
Par rapport à l'hélium, la réactivité chimique de l'oxygène est extrêmement élevée. Même s'il s'agit d'un gaz stable di-moléculaire à température ambiante, il réagit rapidement avec autant d'éléments et de composés. Cependant, l'oxygène ne réagit pas avec lui-même, l'azote, les acides, les bases et l'eau dans des conditions normales. L'oxygène peut agir à la fois comme agent oxydant et agent réducteur; Par conséquent, il montre tellement de réactions chimiques. Il a la deuxième valeur d'électronégativité la plus élevée (à côté du fluor) à partir d'autres éléments réactifs. La solubilité de l'oxygène dans l'eau dépend de la température.
États d'oxydation:
Hélium:
L'hélium ne montre pas plusieurs états d'oxydation. Il n'a qu'un seul état d'oxydation; c'est nul.
Oxygène:
L'état d'oxydation le plus courant de l'oxygène est -2. Mais, il est capable d'avoir des états d'oxydation de -2, -1, -1/2, 0, +1 et +2.
Isotopes:
Hélium:
Il existe deux types d'isotopes d'hélium naturels; Helium 3 (3Il) et de l'hélium 4 (4Il). L'abondance relative de 3Il est très bas par rapport à 4Il. Trois isotopes radioactifs de l'hélium ont été créés, mais ils n'ont aucune application commerciale.
Oxygène:
L'oxygène a quatre isotopes, mais seulement trois isotopes sont stables; ils sont 16O, 17O et18O. Le type le plus abondant est 16O, qui fait environ 99.762%.
Applications:
Hélium:
Le comportement chimiquement inerte de l'hélium possède un nombre nombreuses applications. Il est utilisé dans des recherches à basse température dans les systèmes de refroidissement, comme source de carburant dans les roquettes, dans le processus de soudage, dans les systèmes de détection de plomb, pour remplir des ballons et empêcher les objets de réagir avec l'oxygène.
Oxygène:
L'oxygène a de nombreuses utilisations dans notre vie quotidienne, à partir de la respiration; Les humains et les animaux ne peuvent pas vivre sans oxygène. Certains autres exemples incluent; pour produire des médicaments, des acides, en combustion, la purification de l'eau, le soudage et la fusion des métaux.
Image gracieuseté: 1. Electron Shell 002 Helium - No Label by Pumbaa (Original Work par Greg Robson) [CC BY-SA 2.0], via Wikimedia Commons 2. Coquille d'électrons 008 oxygène (non-métal diatomique) - pas d'étiquette par Depiep (propre travail) [CC BY-SA 3.0], via Wikimedia Commons

