Différence entre Gilman et Grignard Reagent
Le différence clé Entre Gilman et le réactif Grignard est que Le réactif Gilman est un réactif de cuivre et de lithium, tandis que le réactif Grignard est un réactif du magnésium.
Un réactif est une substance que nous pouvons ajouter à un mélange réactionnel afin de provoquer une réaction chimique ou de tester si une réaction chimique se produit dans un système particulier. Le réactif Gilman et le réactif Grignard sont ces deux types de substances.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que le réactif Gilman
3. Qu'est-ce que le réactif Grignard
4. Comparaison côte à côte - réactif Gilman vs Grignard sous forme tabulaire
5. Résumé
Qu'est-ce que le réactif Gilman?
Le réactif Gilman est un réactif des métaux de cuivre et de lithium. Par conséquent, nous pouvons le nommer en tant que substance diorganocopper. La formule chimique générale de cette substance est r2culi. Dans cette formule chimique, R est soit un alkyle ou un groupe aryle. Ce réactif est très utile car contrairement à certains autres réactifs métalliques, le réactif Gilman peut réagir avec des halogénures organiques pour remplacer le groupe halogénures par un groupe R. Ces types de réactions sont nommés comme des réactions Corey-House. Ces réactions de remplacement sont importantes dans la synthèse de produits complexes à partir de blocs de construction simples.

Figure 01: Structure générale d'un réactif Gilman
Ce réactif a été découvert par le scientifique Henry Gilman et ses collègues. Un réactif Gilman commun est le diméthylcopper au lithium ayant la formule chimique (CH3) 2culi. Nous pouvons préparer ce réactif via l'ajout d'iodure de cuivre (i) au méthyllithium en présence de tétrahydrofuran à des températures très basses. Le produit de cette réaction existe sous forme de dimère dans l'éther diéthylique, formant une structure annulaire à huit membres.
Qu'est-ce que le réactif Grignard?
Le réactif Grignard est un réactif contenant du magnésium métal. La formule chimique générale de cette substance est R-Mg-X. Dans cette formule, R fait référence à un groupe chimique organique, Mg fait référence au magnésium et X fait référence à un halogène. Généralement, le groupe R dans ce réactif est soit un alkyle ou un groupe aryle. Il existe deux exemples typiques pour le réactif Grignard; chlorure de méthylmagnésium et bromure de phénylmagnésium.
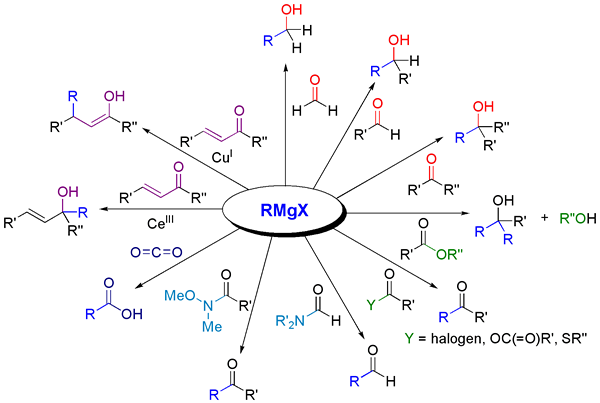
Dans les réactions de synthèse organique, les réactifs Grignard sont des substances populaires. Ces réactifs sont utiles pour créer de nouvelles liaisons carbone-carbone. E.g. Dans la réaction entre le composé halogéné R'-X 'et le réactif Grignard en présence d'un catalyseur approprié, le produit final est R-R' et le sous-produit de la réaction est Mgxx '.

Figure 02: Réactions entre le réactif Grignard et les composés carbonyle
De plus, les réactifs purs de Grignard sont des substances solides extrêmement réactives. Par conséquent, nous devons gérer ces substances en tant que solutions dans des solvants tels que l'éther diéthylique ou le THF. Ces réactifs sont stables pendant un certain temps si l'eau est exclue de la solution.
Quelle est la différence entre le réactif Gilman et Grignard?
La principale différence entre Gilman et le réactif Grignard est que le réactif Gilman est un réactif de cuivre et de lithium alors que le réactif Grignard est un réactif du magnésium. De plus, les réactifs Gilman se produisent à l'état liquide tandis que les réactifs de Grignard, lorsqu'ils sont purs, se produisent dans l'état solide.
L'infographie suivante résume la différence entre Gilman et le réactif Grignard.
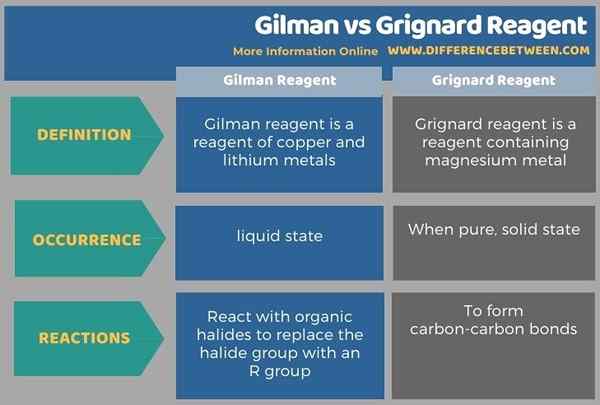
Résumé - Réactif Gilman vs Grignard
Un réactif est une substance que nous pouvons ajouter à un mélange réactionnel afin de provoquer une réaction chimique ou de tester si une réaction chimique se produit dans un système particulier. La principale différence entre Gilman et le réactif Grignard est que le réactif Gilman est un réactif de cuivre et de lithium alors que le réactif Grignard est un réactif du magnésium.
Référence:
1. Carey, F. (2008, 22 juillet). Réactif Gilman. Encyclopédie Britannica. Récupéré le 07 octobre 2020, disponible ici.
2. Réactif Gilman. Wikipédia. (2020, 29 août). Récupéré le 07 octobre 2020, disponible ici.
Image gracieuseté:
1. «Gilman Reagent2» par Sidar à l'anglais Wikipedia - transféré de EN.wikipedia aux communes par t.Vanschaik utilisant CommonShelper. (Domaine public) via Commons Wikimedia
2. «Grignard with Carbony» de Calvero. - Propre travail, fait avec ChemDraw (domaine public) via Commons Wikimedia


