Différence entre les diastéréomères et les énantiomères
Le différence clé entre les diastéréomères et les énantiomères Les diastéréomères d'une molécule ne sont pas des images miroir les uns des autres tandis que les énantiomères sont des images miroir les unes des autres.
Il peut y avoir plusieurs formules structurelles pour une seule formule moléculaire. Ceux-ci sont appelés isomères. Nous pouvons définir les isomères comme «différents composés qui ont la même formule moléculaire."Il existe principalement deux types d'isomères: les isomères constitutionnels et les stéréoisomères. Les diastéréomères et les énantiomères sont les deux types de stéréoisomères.
CONTENU
1. Aperçu et différence clé
2. Quels sont les diastéréomères
3. Que sont les énantiomères
4. Comparaison côte à côte - diastéréomères vs énantiomères sous forme tabulaire
5. Résumé
Quels sont les diastéréomères?
Les diastéréomères sont des stéréoisomères dont les molécules ne sont pas des images miroir les unes des autres. Par exemple, les IC et les isomères trans sont des diastéréomères. Ici, la connectivité des atomes est la même.

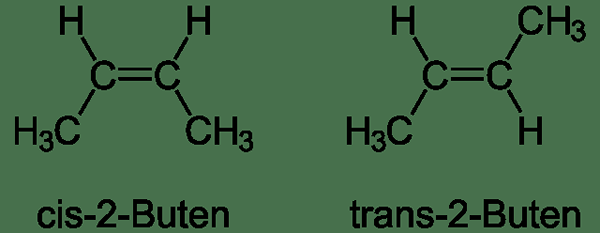
Figure 01: Diastéréomères
Dans l'exemple ci-dessus, les deux composés ont une double liaison carbone-carbone. Pour chaque carbone, un groupe méthyle et un atome d'hydrogène sont connectés. Les cis et les molécules trans ne diffèrent que de la façon dont les atomes sont disposés dans l'espace. Autrement dit, dans CIS Isomer, les deux hydrogènes sont du même côté de la double liaison carbone. Cependant, dans l'isomère trans, les atomes d'hydrogène sont de chaque côté de la double liaison carbone. De plus, les deux structures ne sont pas des images miroir les unes des autres. Par conséquent, ce sont des diastéréomères. Cependant, les CIS et les molécules trans ne sont pas le seul type de diastéréomères que nous pouvons trouver.
Que sont les énantiomères?
Les énantiomères sont des stéréoisomères dont les molécules sont des images miroir non superprimables les unes des autres. Les énantiomères ne sont possibles qu'avec des molécules chirales. Une molécule chirale est une molécule qui n'est pas identique à son image miroir. Pour qu'une molécule soit chirale, elle devrait avoir un atome de carbone tétraédrique avec quatre groupes différents qui y sont attachés. Cet atome de carbone est connu comme un stéréocentre. Les molécules chirales font des images miroir qui ne sont pas superposables. Ainsi, la molécule et l'image miroir sont des énantiomères les uns des autres. Voici un exemple de composé qui forme des énantiomères.
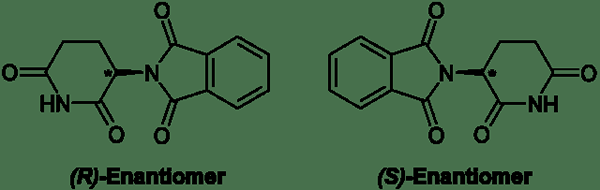
Figure 02: Énantiomères
Nous nommons généralement des énantiomères en utilisant le système R et S. Les énantiomères n'ont pas de points d'ébullition différents, des points de fusion, des solubilités, différents spectres infrarouges, etc. Toutes ces propriétés chimiques et physiques des énantiomères sont similaires car les forces intermoléculaires sont similaires dans les deux isomères. Ils ne se séparent que par leurs différents comportements vers la lumière polarisée par le plan. C'est-à-dire que les énantiomères tournent le plan de la lumière polarisée plane dans des directions opposées. Cependant, ils tournent la lumière en quantités égales. En raison de leur effet sur la lumière polarisée, les énantiomères sont optiquement actifs. Le mélange équimolaire de deux énantiomères est un mélange racémique. Un mélange racémique ne montre aucune rotation de la lumière polarisée; Par conséquent, il est optiquement inactif.
Quelle est la différence entre les diastéréomères et les énantiomères?
La principale différence entre les diastéréomères et les énantiomères est que les diastéréomères d'une molécule ne sont pas des images miroir les uns des autres tandis que les énantiomères sont des images miroir. Les molécules avec plus d'un stéréocentre peuvent être des diastéréomères s'ils ne sont pas des images miroir les uns des autres. Cependant, s'il n'y a qu'un seul stéréocentre, alors cette molécule a des énantiomères. Les diastéréomères ont des propriétés physiques et chimiques différentes. Mais les énantiomères ont des propriétés physiques et chimiques similaires à l'exception de leurs différentes propriétés optiques vers la lumière polarisée en plan.

Résumé - Diastéréomères vs énantiomères
Les diastéréomères et les énantiomères sont les deux types de stéréoisomères. La principale différence entre les diastéréomères et les énantiomères est que les diastéréomères d'une molécule ne sont pas des images miroir les unes des autres, mais les énantiomères sont des images miroir.
Référence:
1. Helmenstine, Anne Marie. «Définition de l'énantiomère.”Thoughtco, dec. 5, 2018, disponible ici.
Image gracieuseté:
1. «CIS-Trans-2-Buten» par Neurotiker - Propre travaux (domaine public) via Commons Wikimedia
2. «Thalidomide-Enantiomers» de Klaus Hoffmeier - Propre travaux (domaine public) via Commons Wikimedia


