Différence entre la liaison covalente et la liaison dative
Le différence clé entre la liaison covalente et la liaison dative est que le La liaison covalente se forme lorsque des électrons non appariés de deux atomes s'associent les uns aux autres alors que la liaison dative se forme lorsqu'un atome donne l'une de ses paires d'électrons à un autre atome.
Bien que la liaison dative ressemble à une liaison covalente, ils sont différents les uns des autres lorsque nous considérons la formation de la liaison. Mais il n'y a pas de différence entre la liaison covalente et la liaison dative après sa formation. Par conséquent, nous appelons généralement la liaison dative une obligation covalente, ce qui n'est pas faux.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que la liaison covalente
3. Qu'est-ce que le lien datif
4. Comparaison côte à côte - liaison covalente vs liaison dative sous forme tabulaire
5. Résumé
Qu'est-ce que la liaison covalente?
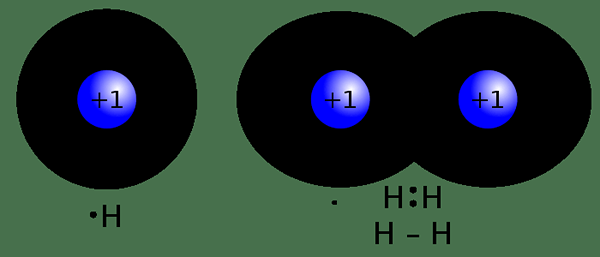
Une liaison covalente est une forme de liaison chimique qui se forme lorsque deux atomes partagent une paire d'électrons. Nous l'appelons une «liaison moléculaire». Les électrons qui sont partagés sont des «paires partagées» ou des «paires de liaison». Une liaison covalente formée en raison de l'équilibre stable des forces attractives et répulsives entre les atomes lorsqu'ils partagent des électrons. Ce partage d'électrons permet à chaque atome d'avoir l'équivalent d'une coque extérieure complète. Ce type de liaison se forme entre deux atomes non métalliques ayant des valeurs d'électronégativité presque similaires ou entre un électron et un ion métallique chargé positivement.

Figure 01: Formation d'une liaison covalente entre deux atomes d'hydrogène
Les obligations covalentes sont principalement de deux types; Ce sont des liaisons polaires et des liaisons non polaires. Les liaisons polaires existent entre deux atomes avec une différence entre leurs valeurs d'électronégativité dans la plage de 0.4 à 1.7. Une liaison non polaire se forme si cette différence est inférieure à 0.4. En effet, une différence élevée entre les valeurs de l'électronégativité signifie, un atome (ayant la valeur d'électronégativité plus élevée) attire les électrons plus que l'autre atome, ce qui fait la liaison, polaire.
Il existe trois principaux types de liaisons covalentes en fonction du nombre de paires d'électrons qui sont partagées entre deux atomes. Ce sont des liaisons simples qui impliquent une paire d'électrons, des liaisons doubles qui impliquent deux paires d'électrons et une triple liaison qui implique trois paires d'électrons.
Qu'est-ce que le lien datif?
Une liaison dative est un type de liaison covalente qui se forme lorsqu'un atome donne sa paire d'électrons à un autre atome. Après la formation de la liaison, il ressemble exactement à une liaison covalente. C'est parce que les deux atomes partagent la même paire d'électrons que la paire de liaisons.
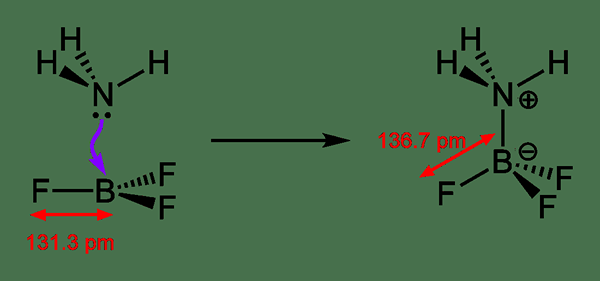
Figure 02: Formation d'un lien datif
Les synonymes pour cette liaison sont une «liaison dipolaire» et une «liaison coordonnée». L'exemple le plus courant est les liaisons dans les complexes de coordination. Là, les ions métalliques se lient aux ligands via ces liaisons de coordonnées.
Quelle est la différence entre la liaison covalente et la liaison dative?
Une liaison covalente est une forme de liaison chimique qui se forme lorsque deux atomes partagent une paire d'électrons. Une liaison dative est un type de liaison covalente qui se forme lorsqu'un atome donne sa paire d'électrons à un autre atome. Ils diffèrent les uns des autres en fonction de la façon dont ils se forment. Par conséquent, la principale différence entre la liaison covalente et la liaison dative est qu'une liaison covalente se forme lorsque des électrons non appariés de deux atomes s'associent l'un à l'autre tandis que la liaison dative se forme lorsqu'un atome donne l'une de ses paires d'électrons à un autre atome.
L'infographie ci-dessous présente la différence entre la liaison covalente et la liaison dative sous forme tabulaire.
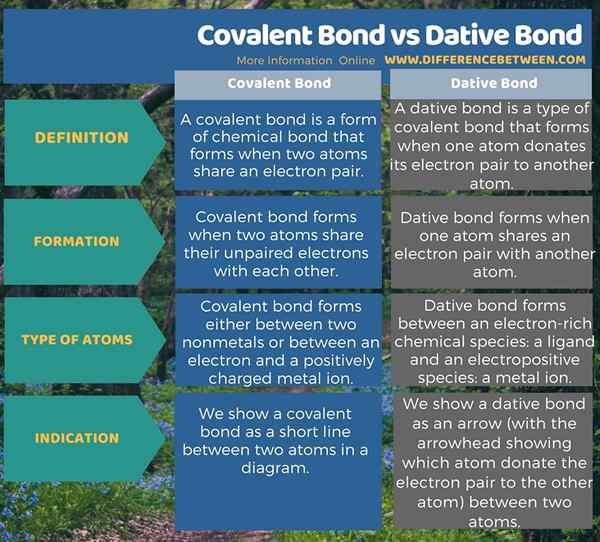
Résumé - Obligation covalente vs liaison dative
Après la formation de la liaison, la liaison covalente et la liaison dative semblent similaires. Cependant, ils diffèrent les uns des autres en fonction de la façon dont ils se forment. La différence entre la liaison covalente et la liaison dative est qu'une liaison covalente se forme lorsque des électrons non appariés de deux atomes s'associent les uns aux autres alors que la liaison dative se forme lorsqu'un atome donne l'une de ses paires d'électrons à un autre atome.
Référence:
1. Helmenstine, Anne Marie, Ph.D. «Définition des obligations covalentes.”Thoughtco, Jun. 22, 2018. Disponible ici
2. Helmenstine, Anne Marie, Ph.D. «Définition des obligations datives (obligation coordonnée).”Thoughtco, Jun. 22, 2018. Disponible ici
Image gracieuseté:
1.«Hydrogène de liaison covalente» par Jacek FH - Propre travaux, (CC BY-SA 3.0) via Commons Wikimedia
2.«NH3-BF3-adduct-lingening-2d» par Ben Mills - propre travail, (domaine public) via Commons Wikimedia


