Différence entre BCC et FCC
Différence clé - BCC VS FCC
Les termes BCC et FCC sont utilisés pour nommer deux arrangements différents de structures cristallines. BCC représente structure cubique centrée sur le corps Alors que la FCC représente Structure cubique centrée sur le visage. Ce sont des formes de réseaux cubes. Par conséquent, ces arrangements ont des sphères (atomes, molécules ou ions à partir desquels le réseau est fait) organisé en structures cubes. La cellule unitaire de BCC a des sphères dans les coins d'un cube et une sphère au centre du cube. Puisqu'il y a huit coins dans un cube, le nombre total de sphères présents dans une cellule unitaire BCC est 9. La cellule unitaire de la FCC a des sphères dans chaque coin d'un cube et aussi au centre de chaque visage cube. Ensuite, la cellule unitaire de FCC a 12 sphères. Le différence clé Entre BCC et FCC est que Le nombre de coordination de BCC est de 8 tandis que le numéro de coordination de FCC est 12.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que BCC
3. Qu'est-ce que la FCC
4. Similitudes entre BCC et FCC
5. Comparaison côte à côte - BCC vs FCC sous forme tabulaire
6. Résumé
Qu'est-ce que BCC?
Le terme BCC représente la disposition cubique centrée sur le corps des sphères (atomes, molécule ou ions à partir desquels le réseau est fait). Dans cet arrangement, les sphères sont situées dans chaque coin d'un cube et une sphère au milieu du cube. Une cellule unitaire d'un réseau est la plus petite unité qui ressemble à toute la structure du réseau. Puisqu'un cube a 8 coins, il y a un total de 9 sphères dans une structure BCC (huit dans les coins plus au milieu).
Cependant, chaque sphère dans le coin de la cellule unitaire de BCC est membre de la cellule unitaire voisine. C'est parce que le réseau est composé de nombreuses cellules unitaires emballées ensemble. Puisqu'il y a 8 sphères dans une cellule unitaire qui sont les coins d'autres cellules unitaires, le nombre de coordination de la structure BCC est connu pour être 8. Ensuite, lorsqu'elle est considérée comme le total net des sphères dans une cellule unitaire BCC, il a 2 sphères car un coin en a 1/8e des sphères. Les huit coins forment ensemble une sphère, et il y a une sphère au milieu, ainsi que des résultats dans deux sphères.

Figure 01: Structure BCC
L'emballage des sphères dans la disposition BCC n'est pas serré. Cela signifie que l'emballage des sphères en BCC n'est pas un emballage étroit comme dans la FCC (cubique centrée sur le visage) ou HCP (emballage de fermeture hexagonale). Le facteur d'emballage de BCC est 0.68. Le facteur d'emballage est le volume de sphères par le volume de la cellule unitaire. Des exemples de métaux qui ont la structure BCC comprennent le lithium (LI), le sodium (NA), le potassium (K), le chrome (CR) et le baryum (BA).
Qu'est-ce que la FCC?
Le terme FCC signifie la disposition cubique centrée sur le visage des sphères. Dans cette disposition, les sphères sont situées dans chaque coin d'un cube (cellule unitaire) et dans les centres de chaque visage cube. Ici aussi, chaque sphère dans les coins est membre de la cellule unitaire voisine. En dehors de cela, chaque sphère au centre de la face cubique est partagée avec la cellule unitaire adjacente.
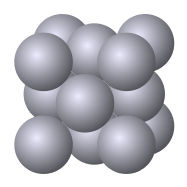
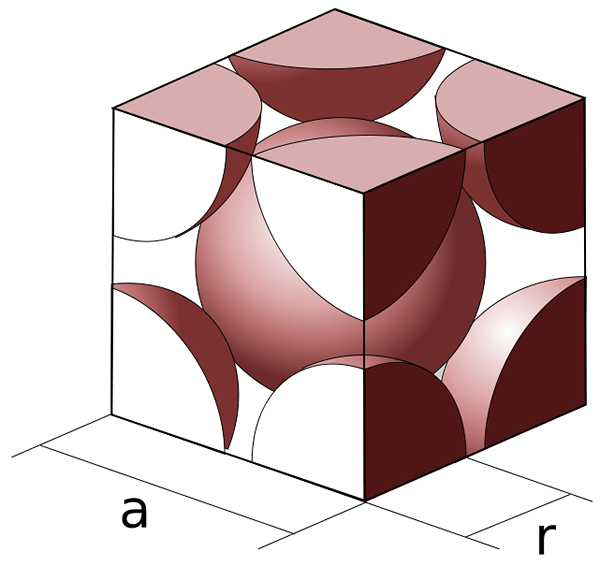
Figure 2: Structure FCC
Le numéro de coordination de la FCC est 12. C'est parce qu'il y a 12 sphères par cellule unitaire qui sont partagées avec d'autres cellules unitaires. Le total net des sphères présents dans la cellule unitaire FCC est 4. Il peut être calculé comme suit.
Sphères totales dans les coins = (1/8) x 8 = 1
Sphères totales dans les faces cubes = (1/2) x 6 = 3
Alors les sphères totales par cellule unitaire = 1 + 3 = 4
La structure FCC a plus d'emballage des sphères que celle de BCC (le pack de sphères plus près). Le facteur d'emballage de la structure FCC est 0.74. Cela signifie que le rapport entre le volume occupé par les sphères et le volume total de la cellule unitaire est 0.74. Quelques exemples de métaux ayant une structure FCC sont l'aluminium (AL), le cuivre (Cu), l'or (Au), le plomb (PB) et le nickel (NI).
Quelles sont les similitudes entre BCC et FCC?
- BCC et FCC sont des formes de disposition des réseaux cubes.
- La cellule unitaire des structures BCC et FCC est un cube.
Quelle est la différence entre BCC et FCC?
BCC vs FCC | |
| Le terme BCC représente la disposition cubique centrée sur le corps des sphères (atomes, molécule ou ions à partir desquels le réseau est fait). | Le terme FCC signifie la disposition cubique centrée sur le visage des sphères. |
| Arrangement des sphères | |
| BCC a des sphères dans les huit coins d'un cube et une sphère au centre du cube. | La FCC a des sphères dans les huit coins d'un cube et aussi dans les centres des visages cubiques. |
| Numéro de coordination | |
| Le numéro de coordination de la structure BCC est 8. | Le numéro de coordination de la structure FCC est 12. |
| Facteur d'emballage | |
| Le facteur d'emballage de BCC est 0.68 | Le facteur d'emballage de la FCC est 0.74 |
| Nombre de sphères dans une cellule unitaire | |
| Une cellule unitaire de BCC a un total net de 2 sphères. | Une cellule unitaire de FCC a un total net de 4 sphères. |
| Exemples | |
| Certains exemples de métaux qui ont la structure BCC comprennent le lithium (LI), le sodium (NA), le potassium (K), le chrome (CR) et le baryum (BA). | Quelques exemples de métaux ayant une structure FCC sont l'aluminium (AL), le cuivre (Cu), l'or (Au), le plomb (PB) et le nickel (NI). |
Résumé - BCC VS FCC
BCC signifie la disposition cubique centrée sur le corps. La FCC signifie la disposition cubique centrée sur le visage. Ces dispositions sont utilisées pour décrire l'emplacement des atomes, des molécules ou des ions et les espaces vides présents dans une structure de réseau. La différence entre BCC et FCC est que le nombre de coordination de BCC est 8 tandis que le nombre de coordination de FCC est 12.
Référence:
1.Structures cristallines métalliques primaires. Disponible ici
2.«FCC et BCC.”Bindt. Disponible ici
Image gracieuseté:
1.'CCC Crystal Cell (Opaque)' par Daniele Pugliesi (CC BY-SA 3.0) via Commons Wikimedia
2.«FCC Crystal Structure» User: arte - propre travail, (domaine public) via Commons Wikimedia


