Différence entre l'argon et l'oxygène
Différence clé - Argon VS. Oxygène
L'argon et l'oxygène sont deux éléments chimiques dans le tableau périodique. Ce sont tous deux des éléments gazeux, où l'argon se trouve dans la famille de gaz noble et l'oxygène provient du groupe de chalcogène dans le tableau périodique. L'argon est un gaz inerte alors que l'oxygène est un gaz très réactif. L'oxygène est l'un des éléments les plus abondants de cette planète tandis que l'argon est l'un des gaz nobles les plus abondants. L'argon est produit lorsque l'oxygène de haute pureté est fabriqué. Ils ont des points d'ébullition relativement proches, mais leurs propriétés chimiques sont très différentes les unes des autres. Comme vous pouvez observer les différences entre l'argon et l'oxygène sont nombreux. Cet article tente de vous fournir une compréhension clarifiée des différences.
Qu'est-ce que l'argon?
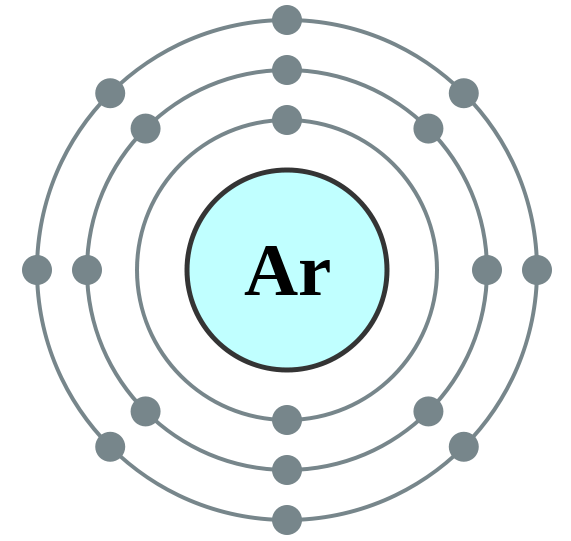
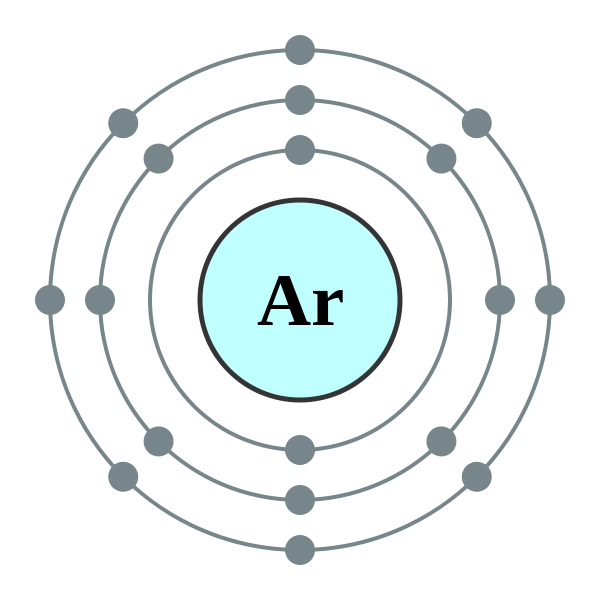
Argon (AR) est un membre d'une famille spéciale; Ils sont appelés gaz «rares», «nobles» ou «inertes». Tous les gaz de cette famille ont une coquille la plus externe totalement remplie et leur réactivité chimique est presque nulle. L'argon est un gaz monatomique, incolore, inodore, insipide et non toxique. L'argon est légèrement soluble dans l'eau. Son abondance dans l'atmosphère est de près de 0.934% en volume. L'argon est considéré comme le gaz inerte le plus abondant. Tous les membres de la famille de gaz Noble émettent de la lumière lorsqu'ils sont électriques excités; Dans ce cas, Argon produit une lumière bleu pâle-violet.
Qu'est-ce que l'oxygène?
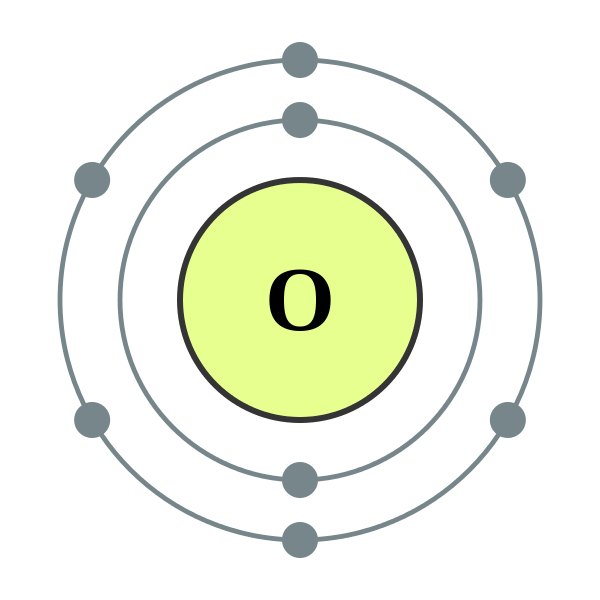
L'oxygène peut être considéré comme L'un des éléments les plus abondants de la terre. Environ 21% de l'oxygène élémentaire libre est présent dans notre atmosphère. De plus, il est combiné avec d'autres composés tels que l'eau et les minéraux. Même notre corps humain fonctionne en utilisant de l'oxygène et il contient 65% d'oxygène par masse. L'oxygène se produit naturellement sous forme de molécules gazeuses diatomiques, o2 (g). C'est un gaz incolore, insipide et inodore avec ses propriétés chimiques et physiques uniques. La densité de l'oxygène est supérieure à l'air et a une très faible solubilité dans l'eau.
La réactivité chimique de l'oxygène est très élevée; Il réagit avec presque tous les éléments dans différentes conditions, à l'exception des gaz nobles et certains des métaux moins réactifs. L'oxygène est l'élément le plus réactif à côté du fluor (F).
Quelle est la différence entre l'argon et l'oxygène?
Propriétés:
| Propriété | Argon | Oxygène |
| Numéro atomique | 18 | 8 |
| Configuration électronique | 1s² 2S² 2P63S² 3P⁶ | 1S² 2S² 2P⁴ |
| Point d'ébullition | -185.9 ° C (-302.6 ° F) | -182 ° C (-297 ° F) |
| Point de fusion | -189 ° C (-308 ° F) | -218 ° C (-361 ° F) |
Lourdeur:
Argon: L'argon est 1.4 fois aussi lourd que l'air; Il n'est pas respirant comme de l'oxygène et peut provoquer le suffocation en se réglant dans les parties inférieures sur les poumons.
Oxygène: L'oxygène est également plus dense que l'air, mais c'est un gaz léger qui est respirant.
Les usages:
Argon: L'argon est un gaz inerte même à des températures élevées, et pour cette raison, il est utilisé dans certains processus industriels critiques comme dans la fabrication d'acier inoxydable de haute qualité et dans la production de cristaux de silicium sans impureté pour les semi-conducteurs. Il est largement utilisé comme gaz de remplissage inerte dans les ampoules. Il reste non réactif même lorsque l'ampoule est chauffée à des températures élevées.
Oxygène: L'oxygène est largement utilisé dans l'industrie métallique avec de l'acétylène et d'autres gaz carburants pour la coupe, le soudage, la fusion, le durcissement, l'écran et le nettoyage. L'air enrichi d'oxygène gazeux ou d'oxygène est utilisé dans la fabrication en acier et en fer, dans le processus de raffinage chimique et de chauffage pour éliminer le carbone et dans la réaction d'oxydation.
L'industrie du pétrole utilise également largement l'oxygène comme alimentation pour réagir avec les hydrocarbures pour produire des produits chimiques tels que les aldéhydes et les alcools.
Image gracieuseté:
1. Electron Shell 018 Argon - No Label by Commons: User: Pumbaa (Original Work by Commons: User: Greg Robson) [CC BY-SA 2.0], via Wikimedia Commons
2. Coquille d'électrons 008 oxygène (non-métal diatomique) - pas d'étiquette par Depiep (propre travail) [CC BY-SA 3.0], via Wikimedia Commons


