Différence entre la solution aqueuse et non aqueuse
Le différence clé entre une solution aqueuse et non aqueuse est que le Le solvant d'une solution aqueuse est de l'eau alors que, dans des solutions non aqueuses, le solvant est une substance autre que l'eau.
Une solution contient un solvant et des solutés (s). Les solutés sont dissous dans le solvant. Ici, les solutés et le solvant devraient avoir la même polarité. De plus, si le solvant est polaire et que les solutés sont non polaires ou vice versa, les solutés ne se dissolveront pas dans le solvant, et nous ne pouvons pas obtenir de solution.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que la solution aqueuse
3. Quelle est la solution non aqueuse
4. Comparaison côte à côte - solution aqueuse vs non aqueuse sous forme tabulaire
5. Résumé
Qu'est-ce qu'une solution aqueuse?
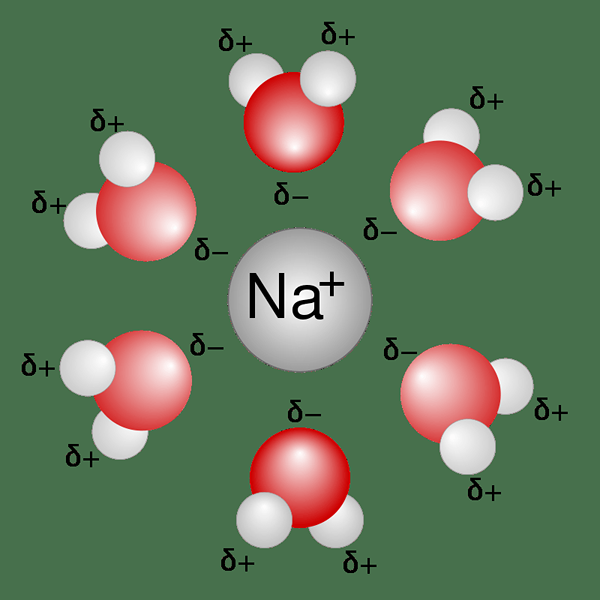
Une solution aqueuse est toute solution qui contient de l'eau comme solvant. Ici, les solutés doivent être hydrophiles et polaires pour se dissoudre dans l'eau pour donner une solution aqueuse. Bien que nous nommez l'eau comme solvant universel, nous ne pouvons pas dissoudre presque tout ce qu'il y a. Par exemple, nous ne pouvons pas dissoudre les graisses dans l'eau, il n'y a donc pas de solutions de graisse aqueuses nulle part.

Figure 01: ions sodium dans l'eau
Lors de l'écriture d'une équation chimique, nous utilisons le symbole (aq) comme indice pour indiquer que la substance est dans une solution aqueuse. Si le soluté peut se dissocier en ions lors de la dissolution dans l'eau, nous disons que la solution aqueuse est conductrice car elle peut conduire de l'électricité par la solution en raison de la présence d'ions.
Quelle est la solution non aqueuse?
Une solution non aqueuse est une solution que nous obtenons en dissolvant un soluté dans n'importe quel solvant autre que l'eau. Le solvant peut être un composé organique comme l'acétone, le toluène, l'éther, l'alcool, le benzène, etc.

Figure 02: iode dans l'alcool
Le solvant peut être polaire ou non polaire et en fonction de la polarité pendant que les solutés se dissolvent dans le solvant. Les solutions d'iode dans l'alcool et les solutions d'iode dans le tétrachlorure de carbone sont des exemples de solutions non aqueuses.
Quelle est la différence entre la solution aqueuse et non aqueuse?
Nous pouvons diviser les solutions en deux groupes comme aqueux et non aqueux en fonction du solvant. La principale différence entre la solution aqueuse et non aqueuse est que le solvant d'une solution aqueuse est l'eau, tandis que, dans des solutions non aqueuses, le solvant est une substance autre que l'eau. Solutions aqueuses de chlorure de sodium, d'ammoniac aqueux, etc. sont des exemples de solutions aqueuses lors des solutions d'iode dans l'alcool, des solutions d'iode dans le tétrachlorure de carbone, etc. sont des solutions non aqueuses.

Résumé - Solution aqueuse vs non aqueuse
Fondamentalement, nous pouvons diviser les solutions en deux groupes comme aqueux et non aqueux en fonction du solvant. La principale différence entre la solution aqueuse et non aqueuse est que le solvant d'une solution aqueuse est l'eau alors que, dans des solutions non aqueuses, le solvant est une substance autre que l'eau.
Référence:
1. Helmenstine, Anne Marie. «Définition de la solution aqueuse en chimie."Thoughtco, Jan. 13, 2019, disponible ici.
Image gracieuseté:
1. «Na + H2O» par Taxman - (Domaine public) via Commons Wikimedia
2. "J Crow's Lugol's Iodine 2" par Amin - Propre travaux (CC BY-SA 4.0) via Commons Wikimedia


