Différence entre l'aldéhyde et la cétone
Le différence clé entre l'aldéhyde et la cétone est que Le groupe fonctionnel d'un aldéhyde se produit toujours à un terminus tandis que le groupe fonctionnel d'une cétone se produit toujours au milieu d'une molécule.
Les aldéhydes et les cétones sont des molécules organiques avec un groupe carbonyle. Dans un groupe carbonyle, l'atome de carbone a une double liaison à l'oxygène. L'atome de carbonyle carboné est sp2 hybridé. Ainsi, les aldéhydes et les cétones ont un arrangement plan trigonal autour de l'atome de carbonyle carboné. Le groupe carbonyle est un groupe polaire; Ainsi, les aldéhydes et les cétones ont des points d'ébullition plus élevés par rapport aux hydrocarbures ayant le même poids. Cependant, ceux-ci ne peuvent pas créer des liaisons hydrogène plus fortes comme les alcools; Par conséquent, ils ont des points d'ébullition inférieurs que les alcools correspondants. En raison de la capacité de formation de liaisons hydrogène, les aldéhydes et les cétones à faible poids moléculaire sont solubles dans l'eau. Mais lorsque le poids moléculaire augmente, ils deviennent hydrophobes.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que l'aldéhyde
3. Qu'est-ce que le cétone
4. Comparaison côte à côte - aldéhyde vs cétone sous forme tabulaire
5. Résumé
Qu'est-ce que l'aldéhyde?
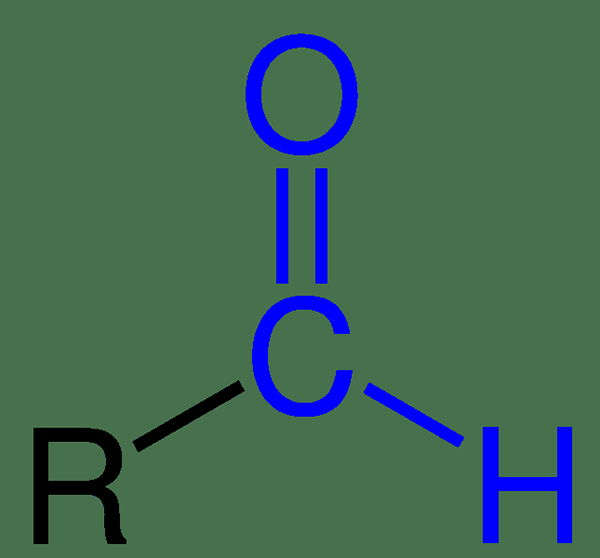
L'aldéhyde a un groupe carbonyle. Ce groupe carbonyle se lie à un autre carbone d'un côté, et de l'autre extrémité, il se connecte avec un atome d'hydrogène. Par conséquent, nous pouvons caractériser les aldéhydes avec le groupe -cho. L'aldéhyde le plus simple est le formaldéhyde. Cependant, cette molécule s'écarte de la formule générale en ayant un atome d'hydrogène au lieu du groupe R.
Dans la nomenclature de l'aldéhyde, selon le système IUPAC, nous utilisons le terme «Al» pour désigner un aldéhyde. Pour les aldéhydes aliphatiques, le «E» de l'alcane correspondant est remplacé par «Al». Par exemple, nous nommons ch3Cho comme éthanal, et ch3Ch2Cho est nommé propanal.

Figure 01: Structure chimique des aldéhydes
Pour les aldéhydes avec des systèmes d'anneau où le groupe aldéhyde se fixe directement à l'anneau, nous utilisons le terme «carbaldehyde» comme suffixe pour les nommer. Cependant, nous nommons le composé C6H6Cho communément comme benzaldéhyde plutôt que d'utiliser du benzenecarbaldéhyde. Nous pouvons synthétiser les aldéhydes par diverses méthodes. Une méthode est en oxydant les alcools primaires. De plus, nous pouvons synthétiser les aldéhydes en réduisant les esters, les nitriles et les chlorures d'acyle.
Qu'est-ce que le cétone?
Dans une cétone, le groupe carbonyle se produit entre deux atomes de carbone. Nous utilisons le suffixe «un» dans la nomenclature de la cétone. Au lieu de «-e» de l'alcane correspondant, nous utilisons le terme «un». De plus, nous comptons la chaîne aliphatique d'une manière qui donne au carbone carbonyle le numéro le plus bas possible. Par exemple, nous nommons le composé ch3Coch2Ch2Ch3 Comme 2-pentanone.

Figure 02: Structure chimique des cétones
De plus, nous pouvons synthétiser des cétones via l'oxydation des alcools secondaires, via l'ozonolyse des alcènes, etc. En dehors de cela, les cétones ont la capacité de subir un tautomérisme kéto-énol. Ce processus se produit, lorsqu'une base forte occupe le α-hydrogène (hydrogène attaché au carbone, qui est à côté du groupe carbonyle). La capacité de libérer l'α-hydrogène rend les cétones plus acides que les alcanes correspondants.
Quelle est la différence entre l'aldéhyde et la cétone?
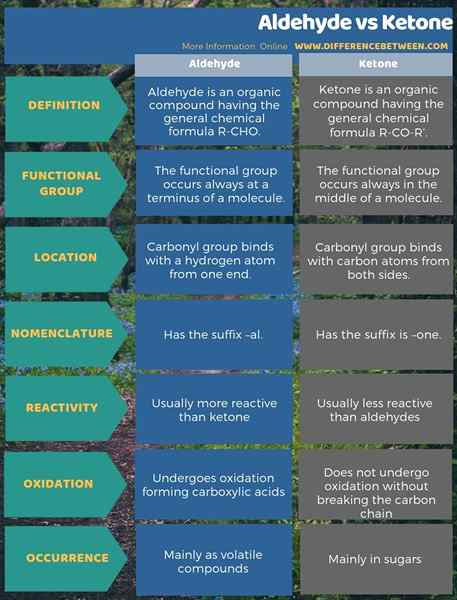
L'aldéhyde est un composé organique ayant la formule chimique générale R-CHO tandis que le cétone est un composé organique ayant la formule chimique générale R-Co-R '. La principale différence entre l'aldéhyde et la cétone est que le groupe fonctionnel d'un aldéhyde se produit toujours à un terminus tandis que le groupe fonctionnel d'une cétone se produit toujours au milieu d'une molécule. De plus, les aldéhydes sont généralement plus réactifs que les cétones.
En tant que autre différence importante entre l'aldéhyde et la cétone, nous pouvons dire que les aldéhydes peuvent subir une oxydation pour former des acides carboxyliques, mais les cétones ne peuvent subir l'oxydation que si nous décomposons ses chaînes de carbone. L'infographie ci-dessous sur la différence entre l'aldéhyde et le cétone présente une comparaison plus détaillée.
Résumé - Aldéhyde vs cétone
Les aldéhydes et les cétones sont des composés organiques. La principale différence entre l'aldéhyde et la cétone est que le groupe fonctionnel d'un aldéhyde se produit toujours à un terminus tandis que le groupe fonctionnel d'une cétone se produit toujours au milieu d'une molécule.
Référence:
1. LibreTexts. «Nomenclature des aldéhydes et des cétones.”Chemistry LibreTexts, National Science Foundation, 2 octobre. 2018. Disponible ici
2. «Cétone.»Wikipedia, Wikimedia Foundation, 7 novembre. 2018. Disponible ici
Image gracieuseté:
1.«Funktionellegruppen Aldehyde» par Mache (Talk) - Propre travaux, (domaine public) via Commons Wikimedia
2.«Ketone-général» (domaine public) via les communes Wikimedia


