Quelle est la différence entre le groupe phosphoryle et le groupe phosphate
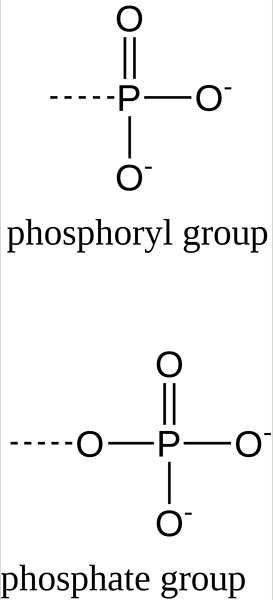
Le Différence clé entre le groupe phosphoryle et le groupe phosphate est que le groupe phosphoryle contient un atome de phosphore lié à trois atomes d'oxygène et à -2 charge, tandis que le groupe phosphate contient un atome de phosphore lié à quatre atomes d'oxygène et à -3 charge.
Le groupe phosphoryle est un ion chimique ayant la formule chimique P+O32- tandis que le groupe phosphate est un anion ayant la formule chimique Po4-3.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que le groupe phosphoryle
3. Qu'est-ce que le groupe phosphate
4. Groupe phosphoryle vs groupe phosphate sous forme tabulaire
5. Résumé - groupe phosphoryle vs groupe phosphate
Qu'est-ce que le groupe phosphoryle?
Le groupe phosphoryle est un ion chimique ayant la formule chimique P+O32-. Par conséquent, cet ion contient des atomes de phosphore et d'oxygène. Il peut exister dans différents états de protonation. Ce terme est utilisé principalement pour les composés chimiques constitués d'un groupe phosphoryle attaché à un autre atome, comme le composé de chlorure de phosphoryle, qui contient un groupe de phosphoryle attaché à un chlorure d'anion. Ce terme est également utile pour décrire les mécanismes catalytiques tels que la phosphorylation.
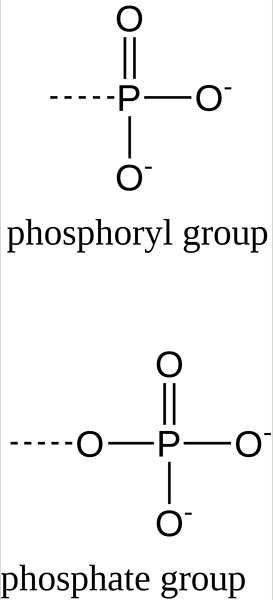
Figure 01: La formule chimique du groupe phosphoryle et du groupe phosphate
Lorsque vous envisagez les processus biochimiques, si un groupe phosphate est impliqué dans une réaction, un groupe phosphoryle est généralement transféré entre les composés substrat. Ces réactions sont connues sous le nom de réactions de transfert de phosphoryle. Cependant, un groupe phosphoryle n'est pas un groupe phosphate.
Qu'est-ce que le groupe phosphate?
Un groupe de phosphate est un anion ayant la formule chimique PO4-3. Ce terme peut être utilisé pour nommer Am anion, composés de sel contenant un groupe de phosphate, un groupe fonctionnel et les esters contenant le groupe phosphate. Le plus souvent, nous appelons cet anion un anion orthophosphate car il se forme à partir de l'acide orthophosphorique.
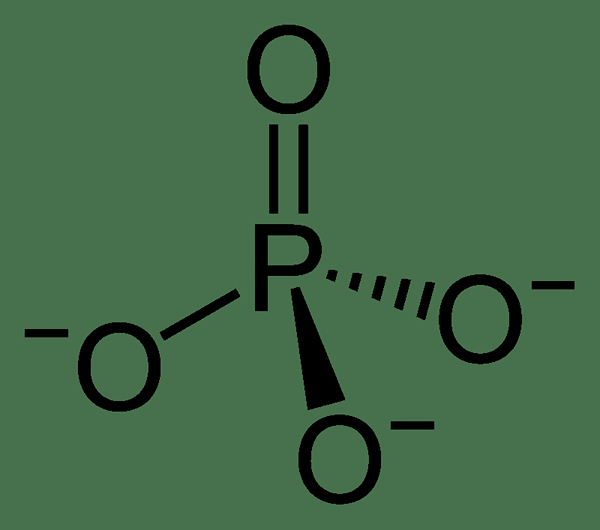
Figure 02: La structure chimique du groupe phosphate
Cet anion se forme à partir de l'acide phosphorique par l'élimination de trois protons. L'élimination d'un proton forme l'anion de dihydrogène phosphate, tandis que l'élimination de deux protons forme l'anion à l'hydrogène phosphate. Ces noms peuvent être utilisés pour désigner leurs composés de sel correspondants.
La masse molaire de l'anion phosphate est 94.97 g / mol. Il y a un atome de phosphore central lié à quatre atomes d'oxygène, et l'anion a une géométrie tétraédrique. La plupart des composés contenant du phosphate sont des substances solubles dans l'eau à température ambiante et à la pression. Certains composés de phosphate sont également insolubles dans l'eau.
Dans les systèmes biologiques, nous pouvons trouver principalement des groupes de phosphate sous forme de phosphate inorganique. Nous pouvons trouver des anions de phosphate libre dans des solutions dans les systèmes biologiques. Sinon, les anions de phosphate se produisent liés à des molécules organiques sous forme d'organophosphates. Généralement, les phosphates peuvent être trouvés comme esters dans les nucléotides, dans l'ADN et dans l'ARN.
Quelle est la différence entre le groupe phosphoryle et le groupe phosphate?
Le groupe phosphoryle est un ion chimique ayant la formule chimique P+O32- Alors que le groupe phosphate est un anion ayant la formule chimique Po4-3. La principale différence entre le groupe phosphoryle et le groupe phosphate est que le groupe phosphoryle contient un atome de phosphore lié à trois atomes d'oxygène et à la charge -2, tandis que le groupe phosphate contient un atome de phosphore lié à quatre atomes d'oxygène et à -3 charge.
La figure suivante présente la différence entre le groupe phosphoryle et le groupe phosphate sous forme tabulaire.
Résumé - groupe phosphoryle vs groupe phosphate
Un groupe phosphoryle est un ion chimique ayant la formule chimique P+O32-. Pendant ce temps, le groupe phosphate est un anion ayant la formule chimique PO4-3. La principale différence entre le groupe phosphoryle et le groupe phosphate est que le groupe phosphoryle contient un atome de phosphore lié à trois atomes d'oxygène et à la charge -2, tandis que le groupe phosphate contient un atome de phosphore lié à quatre atomes d'oxygène et à -3 charge.
Référence:
1. «Groupe de phosphate: définition et explication." Étude.com.
Image gracieuseté:
1. «Groupe de phosphoryle-groupe et phosphate» par Stater - généré avec ChemDraw (CC BY-SA 3.0) via Commons Wikimedia
2. «Phosphat-ion» par Neurotiker ⇌ - Propre travaux (domaine public) via Commons Wikimedia


