Différence entre l'analyse volumétrique et gravimétrique
Le différence clé entre l'analyse volumétrique et gravimétrique est que le L'analyse volumétrique mesure la quantité d'un analyte en utilisant le volume tandis que l'analyse gravimétrique mesure la quantité d'un analyte en utilisant du poids.
Dans une analyse, nous mesurons la quantité d'un composé inconnu avec l'utilisation d'une quantité connue d'un composé connu. Nous pouvons prendre cette quantité en tant que volume ou comme un poids. S'il s'agit de volume, nous l'appelons «analyse volumétrique» ou «Analyse titrimétrique". Si c'est du poids, nous l'appelons «analyse gravimétrique». Les deux sont des techniques analytiques quantitatives car ces techniques peuvent mesurer la quantité d'un échantillon.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que l'analyse volumétrique
3. Qu'est-ce que l'analyse gravimétrique
4. Comparaison côte à côte - Analyse volumétrique vs gravimétrique sous forme tabulaire
5. Résumé
Qu'est-ce que l'analyse volumétrique?
L'analyse volumétrique est un type d'analyse quantitative dans laquelle nous pouvons mesurer la quantité d'un composé inconnu en utilisant son volume. Nous pouvons utiliser des titrages à cet effet. Par conséquent, nous appelons cette analyse une «analyse titrimétrique». Dans un titrage, nous utilisons une deuxième solution ou un réactif pour la détermination du volume du composé inconnu présent dans un échantillon. En déterminant le volume de l'inconnu, nous pouvons déterminer la concentration de ce composé dans l'échantillon.
Analyse volumétrique pour un titrage
Pour un titrage, il y a plusieurs composants dont nous avons besoin dans le système expérimental. Ces composants comprennent une bureautte, un porte-bureau. En règle générale, nous remplissons le réactif (ayant une concentration connue) dans la bureautte et devons prendre l'échantillon (contenant le composé inconnu) dans le bécher (un volume connu). De plus, nous devons utiliser des indicateurs pour la détermination du point final du titrage. De plus, il est important de choisir le bon indicateur pour un titrage particulier selon la plage de pH dans laquelle nous faisons le titrage. Ex: L'indicateur phénolphthalein fonctionne à la plage de pH de 8.3-10.0. L'indicateur donne un changement de couleur au point final. Ex: la couleur de la phénolphtaleine à pH 8.3 est incolore, et à pH 10.0, il montre une couleur rose pâle.

Figure 01: une titration acide-base
De plus, le deuxième réactif que nous remplissons dans la bureautte devrait avoir une réaction considérable afin de donner un point de terminaison (sauf s'il ne donne pas de point final ou de changement de couleur de l'indicateur). Ce que nous mesurons, c'est le volume du réactif (dans la bureautte) qui réagit avec le composé de l'échantillon. Nous pouvons utiliser des relations stoechiométriques pour déterminer les moles de l'inconnu présent dans l'échantillon en utilisant l'équation suivante.
C1v1 = C2v2
Ici, C1 est la concentration du réactif dans la bureautte, V1 est le volume du réactif qui réagit avec l'échantillon, C2 est la concentration inconnue de l'échantillon, et V2 est le volume de l'échantillon que nous avons prélevé dans le bécher pour le béche analyse.
Qu'est-ce que l'analyse gravimétrique?
L'analyse gravimétrique est un type d'analyse quantitative dans laquelle nous pouvons déterminer le poids d'un composé inconnu dans un échantillon. Cette méthode implique des réactions de précipitation pour la séparation du composé souhaité d'un échantillon. Une réaction de précipitations peut convertir un composé dissous en précipité que nous pouvons peser. Si l'échantillon est un mélange de plusieurs solides, nous pouvons d'abord dissoudre l'échantillon dans un solvant approprié, puis nous pouvons ajouter un réactif approprié qui peut précipiter le composé dont nous avons besoin. Nous l'appelons un agent précipitant. Finalement, nous pouvons séparer le précipité par filtration et peser.
Plus important encore, l'agent précipitant ne doit précipiter que le composé requis. De plus, la filtration de la devrait laver tous les autres constituants autres que le composé requis. Pour l'élimination des constituants indésirables qui sont encore présents sur le précipité, nous pouvons laver le précipité à l'aide d'eau ou tout autre solvant qui ne dissout pas le précipité. Ensuite, nous pouvons sécher le précipité et peser.

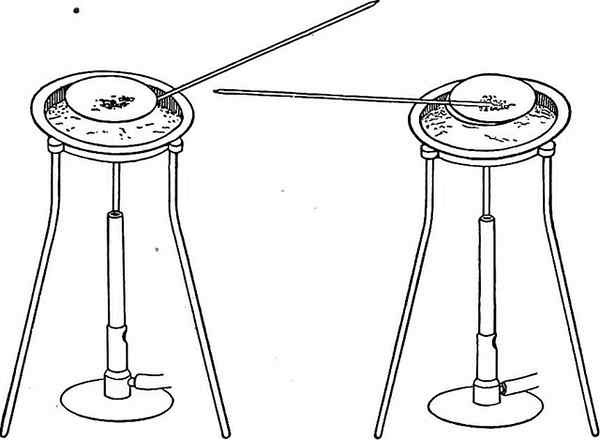
Figure 02: Évaporation des composés volatils afin d'isoler le précipité
Outre les précipitations, nous pouvons analyser un composé en évaporant les composants volatils de l'échantillon à une température appropriée. Nous pouvons le faire en chauffant ou en décomposant chimiquement l'échantillon. La volatilisation peut être directe ou indirecte. L'allumage est un exemple de méthode directe. Un exemple de méthode indirecte est la mesure de la perte de la teneur en eau de l'échantillon pendant le traitement thermique.
Quelle est la différence entre l'analyse volumétrique et gravimétrique?
L'analyse volumétrique est un type d'analyse quantitative dans laquelle nous pouvons mesurer la quantité d'un composé inconnu en utilisant son volume. Il mesure le volume du composé souhaité dans les unités de volume telles que L (litres), ML, M3 ou dm3. L'analyse gravimétrique est un type d'analyse quantitative dans laquelle nous pouvons déterminer le poids d'un composé inconnu dans un échantillon. Il mesure la masse du composé souhaité dans les unités de MAS telles que Mg, G et Kg. C'est la principale différence entre l'analyse volumétrique et gravimétrique.
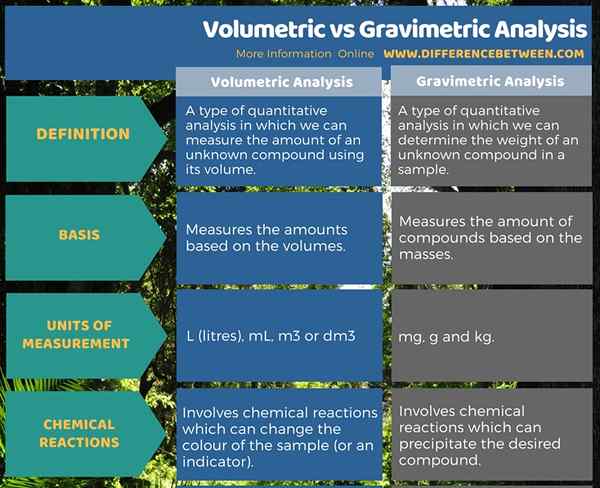
Résumé - Analyse volumétrique vs gravimétrique
Nous pouvons déterminer la quantité d'un composé qui est présent dans un échantillon donné en utilisant une analyse volumétrique ou une analyse gravimétrique. La différence entre l'analyse volumétrique et gravimétrique est que l'analyse volumétrique (ou Analyse titrimétrique) mesure la quantité d'un analyte en utilisant le volume tandis que l'analyse gravimétrique mesure la quantité d'un analyte en utilisant le poids.
Référence:
1. Britannica, les éditeurs de l'Encyclopaedia. "Analyse volumètrique.”Encyclopædia Britannica. Encyclopædia Britannica, Inc., 24 juin 2014. Disponible ici
2. Britannica, les éditeurs de l'Encyclopaedia. "Analyse gravimétrique.»Encyclopædia Britannica, Encyclopædia Britannica, Inc., 17 avril. 2018. Disponible ici
Image gracieuseté:
1.'PHENOLPHTHALEIN IN FLASK'BY 384 - Propre travaux, (CC BY-SA 4.0) via Commons Wikimedia
2.'14765613865' par Internet Archive Book Images via Flickr


